تکنیک ها, میکروبیولوژی, ویدیو های آموزشی
تست آنتی بیوگرام
Disk diffusion test
تست انتشار دیسکی
تست انتشار دیسک که همچنین به عنوان تست انتشار آگار(agar diffusion test)، تست کربی باوئر(Kirby–Bauer test)، تست حساسیت آنتی بیوتیکی انتشار دیسک(disc-diffusion antibiotic susceptibility test)، تست حساسیت آنتی بیوتیکی انتشار دیسک(disc-diffusion antibiotic sensitivity test) و تست KB(KB test) نیز شناخته میشود یک سنجش میکروبیولوژیکی مبتنی بر کشت است که در آزمایشگاههای تشخیصی و سنتز دارو استفاده میشود.
در آزمایشگاههای تشخیصی، این روش برای تعیین حساسیت باکتریهای جدا شده از عفونت بیمار به آنتی بیوتیک های تایید شده بالینی استفاده میشود. این به پزشکان اجازه میدهد تا مناسب ترین درمان آنتی بیوتیکی را تجویز کنند. در آزمایشگاههای کشف دارو، بهویژه آزمایشگاههای اکتشاف زیستی، از این روش برای غربالگری مواد بیولوژیکی (مانند عصارههای گیاهی، براث های تخمیر باکتریایی) و کاندیدهای دارویی برای فعالیت ضد باکتریایی استفاده میشود. هنگام کاوش زیستی، سنجش را میتوان با سویههای جفتی از باکتریها برای دستیابی به تکثیر زدایی و شناسایی موقت مکانیسم اثر ضد باکتریایی انجام داد.
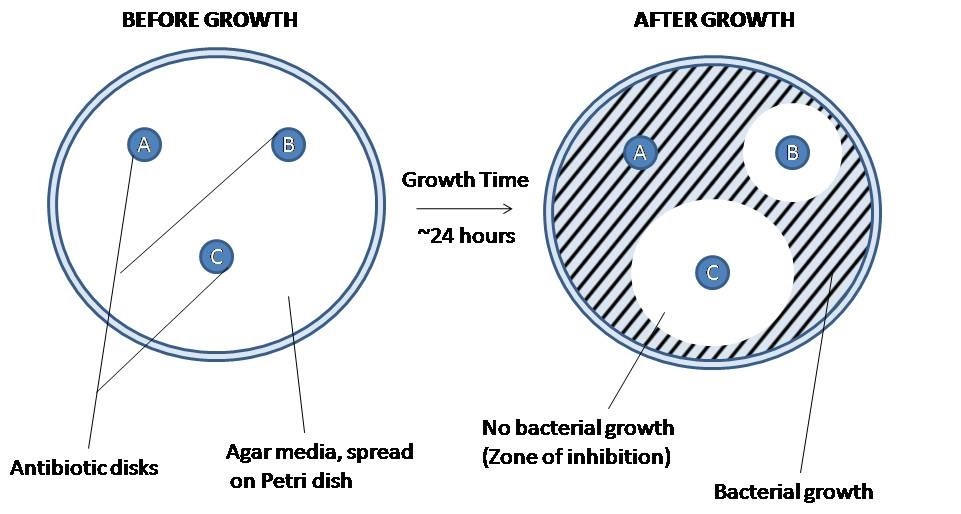
در آزمایشگاههای تشخیصی، آزمایش با تلقیح سطح پلیت آگار با باکتریهای جدا شده از عفونت بیمار انجام میشود. سپس دیسک های کاغذی حاوی آنتی بیوتیک روی آگار اعمال میشود و پلیت انکوبه میشود. اگر یک آنتی بیوتیک رشد باکتری را متوقف کند یا باکتری را از بین ببرد، ناحیهای در اطراف دیسک وجود خواهد داشت که در آن باکتری به اندازه کافی رشد نکرده است که قابل مشاهده باشد. به این ناحیه، منطقه بازداری میگویند.
سپس میتوان با مقایسه اندازه این مناطق بازدارندگی با پایگاههای اطلاعاتی در مورد باکتریهای حساس به آنتیبیوتیک، نسبتاً حساس و مقاوم، حساسیت باکتری به هر آنتیبیوتیک را به صورت نیمه کمی تعیین کرد. به این ترتیب می توان مناسب ترین آنتی بیوتیک را برای درمان عفونت بیمار شناسایی کرد. اگرچه آزمایش دیفیوژن دیسک را نمی توان برای افتراق فعالیت باکتریواستاتیک و باکتری کش استفاده کرد، اما نسبت به سایر روشهای تست حساسیت مانند رقیق سازی براث، کمتر دشوار است.
در آزمایشگاه های تشخیصی، از تست انتشار دیسک برای تعیین حساسیت بالینی باکتری ها به آنتی بیوتیک های مختلف استفاده می شود. یک آنتی بیوتیک موثر منطقه بزرگی از بازدارندگی (دیسک C)را ایجاد می کند، در حالی که یک آنتی بیوتیک بی اثر ممکن است اصلاً بر رشد باکتری تأثیر نگذارد (دیسک A). آنتی بیوتیک هایی که یک ایزوله باکتری تا حدی به آن حساس است، یک ناحیه مهاری با اندازه متوسط ایجاد می کند (دیسک B)
در آزمایشگاههای کشف دارو، آزمایش انتشار دیسک کمی متفاوت از آزمایشگاههای تشخیصی انجام میشود. در این روش، این سویه باکتری نیست که باید مشخص شود، بلکه یک عصاره آزمایشی (به عنوان مثال یک گیاه یا عصاره میکروبی) است. بنابراین پلیت آگار با یک سویه باکتریایی با فنوتیپ شناخته شده (اغلب سویه ATCC یا NCTC) تلقیح میشود و دیسک های حاوی عصاره آزمایش روی سطح اعمال میشود.
اندازه منطقه بازدارندگی را نمیتوان به عنوان یک معیار نیمه کمی برای قدرت ضد باکتری استفاده کرد زیرا عصارههای مختلف حاوی مولکولهایی با ویژگیهای انتشار متفاوت (اندازه های مولکولی مختلف، آب دوستی و غیره) هستند. با این وجود، میتوان از اندازههای ناحیه بازدارنده به منظور حذف مجدد استفاده کرد. این امر با آزمایش هر عصاره در برابر سویههای جفت باکتری (مانند سویههای حساس و مقاوم به استرپتومایسین برای شناسایی عصارههای حاوی استرپتومایسین) به دست میآید. سویه های جفتی (مانند گونه های وحشی و سویه های دارای بیان بیش از حد هدف) نیز می توانند برای شناسایی مکانیسم اثر ضد باکتریایی استفاده شوند.
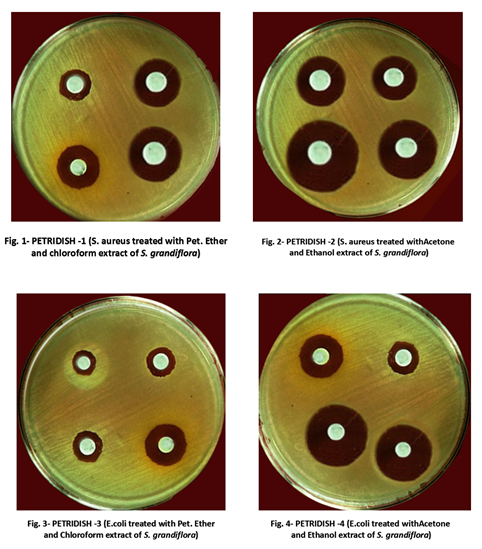
در آزمایشگاههای کشف دارو، از آزمایش انتشار دیسک برای غربالگری عصارههای محصول طبیعی از نظر فعالیت ضد باکتریایی استفاده میشود. عصارههایی با فعالیت ضد باکتریایی، به عنوان مثال عصارههای نفتی اتر، کلروفرم، اتانول و استون در بالا، یک منطقه بازدارندگی ایجاد میکنند.
تاریخچه
انتشار آگار برای اولین بار توسط Martinus Beijerinck در سال 1889 برای مطالعه اثر اکسینها بر رشد باکتریها استفاده شد. با این حال، این روش توسط بسیاری از دانشمندان و سازمانهای علمی در طول سالها توسعه، پالایش و استانداردسازی شده است.
اصول
کشت خالص باکتری در سالین معلق میشود، کدورت آن استاندارد میشود و به طور یکنواخت روی پلیت آگار قرار میگیرد. سپس یک دیسک کاغذ صافی آغشته به آنتی بیوتیک یا عصاره روی سطح آگار قرار می گیرد. مواد تشکیل دهنده دیسک از کاغذ صافی به داخل آگار پخش میشود. غلظت این ترکیبات در کنار دیسک بالاترین مقدار خواهد بود و با افزایش فاصله از دیسک کاهش مییابد.
اگر آنتی بیوتیک یا عصاره در غلظت معینی در برابر باکتری ها موثر باشد، هیچ کلونی در جایی که غلظت در آگار بیشتر یا مساوی غلظت موثر باشد رشد نخواهد کرد. این منطقه مهار است. به طور کلی، مناطق بازدارندگی بزرگتر با حداقل غلظت مهاری کمتر (MICs) آنتی بیوتیک یا عصاره برای آن سویه باکتریایی مرتبط است. یک استثنا در این مورد زمانی است که مولکولهای آنتیبیوتیک یا عصاره بزرگ یا آبگریز هستند، زیرا به آرامی در آگار پخش میشوند.
تست استاندارد کربی-بائر: دیسکهای سفید حاوی آنتیبیوتیکها روی صفحه آگار باکتری نشان داده شده است. مناطق دایره ای از رشد ضعیف باکتری ها اطراف برخی دیسک ها را احاطه کرده است که نشان دهنده حساسیت به آنتی بیوتیک است.
روشهای استاندارد
آماده سازی پلیت آگار و تلقیح
تمام جنبههای روش کربی-بائر برای اطمینان از نتایج منسجم و دقیق استاندارد شده است. به همین دلیل، یک آزمایشگاه باید این استانداردها را رعایت کند. محیط مورد استفاده در آزمایش کربی باوئر باید آگار مولر-هینتون با عمق 4 میلی متر باشد که در ظروف پتری 100 یا 150 میلی متری ریخته شود. سطح pH آگار باید بین 7.2 تا 7.4 باشد. تلقیح باکتری با رقیق کردن یک محیط کشت براث برای مطابقت با استاندارد کدورت 0.5 مک فارلند، که معادل تقریباً 150 میلیون سلول در هر میلی لیتر است، تهیه میشود.
تلقیح و انکوبه کردن
با استفاده از روش آسپتیک، کشت براث یک ارگانیسم خاص با یک سواب استریل جمع آوری میشود. در مورد باکتریهای گرم منفی، مایع اضافی با فشار دادن یا چرخاندن ملایم سواب به سمت داخل لوله خارج میشود. سپس سواب روی صفحه آگار مولر-هینتون قرار میگیرد تا یک چمن باکتریایی تشکیل شود. برای به دست آوردن رشد یکنواخت، صفحه آگار را با سواب در یک جهت رگه میزنند، 120 درجه میچرخانند و دوباره رگه میزنند، 120 درجه دیگر میچرخانند و دوباره رگه میزنند.
سپس با استفاده از یک دیسک پخش کننده آنتی بیوتیک، دیسکهای حاوی آنتی بیوتیک های خاص روی پلیت اعمال میشود. این کار باید ظرف 15 دقیقه پس از تلقیح انجام شود. فورسپس(forceps) استریل شده با شعله برای فشار دادن به آرامی هر دیسک روی آگار و اطمینان از اتصال آن استفاده میشود. سپس پلیتها در طول شب و معمولاً در دمای 35 درجه سانتیگراد انکوبه میشوند. پلیتها باید ظرف 15 دقیقه پس از استفاده از دیسکهای آنتی بیوتیک انکوبه شوند.
روشهای جایگزین
انواع مختلفی از روش انتشار دیسک ایجاد شده است، از جمله روشهای Oxford penicillin cup و Etest که در آزمایشگاههای تشخیصی بیمارستانی استفاده میشوند، و روشهای انتشار چاه، انتشار سیلندر و بیواتوگرافی مورد استفاده در آزمایشگاههای کشف و توسعه دارو.






برای تست آنتی بیوگرام میکروب سل
جهت استعلام قیمت و جزئیات با ما تماس بگیرید