بیماری ها
لوسمی دوران کودکی (Childhood Leukemia) چیست؟
سرطان زمانی شروع میشود که سلولهای بدن شروع به رشد خارج از کنترل میکنند. تقریباً سلولهای موجود در هر قسمت از بدن میتوانند به سرطان تبدیل شوند. لوسمیها سرطانهایی هستند که از سلولهایی شروع میشوند که به طور معمول به انواع مختلف سلولهای خونی تبدیل میشوند. اغلب، لوسمی در اشکال اولیه گلبولهای سفید شروع میشود اما برخی از سرطان خونها در انواع دیگر سلولهای خونی نیز آغاز میشوند.
انواع سرطان خون در کودکان
انواع مختلفی از لوسمی وجود دارد که عمدتاً بر اساس موارد زیر دسته بندی میشوند:
- اگر لوسمی حاد (با رشد سریع) یا مزمن (با رشد کندتر) باشد.
- اگر لوسمی در سلولهای میلوئیدی یا سلولهای لنفوئیدی شروع شود.
دانستن نوع خاص سرطان خون یک کودک میتواند به پزشکان کمک کند تا وضعیت آتی (چشم انداز) هر کودک را بهتر پیش بینی کرده و بهترین درمان را برای وی انتخاب کنند.
لوسمیهای حاد (Acute leukemias)
بیشتر لوسمیهای دوران کودکی حاد هستند. این لوسمیها میتوانند به سرعت پیشرفت کنند و معمولاً باید فوراً درمان شوند. انواع اصلی لوسمی حاد عبارتند از:
- لوسمی حاد لنفوسیتی (لنفوبلاستیک) (ALL): از هر 4 لوسمی دوران کودکی، 3 مورد آن ALL است. این لوسمیها در اشکال اولیه گلبولهای سفید خون به نام لنفوسیتها (lymphocytes) شروع میشوند.
- لوسمی حاد میلوئیدی (AML): این نوع لوسمی که به آن لوسمی حاد میلوژن (acute myelogenous leukemia)، لوسمی حاد میلوسیتیک (acute myelocytic leukemia) یا لوسمی حاد غیر لنفوسیتی (acute non-lymphocytic leukemia) نیز گفته میشود، بیشتر موارد باقی مانده از لوسمی دوران کودکی را تشکیل میدهد. AML از سلولهای میلوئیدی شروع میشود که به طور معمول گلبولهای سفید (به غیر از لنفوسیتها)، گلبولهای قرمز خون یا پلاکتها را تشکیل میدهند.
به ندرت، لوسمیهای حاد میتوانند دارای ویژگیهای ALL و AML باشند. به این لوسمیهای ترکیبی، لوسمیهای تمایز نیافته حاد (acute undifferentiated leukemias) یا لوسمیهای حاد فنوتیپ مختلط (MPAL) میگویند. به طور کلی در کودکان با این بیماریها مانند ALL رفتار میشود و معمولاً به درمان نیز مانند ALL پاسخ میدهند.
هر دو ALL و AML دارای انواع فرعی هستند.
لوسمیهای مزمن (Chronic leukemias)
بروز لوسمی مزمن در کودکان نادر است. این لوسمیها نسبت به لوسمیهای حاد آهسته تر رشد میکنند اما درمان آنها نیز سخت تر است. لوسمیهای مزمن را میتوان به 2 نوع اصلی تقسیم کرد:
- لوسمی میلوئیدی مزمن (CML): که به آن لوسمی میلوژن مزمن (chronic myelogenous leukemia) نیز گفته میشود. CML در کودکان نادر است. درمان این بیماری مشابه درمان آن در بزرگسالان است.
- لوسمی لنفوسیتی مزمن (CLL): این لوسمی در کودکان بسیار نادر است.
لوسمی میلومونوسیتی نوجوانان (Juvenile myelomonocytic leukemia یا JMML)
این نوع نادر لوسمی نه مزمن است و نه حاد. در سلولهای میلوئیدی شروع میشود اما معمولاً به سرعت AML یا به کندی CML رشد نمیکند. اغلب در کودکان خردسال (متوسط سن 2 سال) رخ میدهد. علائم این بیماری میتواند شامل رنگ پریدگی پوست، تب، سرفه، کبودی یا خونریزی آسان، مشکل در تنفس (به دلیل تعداد زیاد گلبولهای سفید خون در ریهها)، زوائد پوستی و بزرگ شدن طحال، کبد و غدد لنفاوی باشد.
مغز استخوان، خون و بافت لنفاوی طبیعی
برای درک لوسمی، دانستن اطلاعاتی در مورد مغز استخوان، خون و سیستم لنفاوی به شما کمک میکند.
مغز استخوان (Bone marrow)
مغز استخوان بخش داخلی نرم برخی از استخوانها است. از سلولهای خون ساز، سلولهای چربی و بافتهای حمایت کننده تشکیل شده است. تعداد کمی از سلولهای سازنده خون را سلولهای بنیادی خون (blood stem cells) تشکیل میدهند.
سلولهای بنیادی خون برای ساخت سلولهای خونی جدید، یک سری تغییرات را پشت سر میگذارند. در طی این فرآیند، سلولها یا به لنفوسیت (نوعی گلبول سفید) یا سایر سلولهای خون ساز تبدیل میشوند که انواع سلولهای میلوئیدی هستند. سلولهای میلوئیدی میتوانند به گلبولهای قرمز، گلبولهای سفید (به غیر از لنفوسیتها) یا پلاکت تبدیل شوند.
سلولهای قرمز خون (Red blood cells)
گلبولهای قرمز خون (RBCs) اکسیژن را از ریهها به سایر بافتهای بدن حمل میکنند و دی اکسید کربن را به ریهها برمیگردانند تا از این طریق از بدن خارج شود.
پلاکتها (Platelets)
پلاکتها در واقع قطعات سلولی هستند که توسط نوعی سلول مغز استخوان به نام مگاکاریوسیت (megakaryocyte) ساخته میشوند. پلاکتها با بستن سوراخهایی در رگهای خونی در توقف خونریزی حائز اهمیت هستند.
گلبولهای سفید خون (White blood cells)
گلبولهای سفید (WBC) به بدن در مبارزه با عفونتها کمک میکنند. انواع مختلفی از گلبولهای سفید وجود دارد:
- لنفوسیتها (Lymphocytes)، WBCهای بالغی هستند که از لنفوبلاستها (lymphoblasts) – نوعی سلول خون ساز در مغز استخوان – ایجاد میشوند. لنفوسیتها سلولهای اصلی هستند که بافت لنفاوی – بخش عمده ای از سیستم ایمنی – را تشکیل میدهند. بافت لنفاوی در غدد لنفاوی، تیموس (یک اندام کوچک در پشت استخوان سینه)، طحال، لوزهها و آدنوئیدها (adenoids) و مغز استخوان یافت میشود. همچنین این سلولها از طریق دستگاه گوارش و دستگاه تنفسی پراکنده میشود. 2 نوع اصلی لنفوسیت وجود دارد: سلولهای B و سلولهای T. (ALL، شایع ترین نوع لوسمی دوران کودکی، میتواند در سلولهای B یا T شروع شود.
- گرانولوسیتها (Granulocytes)، WBCهای بالغی هستند که از میلوبلاستها (myeloblasts) – نوعی سلول خون ساز در مغز استخوان – ایجاد میشوند. گرانولوسیتها دارای گرانولهایی هستند که به صورت لکههایی در زیر میکروسکوپ دیده میشوند. این گرانولها حاوی آنزیمها و سایر موادی هستند که میتوانند میکروبهایی مانند باکتریها را از بین ببرند. 3 نوع گرانولوسیت – نوتروفیلها (neutrophils)، بازوفیلها (basophils) و ائوزینوفیلها (eosinophils) – در زیر میکروسکوپ با اندازه و رنگ گرانولهایشان از هم متمایز میشوند.
- مونوسیتها (Monocytes) از مونوبلاستهای خون ساز در مغز استخوان ایجاد شده و به گرانولوسیتها مربوط میشوند. پس از حدود یک روز گردش در خون، مونوسیتها وارد بافتهای بدن میشوند تا به ماکروفاژ (macrophages) تبدیل شوند که میتواند با احاطه و هضم برخی میکروبها، آنها را از بین ببرد.
شروع و گسترش لوسمی در بدن
لوسمی از مغز استخوان شروع میشود. سلولهای لوسمی میتوانند در آن جا تجمع پیدا کنند و سلولهای طبیعی را از بین ببرند. اغلب، سلولهای سرطانی خون نسبتاً سریع به جریان خون میریزند. همچنین برخی از انواع سرطان خون میتوانند به سایر قسمتهای بدن مانند غدد لنفاوی، طحال، کبد، سیستم عصبی مرکزی (مغز و نخاع)، بیضهها یا سایر اندامها سرایت کنند.
برخی دیگر از سرطانهای دوران کودکی، مانند نوروبلاستوما (neuroblastoma) یا رابدومیوسارکوما (rhabdomyosarcoma)، از سایر اندامها شروع میشوند و میتوانند به مغز استخوان سرایت کنند اما این سرطانها دیگر لوسمی نیستند.
آمار کلیدی برای لوسمی دوران کودکی
سرطان خون شایع ترین سرطان در کودکان و نوجوانان است که تقریباً از هر 3 سرطان 1 مورد را شامل میشود. با این حال، به طور کلی، لوسمی دوران کودکی یک بیماری نادر است.
از هر 4 لوسمی در کودکان و نوجوانان، 3 مورد آن لوسمی لنفوسیتی حاد (ALL) است. بیشتر موارد باقی مانده لوسمی حاد میلوئیدی (AML) است.
- ALL در اوایل دوران کودکی شایع است و بین 2 تا 5 سالگی به اوج خود میرسد.
- AML بیشتر در سالهای کودکی گسترش مییابد اما در 2 سال اول زندگی و در طول سالهای نوجوانی کمی شایع تر است.
- ALL در میان کودکان اسپانیایی و سفید پوست کمی بیشتر از کودکان آفریقایی-آمریکایی و آسیایی-آمریکایی شایع است و در پسران بیشتر از دختران رخ میدهد.
- AML به طور مساوی در بین پسران و دختران از همه نژادها رخ میدهد.
لوسمی مزمن در کودکان نادر است. بیشتر آنها لوسمی میلوئیدی مزمن (CML) هستند که در نوجوانان بیشتر از کودکان کوچکتر رخ میدهد.
لوسمی میلومونوسیتی نوجوانان (JMML) نیز نادر است. این بیماری معمولاً در کودکان خردسال با میانگین سنی حدود 2 سال رخ میدهد و در پسران کمی بیشتر از دختران دیده میشود.
علائم و نشانههای لوسمی دوران کودکی
بسیاری از علائم لوسمی دوران کودکی میتواند دلایل دیگری نیز داشته باشد و اغلب این علائم ناشی از سرطان خون نیستند. با این حال، اگر کودک شما هر یک از آنها را دارد، مهم است که با او به پزشک مراجعه کنید تا بتوان علت را پیدا کرده و در صورت نیاز آن را درمان کرد.
سرطان خون در مغز استخوان – جایی که سلولهای خونی جدید ساخته میشود -شروع میشود. علائم لوسمی اغلب به دلیل وجود مشکلاتی در مغز استخوان ایجاد میشود. همان طور که سلولهای سرطانی خون در مغز آن ساخته میشوند، میتوانند سلولهای طبیعی خون را از بین ببرند. در نتیجه، ممکن است یک کودک گلبولهای قرمز طبیعی، گلبولهای سفید و پلاکتهای خونی کافی نداشته باشد. این کمبودها در آزمایش خون خود را نشان میدهند اما میتوانند علائمی نیز ایجاد کنند. سلولهای لوسمی ممکن است به سایر قسمتهای بدن نیز حمله کنند که این کار میتواند علائمی را به همراه داشته باشد.
علائم ناشی از تعداد کم گلبولهای قرمز خون (کم خونی): گلبولهای قرمز خون اکسیژن را به تمام سلولهای بدن حمل میکنند. کمبود گلبولهای قرمز میتواند علائمی مانند موارد زیر را در کودک ایجاد کند:
- احساس خستگی (fatigue)
- احساس ضعف
- احساس سرما
- احساس سرگیجه یا سبکی سر
- تنگی نفس
- پوست رنگ پریده تر
علائم کمبود گلبولهای سفید طبیعی: گلبولهای سفید به بدن کمک میکنند تا با میکروبها مبارزه کند. کودکان مبتلا به لوسمی اغلب تعداد گلبولهای سفید خون بالایی دارن، اما بیشتر آنها سلولهای لوسمی هستند که بدن را در برابر عفونت محافظت نمیکنند و گلبولهای سفید طبیعی نیز به اندازه کافی وجود ندارد. این اتفاق میتواند منجر به بروز موارد زیر شود:
- عفونتهایی که میتوانند به دلیل کمبود گلبولهای سفید طبیعی ایجاد شوند. کودکان مبتلا به لوسمی ممکن است به عفونتهایی مبتلا شوند که به نظر میرسد از بین نمیروند یا ممکن است یکی پس از دیگری فرد را مبتلا کنند.
- اغلب تب علامت اصلی عفونت است. اما برخی از کودکان ممکن است بدون داشتن عفونت تب داشته باشند.
علائم ناشی از تعداد کم پلاکت خون: پلاکتهای موجود در خون به طور معمول به توقف خونریزی کمک میکنند. کمبود پلاکت میتواند منجر به موارد زیر شود:
- کبودی و خونریزی آسان
- خونریزیهای مکرر یا شدید بینی
- خونریزی لثه
درد استخوان یا مفاصل: این درد به دلیل تجمع سلولهای سرطانی خون در نزدیکی سطح استخوان یا داخل مفصل ایجاد میشود.
تورم شکم (belly): سلولهای سرطانی خون میتوانند در کبد و طحال جمع شوند و این اندامها را بزرگتر کنند. این اتفاق ممکن است به صورت پری یا تورم شکم مشاهده شود. دندههای پایینی معمولاً این اندامها را میپوشانند اما وقتی بزرگ میشوند، پزشک اغلب میتواند آنها را احساس کند.
از دست دادن اشتها و کاهش وزن: اگر طحال و یا کبد فرد به اندازه کافی بزرگ شوند، میتوانند به اندامهای دیگری مانند معده فشار وارد کنند. این پدیده میتواند باعث شود که کودک پس از خوردن مقدار کمی غذا احساس سیری کند و به مرور زمان باعث کاهش اشتها و کاهش وزن وی شود.
غدد لنفاوی متورم: برخی از لوسمیها به غدد لنفاوی گسترش مییابند که معمولاً مجموعهای کوچک (به اندازه لوبیا) از سلولهای ایمنی در بدن هستند. گرههای متورم ممکن است به صورت تودههایی در زیر پوست در قسمتهای خاصی از بدن (مانند دو طرف گردن، نواحی زیر بغل، بالای استخوان ترقوه یا کشاله ران) دیده یا احساس شوند. گرههای لنفاوی داخل قفسه سینه یا شکم نیز میتوانند متورم شوند اما این غدد فقط در آزمایشهای تصویر برداری مانند سی تی اسکن یا ام آر آی قابل مشاهده هستند.
در نوزادان و کودکان، غدد لنفاوی اغلب زمانی که با عفونت مبارزه میکنند بزرگتر میشوند. بزرگ شدن غدد لنفاوی در کودک بسیار بیشتر از سرطان خون نشانه عفونت است اما باید توسط پزشک بررسی و به دقت پیگیری شود.
سرفه یا مشکل در تنفس: برخی از انواع سرطان خون میتوانند بر ساختارهای موجود در وسط قفسه سینه، مانند غدد لنفاوی یا تیموس (عضو کوچکی در جلوی نای و لوله تنفسی که به ریهها منتهی میشود) تأثیر بگذارند. بزرگ شدن تیموس یا غدد لنفاوی در قفسه سینه میتواند روی نای فشار بیاورد و باعث ایجاد سرفه یا مشکل تنفسی شود.
در برخی موارد که تعداد گلبولهای سفید خون بسیار زیاد است، سلولهای لوسمی میتوانند در رگهای خونی کوچک ریهها تجمع کنند که خود این پدیده میتواند باعث مشکلات تنفسی نیز شود.
تورم صورت و بازوها: تیموس بزرگ شده ممکن است روی ورید کانا فوقانی (superior vena cava یا SVC) فشار بیاورد. این رگ سیاهرگ بزرگی است که خون را از سر و بازوها به سمت قلب میبرد. این اتفاق میتواند باعث شود که خون در رگها «بازگشت» داده شود که به عنوان سندرم SVC شناخته میشود و میتواند منجر به تورم در صورت، گردن، بازوها و قسمت بالای سینه شود (گاهی اوقات با رنگ پوست مایل به قرمز) شود. علائم همچنین میتواند شامل سردرد، سرگیجه و تغییر در هوشیاری در صورت تاثیر بر مغز باشد. سندرم SVC میتواند تهدید کننده زندگی باشد و بنابراین باید فورا درمان شود.
سردرد، تشنج، استفراغ: تعداد کمی از کودکان مبتلا به نوعی سرطان خون هستند که در ابتدا به مغز و نخاع سرایت کرده است. این حالت میتواند منجر به بروز علائمی مانند سردرد، مشکل در تمرکز، ضعف، تشنج، استفراغ، مشکلات تعادل و تاری دید شود.
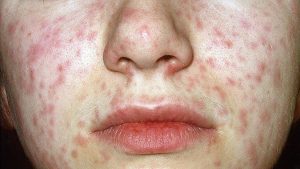
زوائد پوستی یا مشکلات لثه: در کودکان مبتلا به لوسمی میلوئید حاد (AML)، سلولهای لوسمی ممکن است به لثهها گسترش یافته و باعث تورم، درد و خونریزی شوند.
اگر AML به پوست سرایت کند، میتواند لکههای کوچک و تیره ای را ایجاد کند که شبیه زوائد معمولی هستند. مجموعه ای از سلولهای AML در زیر پوست یا در سایر قسمتهای بدن، کلروما (chloroma) یا سارکوم گرانولوسیتی (granulocytic sarcoma) نامیده میشود.
خستگی و ضعف شدید: یک پیامد نادر اما بسیار جدی AML خستگی مفرط، ضعف و ابهام در گفتار است. این علامت میتواند زمانی اتفاق بیفتد که تعداد بسیار زیاد سلولهای لوسمی خون را غلیظ کرده و گردش خون را از طریق رگهای خونی کوچک مغز کند میکند.
باز هم، بیشتر علائم بالا به احتمال زیاد ناشی از چیزی غیر از سرطان خون است. با این حال، مهم است که این علائم توسط پزشک بررسی شود تا در صورت نیاز بتوان علت را پیدا کرده و آن را درمان کرد.
چه چیزی باعث بروز لوسمی دوران کودکی میشود؟
علت دقیق اکثر لوسمیهای دوران کودکی مشخص نیست. اکثر کودکان مبتلا به لوسمی هیچ عامل خطرزای شناخته شدهای ندارند.
با این حال، دانشمندان دریافتهاند که تغییرات خاصی در DNA درون سلولهای طبیعی مغز استخوان میتواند باعث رشد خارج از کنترل آنها و تبدیل شدن به سلولهای سرطانی خون شود. DNA ماده شیمیایی موجود در سلولهای ما است که ژنهای ما را میسازد که عملکرد سلولهای ما را کنترل میکند. ما معمولا شبیه والدین خود هستیم زیرا آنها منبع DNA ما هستند. اما ژنهای ما چیزی بیشتر از ظاهر ما را تحت تأثیر قرار میدهند.
برخی از ژنها زمانی را کنترل میکنند که سلولهای ما رشد میکنند، به سلولهای جدید تقسیم میشوند و در زمان مناسب میمیرند:
- ژنهایی که به رشد، تقسیم یا زنده ماندن سلولها کمک میکنند، انکوژن (oncogenes) نامیده میشوند.
- ژنهایی که به کنترل تقسیم سلولی کمک میکنند یا باعث مرگ سلولها در زمان مناسب میشوند، ژنهای سرکوب کننده تومور (tumor suppressor genes) نامیده میشوند.
سرطانها میتوانند ناشی از جهشهای DNA (یا انواع دیگر تغییرات) باشند که انکوژنها را روشن نگه میدارد یا ژنهای سرکوب کننده تومور را خاموش میکند. این تغییرات ژنی میتواند از والدین به ارث برسد (همان طور که گاهی در مورد لوسمیهای دوران کودکی رخ میدهد)، یا اگر سلولهای بدن هنگام تقسیم شدن برای ساختن سلولهای جدید اشتباه کنند، به طور تصادفی در طول زندگی فرد اتفاق بیفتند.
نوع رایج تغییر DNA که میتواند منجر به لوسمی شود، به عنوان جابجایی کروموزوم (chromosome translocation) شناخته میشود. DNA انسان در 23 جفت کروموزوم بسته بندی شده است. در یک جابجایی، DNA از یک کروموزوم شکسته میشود و به کروموزوم دیگری متصل میشود. نقطه ای از کروموزوم که در آن شکستگی رخ میدهد میتواند بر انکوژنها یا ژنهای سرکوبگر تومور تأثیر بگذارد. به عنوان مثال، جابجایی که تقریباً در تمام موارد لوسمی میلوئیدی مزمن دوران کودکی (CML) و در برخی موارد لوسمی لنفوسیتی حاد دوران کودکی (ALL) مشاهده میشود، مبادله DNA بین کروموزومهای 9 و 22 است که منجر ایجاد چیزی میشود که به عنوان کروموزوم فیلادلفیا (Philadelphia chromosome) شناخته میشود. این اتفاق یک انکوژن به نام BCR-ABL ایجاد میکند که به رشد سلولهای سرطان خون کمک میکند. بسیاری از تغییرات دیگر در کروموزومها یا در ژنهای خاص در لوسمیهای دوران کودکی نیز مشاهده شده است.
جهشهای ژنی ارثی در مقابل اکتسابی
برخی از کودکان جهشهای DNA را از والدین به ارث میبرند که خطر ابتلا به سرطان را در آنها افزایش میدهد. به عنوان مثال، وضعیتی به نام سندرم Li-Fraumeni که از جهش ارثی ژن سرکوبگر تومور TP53 ناشی میشود، خطر ابتلا به سرطان خون و همچنین برخی سرطانهای دیگر را در فرد افزایش میدهد.
برخی از بیماریهای ارثی میتوانند خطر ابتلا به سرطان خون را افزایش دهند اما به نظر نمیرسد که بیشتر لوسمیهای دوران کودکی ناشی از جهشهای ارثی باشند. معمولاً جهشهای DNA مربوط به لوسمی به جای اینکه ارثی باشند، پس از لقاح ایجاد میشوند. برخی از این جهشهای اکتسابی ممکن است در اوایل زندگی، حتی قبل از تولد رخ دهند. در موارد نادر، جهشهای اکتسابی میتوانند در اثر قرار گرفتن در معرض تشعشعات یا مواد شیمیایی سرطانزا ایجاد شوند اما اغلب بدون دلیل ظاهری رخ میدهند.
ترکیبی از عوامل ژنتیکی و محیطی
برخی از مطالعات نشان داده اند که بسیاری از لوسمیهای دوران کودکی ممکن است به دلیل وجود ترکیبی از عوامل ژنتیکی و محیطی ایجاد شوند. مثلا:
ژنهای خاصی به طور معمول نحوه تجزیه بدن و خلاص شدن از شر مواد شیمیایی مضر را کنترل میکنند. برخی از افراد نسخههای متفاوتی از این ژنها دارند که باعث میشود اثر بخشی آنها کاهش یابد. کودکانی که یکی از این تغییرات ژنی را به ارث میبرند، ممکن است در صورت قرار گرفتن در معرض مواد شیمیایی مضر، قادر به تجزیه آنها نباشند. ترکیبی از ژنتیک و قرار گرفتن در معرض عوامل محیطی ممکن است خطر ابتلا به سرطان خون را افزایش دهد.
برخی تحقیقات نشان میدهند که برخی از لوسمیهای دوران کودکی ممکن است ناشی از وجود ترکیبی از تغییرات ژنی خاص همراه با قرار گرفتن در معرض ویروسهای خاص بیش تر از حد طبیعی باشد که در اوایل زندگی اتفاق میافتد. این “عفونت تاخیری” (پس از یک سال اول زندگی) ممکن است سیستم ایمنی بدن را به گونه ای تحت تاثیر قرار دهد که منجر به بروز سرطان خون شود.
تحقیقات در مورد این علل و سایر علل احتمالی سرطان خون در دوران کودکی ادامه دارد. اما در حال حاضر علت بیشتر لوسمیهای دوران کودکی به طور قطع مشخص نیست. علاوه بر این، انواع مختلف لوسمی دوران کودکی ممکن است دلایل متفاوتی داشته باشند.
زیر شاخههای لوسمی دوران کودکی
نوع اصلی و فرعی لوسمی دوران کودکی نقش مهمی در انتخاب گزینههای درمانی و چشم انداز کودک (وضعیت وی در آینده) دارد. تعیین نوع (لوسمی لنفوسیتی حاد (ALL)، لوسمی حاد میلوئیدی (AML) و غیره) و نوع فرعی لوسمی با آزمایش نمونههایی از خون، مغز استخوان و گاهی اوقات غدد لنفاوی یا مایع مغزی نخاعی (CSF) انجام میشود. این موضوع در مبحث آزمایشات برای لوسمی کودکان شرح داده شده است.
اگر در مورد نوع فرعی سرطان خون فرزندتان سؤالی دارید، حتماً از تیم پزشکی خود یا پزشک کودک خود این مسائل را بپرسید.
لوسمی لنفوسیتی حاد (لنفوبلاستیک) (ALL)
لوسمی لنفوسیتی حاد (ALL) یک سرطان با رشد سریع سلولهای لنفوسیت ساز به نام لنفوبلاست است. چندین زیرگروه از ALL وجود دارد که عمدتاً بر اساس موارد زیر دسته بندی شده اند:
- نوع لنفوسیت (بیشتر سلولهای B یا سلول T) که سلولهای لوسمی از آن منشا میگیرند (و اینکه این سلولها چقدر بالغ هستند). این موضوع به عنوان ایمونوفنوتیپ لوسمی (immunophenotype of the leukemia) شناخته میشود.
- اگر سلولهای لوسمی تغییرات ژنی یا کروموزومی خاصی داشته باشند.
ALL سلولB
اغلب در کودکان مبتلا به ALL، لوسمی در اشکال اولیه سلولهای B شروع میشود. چندین زیرگروه از ALL سلول B وجود دارد. ALL سلول B بالغ (که به آن لوسمی بورکیت (Burkitt leukemia) نیز گفته میشود)، یک نوع فرعی نادر است که اساساً همان لنفوم بورکیت (نوعی لنفوم غیر هوچکین یا non-Hodgkin lymphoma) است و به همین روش نیز درمان میشود.
ALL سلولT
این نوع لوسمی، کودکان بزرگتر را بیشتر از ALL سلولهای B تحت تاثیر قرار میدهد. این نوع اغلب باعث بزرگ شدن تیموس (یک اندام کوچک در جلوی نای) میشود که گاهی اوقات میتواند منجر به مشکلات تنفسی شود. همچنین ممکن است در اوایل دوره بیماری به مایع مغزی نخاعی (CSF، مایعی که مغز و نخاع را احاطه کرده است) نیز گسترش یابد.
به غیر از نوع فرعی ALL، عوامل دیگری در تعیین چشمانداز کودک (وضعیت آتی وی) مهم هستند. این موارد در فاکتورهای پیش بینی کننده در لوسمی کودکان نیز توضیح داده شده است.
لوسمی میلوئیدی حاد (AML)
لوسمی حاد میلوئیدی (AML) معمولاً سرطانی با رشد سریع است که در یکی از انواع زیر سلولهای اولیه مغز استخوان (نابالغ) شروع میشود:
- میلوبلاستها: این سلولها به طور معمول گلبولهای سفید خونی به نام گرانولوسیتها (نوتروفیلها، ائوزینوفیلها و بازوفیلها) را تشکیل میدهند.
- مونوبلاستها: این سلولها به طور معمول به گلبولهای سفید به نام مونوسیت و ماکروفاژ تبدیل میشوند.
- اریتروبلاستها (Erythroblasts): این سلولها به گلبولهای قرمز بالغ میشوند.
- مگاکاریوبلاستها (Megakaryoblasts): این سلولها به طور معمول به مگاکاریوسیت تبدیل میشوند، سلولهایی که پلاکتها را میسازند.
AML دارای انواع فرعی است که عمدتاً بر اساس موارد زیر دسته بندی شده اند:
- نوع سلول مغز استخوان که سلولهای لوسمی از آن منشا میگیرند و اینکه سلولها چقدر بالغ هستند (ایمونوفنوتیپ لوسمی).
- اگر سلولهای لوسمی تغییرات ژنی یا کروموزومی خاصی داشته باشند.
- اگر لوسمی مربوط به درمان با سرطان قبلی (با شیمی درمانی یا پرتو درمانی) باشد.
- اگر کودک مبتلا به لوسمی، سندرم داون نیز دارد.
لوسمی پرومیلوسیتیک حاد (APL) یک زیرگروه خاص از AML است. با این نوع لوسمی متفاوت از سایر انواع فرعی AML رفتار میشود و چشم انداز بهتری نیز دارد.
به غیر از نوع فرعی AML، عوامل دیگری در تعیین چشمانداز کودک (وضعیت وی در آینده) مهم هستند. این موارد در فاکتورهای پیش بینی کننده در لوسمی کودکی توضیح داده شده است.
لوسمی میلوئیدی مزمن (CML)
لوسمی میلوئیدی مزمن (CML) معمولاً سرطانی است که رشد کندتر سلولهای مغز استخوان میلوئیدی اولیه (نابالغ) است. CML در کودکان شایع نیست اما ممکن است در آنها نیز رخ دهد.
CML زیرگروه ندارد. در عوض، دوره CML دارای 3 مرحله است که عمدتاً بر اساس تعداد گلبولهای سفید نابالغ – میلوبلاستها (یا بلاستها) – که در خون یا مغز استخوان دیده میشوند، تعیین شده اند. CML گاهی اوقات میتواند در طول زمان به مراحل پیشرفته تر ارتقا یابد.
فاز مزمن CML (Chronic phase)
در این مرحله اولیه، کودکان معمولاً علائم نسبتاً خفیفی دارند (در صورت وجود) و لوسمی معمولاً به درمانهای استاندارد به خوبی پاسخ میدهد. اکثر کودکان در مرحله مزمن هستند که مبتلا به این سرطان تشخیص داده میشوند.
فاز تسریع شده CML (Accelerated phase)
کودکانی که CML آنها در مرحله تسریع شده است ممکن است علائمی مانند تب، تعریق شبانه، کم اشتهایی و کاهش وزن داشته باشند. CML در مرحله تسریع ممکن است به اندازه CML در فاز مزمن به درمان پاسخ ندهد.
فاز تجمع یا بلاست CML (که فاز حاد یا بحران تجمع نیز نامیده میشود)
در این مرحله، سلولهای لوسمی اغلب به بافتها و اندامهای خارج از مغز استخوان گسترش مییابند. کودکان مبتلا به CML در این مرحله اغلب تب، اشتهای ضعیف و کاهش وزن دارند. در این مرحله CML بسیار شبیه یک لوسمی حاد تهاجمی (AML یا در موارد کمتر ALL) عمل میکند.
عوامل خطرزا برای لوسمی دوران کودکی
عامل خطرزا هر چیزی است که بر احتمال ابتلای فرد به بیماری مانند سرطان تأثیر میگذارد. سرطانهای مختلف عوامل خطرزا متفاوتی دارند.
عوامل خطرزا مرتبط با سبک زندگی مانند مصرف دخانیات، رژیم غذایی، وزن بدن و فعالیت بدنی نقش عمده ای در بسیاری از سرطانهای بزرگسالان دارند. اما این عوامل معمولاً سالها طول میکشد تا بر خطر ابتلا به سرطان تأثیر بگذارند و تصور نمیشود که نقش زیادی در سرطانهای دوران کودکی از جمله سرطان خون داشته باشند.
چند عامل خطرزا شناخته شده برای لوسمی دوران کودکی وجود دارد.
عوامل خطرزای ژنتیکی
عوامل خطرزای ژنتیکی آنهایی هستند که بخشی از DNA ما را شامل میشوند (ماده ای که ژنهای ما را میسازد). آنها اغلب از والدین ما به ارث میرسند. در حالی که برخی از عوامل ژنتیکی خطر ابتلا به سرطان خون در دوران کودکی را افزایش میدهند، بیشتر سرطانهای خون به هیچ دلیل ژنتیکی شناخته شده ای مرتبط نیستند.
سندرمهای ژنتیکی
برخی از اختلالات ژنتیکی خطر ابتلای کودک به سرطان خون (لوسمی) را افزایش میدهند:
- سندرم داون (Down syndrome یا تریزومی 21): کودکان مبتلا به سندرم داون یک نسخه (سومین نسخه) اضافی از کروموزوم 21 دارند. احتمال ابتلای این کودکان به لوسمی لنفوسیتی حاد (ALL) یا لوسمی حاد میلوئیدی (AML) بسیار بیشتر از سایر کودکان است (با خطر کلی حدود 2 تا 3 درصد). سندرم داون همچنین با لوسمی گذرا (همچنین به عنوان اختلال میلوپرولیفراتیو گذرا (transient myeloproliferative disorder) شناخته میشود) مرتبط است – یک وضعیت مشابه لوسمی در ماه اول زندگی که اغلب خود به خود و بدون درمان برطرف میشود.
- سندرم Li-Fraumeni: این سندروم یک بیماری ارثی نادر است که در اثر تغییر در ژن TP53 ایجاد میشود. افراد مبتلا به این تغییر در معرض خطر بیشتری برای ابتلا به انواع مختلف سرطان از جمله سرطان خون، سارکوم استخوان یا بافت نرم، سرطان سینه، سرطان غده فوق کلیوی و تومورهای مغزی هستند.
سایر اختلالات ژنتیکی (مانند نوروفیبروماتوز (neurofibromatosis) و کم خونی فانکونی (Fanconi anemia)) نیز خطر ابتلا به سرطان خون و همچنین برخی از انواع دیگر سرطانها را افزایش میدهند.
مشکلات ارثی سیستم ایمنی
برخی از شرایط ارثی باعث میشود کودکانی با مشکلات سیستم ایمنی بدنیا بیایند. این اختلالات شامل موارد زیر است:
- آتاکسی تلانژکتازی (Ataxia-telangiectasia)
- سندرم Wiskott-Aldrich
- سندرم بلوم (Bloom syndrome)
- سندرم شواچمن-دیاموند (Shwachman-Diamond syndrome)
در این کودکان همراه با افزایش خطر ابتلا به عفونتهای جدی ناشی از کاهش دفاع سیستم ایمنی، ممکن است خطر ابتلا به سرطان خون نیز افزایش یابد.
داشتن یک برادر یا خواهر مبتلا به سرطان خون
شانس ابتلا به سرطان خون در خواهران و برادران (Siblings) کودکان مبتلا به لوسمی با شیب ملایمی افزایش مییابد اما خطر کلی هنوز هم پایین است. این خطر در بین دوقلوهای همسان بسیار بیشتر است. اگر یکی از دوقلوها در دوران کودکی به سرطان خون مبتلا شود، دوقلو دیگر نیز تقریباً 1 در 5 احتمال ابتلا به سرطان خون را دارد. اگر سرطان خون در سال اول زندگی ایجاد شود، این خطر بسیار بیشتر است.
به نظر نمیرسد داشتن والدینی که در بزرگسالی به سرطان خون مبتلا شده اند، خطر ابتلا به سرطان خون را در کودک افزایش دهد.
عوامل خطرزای مرتبط با سبک زندگی
عوامل خطرزا مرتبط با سبک زندگی برای برخی از سرطانهای بزرگسالان عبارتند از: سیگار کشیدن، اضافه وزن، نوشیدن بیش از حد الکل و قرار گرفتن بیش از حد در معرض نور خورشید. این نوع عوامل در بسیاری از سرطانهای بزرگسالان مهم هستند اما بعید است که در اکثر سرطانهای دوران کودکی نقشی داشته باشند.
برخی از مطالعات نشان داده اند که مصرف زیاد الکل توسط خانمی در دوران بارداری وی ممکن است خطر ابتلا به سرطان خون را در فرزندش افزایش دهد اما همه مطالعات چنین ارتباطی را پیدا نکرده اند.
عوامل خطرزای زیست محیطی
عوامل خطرزای محیطی تأثیراتی در محیط اطراف ما هستند، مانند تشعشعات و مواد شیمیایی خاص، که خطر ابتلا به بیماریهایی مانند سرطان خون را افزایش میدهند.
قرارگیری در معرض تشعشع
قرار گرفتن در معرض سطوح بالای اشعه یک عامل خطرزا برای ابتلا به لوسمی دوران کودکی است. خطر ابتلا به AML در بازماندگان بمب اتمی ژاپن بسیار بالا بود. اگر جنین در ماههای اول رشد در معرض تشعشعات قرار گیرد، ممکن است خطر ابتلا به سرطان خون در دوران کودکی وی نیز افزایش یابد اما میزان خطر مشخص نیست.
خطرات احتمالی قرار گرفتن جنین یا کودک در معرض سطوح پایین تابش، مانند آزمایشهای اشعه ایکس یا سی تی اسکن، به طور قطع مشخص نیست. برخی از مطالعات افزایش جزئی در میزان خطر ابتلا را پیدا کرده اند، در حالی که برخی دیگر هیچ افزایش خطری را مشاهده نکرده اند. هر گونه افزایش خطر احتمالاً اندک است اما برای ایمن بودن، اکثر پزشکان توصیه میکنند که زنان باردار و کودکان این آزمایشها را انجام ندهند، مگر اینکه کاملاً مورد نیاز باشد.
قرار گرفتن در معرض شیمی درمانی و برخی مواد شیمیایی دیگر
کودکان و بزرگسالانی که برای درمان سایر سرطانها تحت داروهای شیمی درمانی خاص قرار میگیرند، بیشتر در معرض خطر ابتلا به یک سرطان دیگر، معمولاً AML، در اواخر زندگی هستند. داروهایی مانند سیکلوفسفامید (cyclophosphamide)، دوکسوروبیسین (doxorubicin)، اتوپوزید (etoposide) و تنیپوزید (teniposide) با خطر بالاتر سرطان خون مرتبط هستند. این لوسمیها معمولاً در عرض 5 تا 10 سال پس از درمان ایجاد میشوند و معمولاً درمان آنها سخت است.
قرار گرفتن در معرض مواد شیمیایی مانند بنزن (حلالی که در صنعت مواد بهداشتی و پاک کننده و تولید برخی داروها، پلاستیکها و رنگها استفاده میشود) ممکن است باعث سرطان خون حاد در بزرگسالان و به ندرت در کودکان شود. قرار گرفتن در معرض مواد شیمیایی قوی تر با افزایش خطر AML نسبت به ALL مرتبط است.
چندین مطالعه ارتباط احتمالی بین لوسمی دوران کودکی و قرار گرفتن در معرض آفت کشها را در دوران بارداری یا اوایل کودکی پیدا کردهاند. برخی از مطالعات همچنین افزایش احتمالی خطر را در میان مادرانی که قبل از تولد فرزندشان در محل کار در معرض آفت کشها قرار داشته اند، نشان دادهاند. با این حال، اکثر این مطالعات محدودیتهای جدی در روش انجام آنها داشتند. تحقیقات بیشتری برای تأیید این یافتهها و ارائه اطلاعات دقیق تر در مورد خطرات احتمالی مورد نیاز است.
سرکوب سیستم ایمنی
کودکانی که تحت درمان فشرده برای سرکوب سیستم ایمنی خود هستند (عمدتاً کودکانی که پیوند عضو داشتهاند) در معرض خطر ابتلا به برخی سرطانها مانند لنفوم (lymphoma) و ALL هستند.
عوامل خطرزای نامشخص، اثبات نشده یا بحث برانگیز
عوامل دیگری که برای ارتباط احتمالی با لوسمی دوران کودکی مورد مطالعه قرار گرفته اند عبارتند از:
- قرار گرفتن در معرض میدانهای الکترومغناطیسی (مانند زندگی در نزدیکی خطوط برق)
- زندگی در نزدیکی یک نیروگاه هسته ای
- عفونتها (مخصوصاً ناشی از ویروسها) در اوایل زندگی
- سن مادر هنگام تولد فرزند
- سابقه سیگار کشیدن والدین
- قرار گرفتن جنین در معرض هورمونهایی مانند دی اتیل استیل بسترول (DES) یا قرصهای ضد بارداری
- قرار گرفتن پدر در محل کار با مواد شیمیایی و حلالها
- آلودگی شیمیایی آبهای زیرزمینی
تاکنون، اکثر مطالعات ارتباط قوی بین هیچ یک از این عوامل و لوسمی دوران کودکی پیدا نکرده اند اما محققان به مطالعه این عوامل ادامه میدهند.
آیا لوسمی دوران کودکی را میتوان زود تشخیص داد؟
در حال حاضر هیچ آزمایش خون یا سایر آزمایشهای غربالگری برای بیشتر کودکان توصیه نمیشود تا قبل از شروع علائم سرطان خون به دنبال یافتن سرطان خون باشند. لوسمی دوران کودکی اغلب به این دلیل تشخیص داده میشود که کودک علائم یا نشانههایی دارد که باعث مراجعه وی به پزشک شده است. سپس پزشک آزمایشهای خون را تجویز میکند که ممکن است به لوسمی به عنوان علتی برای بروز علائم اشاره کند. بهترین راه برای تشخیص زود هنگام این سرطانها توجه به علائم و نشانههای احتمالی این بیماری است.
برای کودکان در معرض خطر
برای کودکانی که در معرض خطر ابتلا به سرطان خون هستند (برای مثال به دلیل یک بیماری ژنتیکی مانند سندرم Li-Fraumeni یا سندرم داون)، اکثر پزشکان معاینات پزشکی دقیق و منظم و احتمالاً آزمایشهای دیگری را توصیه میکنند. همین امر در مورد کودکانی که برای سایر سرطانها تحت شیمی درمانی و یا پرتو درمانی قرار گرفتهاند و کودکانی که پیوند عضو داشتهاند و داروهای سرکوب کننده سیستم ایمنی مصرف میکنند نیز صادق است. خطر ابتلا به سرطان خون در این کودکان، اگرچه بیشتر از جمعیت عادی است اما هنوز هم اندک است.
آزمایشات لوسمی دوران کودکی
بیشتر علائم و نشانههای لوسمی دوران کودکی به احتمال زیاد علل دیگری مانند عفونت دارند. با این حال، مهم است که پزشک فرزندتان را فوراً از چنین علائمی مطلع کنید تا در صورت نیاز بتوان علت را پیدا کرده و آن را درمان کرد.
معاینات و آزمایشاتی برای تعیین علت علائم انجام خواهد شد. در صورت مشاهده لوسمی، آزمایشات بیشتری برای کشف نوع و نوع فرعی سرطان خون و تصمیم گیری در مورد نحوه درمان آن مورد نیاز است.
تشخیص لوسمی دوران کودکی در اسرع وقت و تعیین نوع سرطان خون بسیار مهم است تا بتوان درمان را به گونه ای تنظیم کرد که بهترین شانس موفقیت را فراهم کند.
تاریخچه پزشکی و معاینه فیزیکی
اگر کودک شما علائم و نشانههایی دارد که نشان میدهد ممکن است سرطان خون داشته باشد، پزشک میخواهد یک تاریخچه پزشکی کامل از شما در اختیار داشته باشد تا در مورد علائم و مدت زمانی که کودک شما آنها را داشته است، مطلع شود. پزشک همچنین ممکن است در مورد قرار گرفتن در معرض عوامل خطرزای احتمالی سوال کند. سابقه خانوادگی سرطان، به ویژه سرطان خون، نیز ممکن است مهم باشد.
در طول معاینه فیزیکی، پزشک هرگونه غدد لنفاوی بزرگ شده، مناطق خونریزی یا کبودی، یا علائم احتمالی عفونت را بررسی میکند. چشمها، دهان و پوست با دقت بررسی میشوند و ممکن است معاینه سیستم عصبی نیز انجام شود. شکم (belly) کودک برای بررسی وجود علائم بزرگ شدن طحال یا کبد معاینه میشود.
آزمایشاتی برای بررسی سرطان خون در کودکان
اگر پزشک فکر میکند که فرزند شما ممکن است سرطان خون داشته باشد، برای اطمینان باید نمونه خون و مغز استخوان بررسی شود. پزشک کودک شما ممکن است برای انجام برخی از این آزمایشات شما را به یک انکولوژیست اطفال ارجاع دهد، پزشکی که در سرطانهای دوران کودکی (از جمله سرطان خون) تخصص دارد. در صورت مشاهده لوسمی، انواع دیگری از آزمایشات نیز ممکن است برای کمک به درمان انجام شوند.
آزمایشات خون
اولین آزمایشاتی که برای بررسی لوسمی انجام میشود، آزمایش خون است. نمونههای خون معمولاً از ورید بازو گرفته میشود اما در نوزادان و کودکان کوچکتر ممکن است از رگهای دیگر (مانند پا یا پوست سر) یا از “انگشتان” نیز گرفته شود.
شمارش خون (Blood counts) و اسمیر خون (blood smears) آزمایشهای معمولی است که روی این نمونهها انجام میشود. شمارش کامل خون (CBC) برای تعیین تعداد سلولهای خونی از هر نوع در خون انجام میشود. برای اسمیر خون، نمونه کوچکی از خون روی یک اسلاید شیشه ای پخش میشود و زیر میکروسکوپ آن را بررسی میکنند. تعداد غیر طبیعی سلولهای خونی و تغییر در ظاهر این سلولها ممکن است پزشک را به وجود سرطان خون مشکوک کند.
اکثر کودکان مبتلا به لوسمی تعداد زیادی گلبول سفید دارند و گلبولهای قرمز و یا پلاکت کافی ندارند. بسیاری از گلبولهای سفید خون به صورت بلاست، نوع اولیه سلولهای خونی هستند که معمولاً فقط در مغز استخوان یافت میشوند. اگرچه این یافتهها ممکن است پزشک را مشکوک به ابتلای کودک به سرطان خون کند، اما معمولاً نمیتوان این بیماری را بدون مشاهده نمونهای از سلولهای مغز استخوان به طور قطعی تشخیص داد.
آسپیراسیون مغز استخوان (Bone marrow aspiration) و بیوپسی یا نمونه برداری (biopsy)
آسپیراسیون و بیوپسی مغز استخوان آزمایشاتی هستند که معمولاً همزمان انجام میشوند. نمونهها معمولاً از پشت استخوانهای لگن (hip) گرفته میشوند اما گاهی اوقات ممکن است از جلوی استخوانهای لگن یا از استخوانهای دیگری نیز برداشته شونزز
قبل از انجام آزمایشات، پوست روی استخوان لگن با تزریق یک بی حس کننده موضعی یا استفاده از کرم بی حس کننده تمیز و بی حس میشود. در بیشتر موارد، به کودک داروهای دیگری نیز داده میشود تا در طول آزمایشها خواب آلود بوده یا حتی بیهوش باشد.
- برای آسپیراسیون مغز استخوان، سپس یک سوزن نازک و تو خالی وارد استخوان میشود و از یک سرنگ برای مکیدن (اسپیراسیون) مقدار کمی از مغز استخوان مایع استفاده میشود.
- بیوپسی مغز استخوان معمولاً درست بعد از آسپیراسیون انجام میشود. یک تکه کوچک از استخوان و مغز آن را با یک سوزن کمی بزرگتر که به پایین و به سمت داخل استخوان فشار داده میشود، بر میدارند. پس از انجام بیوپسی، برای کمک به توقف هرگونه خونریزی، به محل ورود سوزن به بدن فشار وارد میشود.
سپس نمونههای مغز استخوان برای انجام آزمایشات به آزمایشگاه فرستاده میشوند.
آزمایشهای مغز استخوان برای تشخیص سرطان خون استفاده میشوند اما ممکن است بعداً تکرار شوند تا مشخص شود که آیا سرطان خون به درمان پاسخ میدهد یا خیر.
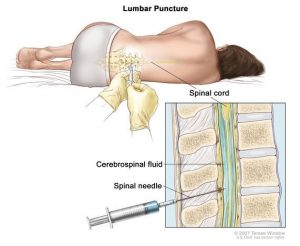
پونکسیون کمری (spinal tap)
این آزمایش برای جستجوی سلولهای لوسمی در مایع مغزی نخاعی (CSF) – که مایعی است که مغز و نخاع را احاطه میکند – استفاده میشود.
برای این آزمایش، پزشک ابتدا یک کرم بی حس کننده را در ناحیهای در قسمت پایین کمر روی ستون فقرات اعمال میکند. پزشک معمولاً به کودک دارویی نیز میدهد تا او را در طول عمل بخواباند. سپس یک سوزن کوچک و تو خالی بین استخوانهای ستون فقرات قرار داده میشود تا مقداری از مایع خارج شود و سپس نمونه برای آزمایش به آزمایشگاه فرستاده میشود.
در کودکانی که قبلاً مبتلا به سرطان خون تشخیص داده شدهاند، از سوراخهای کمری نیز ممکن است برای تزریق داروهای شیمی درمانی به CSF برای جلوگیری یا درمان گسترش سرطان خون به نخاع و مغز استفاده شود. (این عمل به عنوان شیمی درمانی داخل نخاعی (intrathecal chemotherapy) شناخته میشود.)
بیوپسی غدد لنفاوی
این نوع بیوپسی در تشخیص لنفوم مهم است اما به ندرت برای کودکان مبتلا به لوسمی مورد نیاز است.
در طی این روش، جراح پوست را برش میدهد تا کل غدد لنفاوی (که به عنوان بیوپسی اکسیزیونال (excisional biopsy) شناخته میشود) برداشته شود. اگر گره نزدیک سطح پوست باشد، این یک عمل ساده است. اما اگر گره داخل قفسه سینه یا شکم باشد پیچیده تر است. اغلب کودک به بیهوشی عمومی نیاز دارد (حالتی که کودک به خواب فرو میرود).
تستهای آزمایشگاهی برای تشخیص و طبقه بندی لوسمی
تمام نمونههای خون، مغز استخوان و سایر نمونهها برای آزمایشهای بیشتر به آزمایشگاه فرستاده میشوند.
معاینات میکروسکوپی
تمام نمونههای گرفته شده (خون، مغز استخوان، بافت غدد لنفاوی یا CSF) با میکروسکوپ بررسی میشوند. نمونهها ممکن است در معرض مواد شیمیایی (رنگها) قرار بگیرند که میتواند باعث تغییر رنگ در برخی از انواع سلولهای سرطان خون شود.
پزشکان به اندازه، شکل و الگوهای رنگ آمیزی سلولهای خونی در نمونهها نگاه میکنند تا آنها را به انواع خاصی دسته بندی کنند.
یک عنصر کلیدی این است که آیا سلولها بالغ به نظر میرسند (مانند سلولهای خونی طبیعی) یا نابالغ (بدون ویژگیهای سلولهای خونی طبیعی). نابالغ ترین سلولها را بلاست مینامند. وجود بلاستهای بیش از حد در نمونه، به ویژه در خون، نشانه معمولی از وجود سرطان خون است.
ویژگی مهم نمونه مغز استخوان سلولی بودن آن است. مغز استخوان طبیعی حاوی تعداد معینی از سلولهای خون ساز و سلولهای چربی است. گفته میشود مغز استخوان با سلولهای خون ساز بیش از حد، هیپرسلولار (hypercellular) نامیده میشود. اگر تعداد کمی سلولهای خون ساز در نمونه یافت شود، مغز استخوان هیپوسلولار (hypocellular) نامیده میشود.
فلوسیتومتری (Flow cytometry) و ایمونوهیستوشیمی (immunohistochemistry)
این آزمایشها برای طبقه بندی سلولهای لوسمی بر اساس پروتئینهای خاصی در سلولها یا روی سلولها (معروف به ایمونوفنوتایپینگ یا immunophenotyping) استفاده میشوند. این نوع آزمایش برای تعیین نوع دقیق و نوع فرعی سرطان خون بسیار مفید است. این آزمایش اغلب روی سلولهای مغز استخوان انجام میشود اما میتوان آن را روی سلولهای خون، غدد لنفاوی و سایر مایعات بدن نیز انجام داد.
هم برای فلوسیتومتری و هم برای ایمونوهیستوشیمی، نمونههای سلولی با آنتی بادیهایی درمان میشوند که پروتئینهایی هستند که به پروتئینهای دیگر روی سلولها میچسبند. برای ایمونوهیستوشیمی، سلولها در زیر میکروسکوپ بررسی میشوند تا ببینند آیا آنتی بادیها به آنها چسبیدهاند یا نه (یعنی این پروتئینها را دارند)، در حالی که برای فلوسیتومتری از دستگاه خاصی استفاده میشود.
فلوسیتومتری همچنین میتواند برای تخمین مقدار DNA در سلولهای لوسمی استفاده شود. دانستن این موضوع به خصوص در ALL مهم است زیرا سلولهایی با مقادیر DNA بیشتر از حد طبیعی (شاخص DNA 1.16 یا بالاتر) اغلب به شیمی درمانی حساس تر هستند و این سرطان خونها وضعیت آتی (چشم انداز) بهتری دارند.
فلوسیتومتری همچنین میتواند برای اندازه گیری پاسخ به درمان و وجود حداقل بیماری باقی مانده (MRD) در برخی از انواع لوسمیها مورد استفاده قرار گیرد.
آزمایشات کروموزومی
این آزمایشها کروموزومها (رشتههای بلند DNA) درون سلولها را بررسی میکنند. سلولهای طبیعی انسان دارای 23 جفت کروموزوم هستند که هر کدام اندازه مشخصی دارند و در زیر میکروسکوپ به شکل خاصی به نظر میرسند. اما در برخی از انواع لوسمی، سلولها تغییراتی در کروموزوم خود دارند.
به عنوان مثال، گاهی اوقات 2 کروموزوم مقداری از DNA خود را با هم عوض میکنند، به طوری که بخشی از یک کروموزوم به بخشی از کروموزوم متفاوت متصل میشود. این تغییر که جابجایی نامیده میشود، معمولاً در زیر میکروسکوپ قابل مشاهده است. انواع دیگری از تغییرات کروموزومی نیز امکان پذیر است. شناخت این تغییرات میتواند به شناسایی انواع خاصی از لوسمیهای حاد و به تعیین وضعیت بیمار در آینده (چشم انداز) کمک کند.
گاهی اوقات سلولهای لوسمی تعدادی کروموزوم غیر طبیعی دارند (بهجای 46 کروموزوم معمولی) – ممکن است برخی از کروموزومها را از دست بدهند یا نسخههای اضافی از برخی دیگر را داشته باشند. این پدیده همچنین میتواند روی وضعیت کودک تأثیر بگذارد. به عنوان مثال، در ALL، شیمی درمانی در صورتی که سلولها بیش از 50 کروموزوم داشته باشند، تاثیر بیشتری دارد و اگر سلولها کمتر از 46 کروموزوم داشته باشند، کارایی کمتری دارد.
یافتن این نوع تغییرات کروموزومی با آزمایشهای آزمایشگاهی میتواند در پیش بینی چشم انداز و پاسخ کودک به درمان بسیار مفید باشد.
سیتوژنتیک (Cytogenetics): برای این آزمایش، سلولهای سرطانی خون در یک ظرف آزمایشگاهی رشد میکنند و کروموزومها زیر میکروسکوپ بررسی میشوند تا هر گونه تغییر، از جمله کروموزومهای از دست رفته یا اضافی را تشخیص دهند. (شمارش تعداد کروموزومها توسط سیتوژنتیک اطلاعات مشابه اندازه گیری شاخص DNA توسط فلوسیتومتری را فراهم میکند، همان طور که این موضوع در بالا توضیح داده شد.)
آزمایش سیتوژنتیک معمولاً حدود 2 تا 3 هفته طول میکشد زیرا سلولهای سرطان خون باید چند هفته قبل از اینکه کروموزومهای آنها برای بررسی آماده شوند در ظروف آزمایشگاهی رشد کنند.
همه تغییرات کروموزومی را نمیتوان در زیر میکروسکوپ مشاهده کرد. سایر آزمایشات آزمایشگاهی اغلب میتوانند به تشخیص این تغییرات کمک کنند.
هیبریداسیون در محل فلورسنت (FISH یا Fluorescent in situ hybridization): این روش دیگری برای بررسی کروموزومها و ژنها است. در این آزمایش از رنگهای فلورسنت خاصی استفاده میکند که فقط به قسمتهای خاصی از کروموزومهای خاص متصل میشوند. FISH میتواند اکثر تغییرات کروموزومی (مانند جابهجاییها) را که در زیر میکروسکوپ در آزمایشهای سیتوژنتیک استاندارد قابل مشاهده است و همچنین برخی از تغییرات بسیار کوچک را پیدا کند که با آزمایشهای سیتوژنتیک معمولی قابل مشاهده نیستند.
از FISH میتوان برای جستجوی تغییرات خاص در کروموزومها استفاده کرد. میتوان از آن بر روی نمونههای خون یا مغز استخوان استفاده کرد. این روش بسیار دقیق است و معمولاً میتواند در عرض چند روز نتیجه دهد.
واکنش زنجیرهای پلیمراز (Polymerase chain reaction یا PCR): این یک آزمایش بسیار حساس است که میتواند برخی تغییرات کروموزومی و ژنی بسیار کوچک را نیز تشخیص دهد که در زیر میکروسکوپ دیده نمیشوند، حتی اگر سلولهای سرطانی خون در یک نمونه بسیار کم باشد. این آزمایش میتواند در جستجوی تعداد کمی از سلولهای لوسمی (بیماری باقی مانده حداقل یا MRD) که ممکن است با آزمایشهای دیگر در طول درمان و پس از درمان شناسایی نشوند، بسیار مفید باشد.
سایر آزمایشهای مولکولی و ژنتیکی: انواع جدیدتر آزمایشهای آزمایشگاهی، که گاهی به آنها آزمایشهای توالییابی نسل جدید (NGS) نیز گفته میشود، نیز میتوانند بر روی نمونهها برای بررسی تغییرات ژنی خاص در سلولهای سرطان خون انجام شوند.
سایر آزمایشات خون
کودکان مبتلا به لوسمی، آزمایشاتی برای اندازه گیری برخی مواد شیمیایی در خون خواهند داشت تا میزان عملکرد سیستم بدن آنها بررسی شود.
این آزمایشها برای تشخیص سرطان خون استفاده نمیشوند اما در کودکانی که به آن مبتلا هستند، میتوانند به یافتن آسیبهای موجود در کبد، کلیهها یا سایر اندامهای ناشی از گسترش سلولهای سرطان خون یا داروهای شیمی درمانی خاص کمک کنند. همچنین، اغلب آزمایشهایی برای اندازه گیری سطح مواد معدنی مهم خون و برای اطمینان از لخته شدن خون به درستی، انجام میشود.
کودکان همچنین ممکن است برای بررسی وجود عفونت در خون آزمایش شوند. تشخیص و درمان سریع عفونت در کودکان مبتلا به لوسمی بسیار مهم است زیرا سیستم ایمنی ضعیف آنها میتواند باعث گسترش عفونت شود.
تستهای تصویر برداری
در آزمایشهای تصویر برداری از اشعه ایکس، امواج صوتی، میدانهای مغناطیسی یا ذرات رادیو اکتیو برای تهیه تصاویری از داخل بدن استفاده میشود. لوسمی معمولاً تومور ایجاد نمیکند، بنابراین آزمایشهای تصویر برداری به اندازه سایر انواع سرطان مفید نیستند. اما اگر فرد به داشتن سرطان خون مشکوک باشد یا با آن تشخیص داده شده باشد، پزشک کودک شما ممکن است برخی از این آزمایشها را برای درک بهتر وسعت بیماری یا جستجوی مشکلات دیگر مانند عفونتها تجویز کند.
اشعه ایکس قفسه سینه
اشعه ایکس قفسه سینه میتواند به تشخیص بزرگ شدن تیموس یا غدد لنفاوی در قفسه سینه کمک کند. اگر نتیجه آزمایش غیر طبیعی باشد، سی تی اسکن قفسه سینه ممکن است برای مشاهده جزئیات بیشتر انجام شود.
اگر کودک شما عفونت ریه داشته باشد، اشعه ایکس قفسه سینه نیز میتواند به بررسی ذات الریه کمک کند.
توموگرافی کامپیوتری (CT) اسکن
سی تی اسکن معمولاً برای کودکان مبتلا به سرطان خون مورد نیاز نیست اما اگر پزشک مشکوک باشد که سرطان خون در غدد لنفاوی قفسه سینه یا در اندامهایی مانند طحال یا کبد رشد میکند، ممکن است انجام شود. همچنین این روش گاهی اوقات برای مشاهده مغز و نخاع استفاده میشود اما اسکن MRI نیز ممکن است در این مورد مورد استفاده قرار گیرد.
اسکن PET یا CT: برخی از دستگاهها سی تی اسکن را با اسکن توموگرافی گسیل پوزیترون (PET) ترکیب میکنند که این کار میتواند اطلاعات بیشتری را در مورد هر ناحیه غیر طبیعی که در CT ظاهر میشود، ارائه دهد.
اسکن تصویر برداری رزونانس مغناطیسی (MRI)
اسکن ام آر آی، مانند سی تی اسکن، تصاویر دقیقی از بافتهای نرم بدن ایجاد میکند. این کار برای بررسی مغز و نخاع بسیار مفید است، بنابراین اگر پزشک دلیلی از گسترش سرطان خون در بافتی داشته باشد (مانند حالتی که کودک علائمی مانند سردرد، تشنج یا استفراغ داشته باشد) به احتمال زیاد انجام میشود. این آزمایش کودک را در معرض تشعشع قرار نمیدهد.
سونوگرافی (Ultrasound)
از سونوگرافی میتوان برای مشاهده غدد لنفاوی نزدیک سطح بدن یا جستجوی اندامهای بزرگ شده داخل شکم مانند کلیهها، کبد و طحال استفاده کرد. (برای مشاهده اندامها یا غدد لنفاوی موجود در قفسه سینه نمیتوان از آن استفاده کرد زیرا دندهها امواج صوتی را مسدود میکنند.)
انجام این آزمایش نسبتاً آسان است و از تشعشع در آن استفاده نمیشود.
جراحی برای لوسمی دوران کودکی
جراحی نقش بسیار محدودی در درمان سرطان خون کودکان دارد. از آن جایی که سلولهای سرطانی خون به طور گسترده در سراسر مغز استخوان و خون پخش میشوند، درمان این نوع سرطان با جراحی امکان پذیر نیست. جدای از بیوپسی غدد لنفاوی احتمالی، جراحی به ندرت نقشی حتی در تشخیص سرطان خون دارد زیرا این عمل معمولاً با آسپیراسیون مغز استخوان انجام میشود و بیوپسی معمولاً میتواند لوسمی را تشخیص دهد.
قرار دادن کاتتر ورید مرکزی (central venous catheter)
اغلب قبل از شروع شیمی درمانی، جراحی برای قرار دادن یک لوله پلاستیکی کوچک به نام کاتتر وریدی مرکزی (CVC) یا دستگاه دسترسی وریدی (VAD) در یک رگ خونی بزرگ مورد نیاز است. انتهای لوله درست در زیر پوست مانده یا در ناحیه قفسه سینه یا بازو از بدن بیرون میآید.
CVC در طول درمان (اغلب برای چندین ماه) برای دادن داروهای داخل وریدی (IV) مانند شیمی درمانی و نمونه گیری خون در بدن باقی میماند. این کار باعث کاهش تعداد سوزنهای مورد نیاز در طول درمان میشود. برای والدین بسیار مهم است که یاد بگیرند چگونه از کاتتر مراقبت کنند تا از عفونی شدن آن جلوگیری کنند.
پرتو درمانی برای لوسمی دوران کودکی
پرتو درمانی از پرتوهای پرانرژی برای از بین بردن سلولهای سرطانی استفاده میکند.
همیشه برای درمان لوسمی نیازی به پرتو نیست اما میتوان از آن در شرایط خاصی استفاده کرد:
- گاهی اوقات برای جلوگیری یا درمان گسترش لوسمی به مغز یا درمان بیضه در پسران در صورتی که سرطان خون به آنها رسیده باشد، استفاده میشود. اما شیمی درمانی اغلب در این شرایط به جای آن استفاده میشود.
- میتوان از آن (به ندرت) برای درمان توموری که روی نای (windpipe) فشار میآورد، استفاده کرد. اما شیمی درمانی اغلب به جای آن استفاده میشود زیرا ممکن است سریع تر عمل کند.
- پرتو دهی به کل بدن اغلب بخش مهمی از درمان قبل از انجام پیوند سلولهای بنیادی است.
پرتو درمانی چگونه انجام میشود؟
قبل از شروع روند درمان، تیم مراقبین اندازه گیریهای دقیق بدن را برای تعیین زوایای صحیح برای نشانه گیری پرتوهای پرتو و دوز مناسب تابش انجام میدهند. این جلسه برنامه ریزی که شبیه سازی (simulation) نامیده میشود، معمولا شامل انجام تستهای تصویر برداری مانند اسکن سی تی یا ام آر آی است.
این درمان به خودی خود بسیار شبیه گرفتن عکس اشعه ایکس است اما پرتو آن بسیار قوی تر است.
این روش بدون درد است اما برخی از کودکان کوچکتر ممکن است نیاز به آرام بخش داشته باشند تا پزشکان مطمئن شوند که در طول درمان حرکت نمیکنند. هر دوره درمانی فقط چند دقیقه طول میکشد، اگرچه زمان تنظیم – قرار دادن کودک شما در موقعیت مناسب برای درمان – معمولاً بیشتر زمان میبرد.
عوارض جانبی احتمالی اشعه
عوارض جانبی احتمالی کوتاه مدت بستگی به این دارد که تابش کجا را هدف قرار گرفته است و میتواند شامل موارد زیر باشد:
- تغییرات پوستی مانند آفتاب سوختگی
- ریزش مو در ناحیه تحت درمان
- تهوع، استفراغ، یا اسهال
- خستگی
- افزایش خطر عفونت
عوارض جانبی طولانی مدت نیز ممکن است رخ دهد و در متن توضیح داده شدهخ است.
شیمی درمانی برای لوسمی دوران کودکی
شیمی درمانی (Chemo) درمان اصلی اکثر لوسمیهای دوران کودکی است. این درمان همراه با داروهای ضد سرطانی است که در ورید (IV)، ماهیچه، مایع مغزی نخاعی (CSF) اطراف مغز و نخاع یا از طریق دهان مصرف میشوند. به جز زمانی که به CSF وارد میشود، داروهای شیمیائی وارد جریان خون میشوند و به تمام نواحی بدن میرسند و این اتفاق درمان را برای سرطانهایی مانند لوسمی بسیار مفید میکند.
سرطان خون با ترکیبی از چندین داروی شیمی درمانی درمان میشود. پزشکان به صورت دورهای شیمی درمانی را انجام میدهند و هر دوره درمان پس از یک دوره استراحت به بدن زمان میدهد تا بهبود یابد.
به طور کلی، در درمان لوسمی حاد میلوئیدی (AML) از دوزهای بالاتر شیمی درمانی در مدت زمان کوتاه تری (معمولاً کمتر از یک سال) استفاده میشود و در درمان لوسمی لنفوسیتی حاد (ALL) از دوزهای کمتر شیمی درمانی در مدت زمان طولانی تری استفاده میشود. (معمولا 2 تا 3 سال).
برخی از داروهای شیمی درمانی مورد استفاده برای درمان لوسمی کودکان عبارتند از:
- وین کریستین (Vincristine)
- داونوروبیسین (دانومایسین یا Daunorubicin)
- دوکسوروبیسین (آدریامایسین یا Doxorubicin)
- ایداروبیسین (Idarubicin)
- سیتارابین (سیتوزین آرابینوزید یا ara-C)
- ال-آسپارژیناز، PEG-L-آسپارژیناز (پگاسپارگاز یا pegaspargase)
- اتوپوزید (Etoposide)
- 6-مرکاپتوپورین (6-MP)
- 6-تیوگوانین (6-TG)
- متوترکسات (Methotrexate)
- میتوکسانترون (Mitoxantrone)
- سیکلوفسفامید (Cyclophosphamide)
- داروهای کورتیکواستروئیدی مانند پردنیزون (prednisone)، پردنیزولون (prednisolone)، دگزامتازون (dexamethasone) یا هیدروکورتیزون (hydrocortisone)
کودکان احتمالاً چندین مورد از این داروها را در زمانهای مختلف در طول دوره درمان دریافت خواهند کرد اما همه آنها را دریافت نمیکنند.
عوارض جانبی احتمالی شیمی درمانی
داروهای شیمی درمانی میتوانند بر برخی سلولهای طبیعی بدن تأثیر بگذارند که همین امر میتواند منجر به ایجاد عوارض جانبی شود.
عوارض جانبی شیمی درمانی به نوع و دوز داروهای داده شده و طول روند درمان بستگی دارد. این عوارض جانبی میتواند شامل موارد زیر باشد:
- ریزش مو
- زخمهای دهان
- از دست دادن اشتها
- اسهال
- تهوع و استفراغ
داروهای شیمی درمانی همچنین بر سلولهای طبیعی در مغز استخوان نیز تأثیر میگذارند که میتواند تعداد سلولهای خونی را کاهش دهد. این اتفاق میتواند منجر به:
- افزایش خطر ابتلا به عفونتها (به دلیل داشتن گلبولهای سفید طبیعی بسیار کم)
- کبودی و خونریزی به راحتی (به دلیل داشتن تعداد بسیار کم پلاکت خون)
- خستگی (به دلیل داشتن گلبولهای قرمز بسیار کم)
مشکلات مربوط به شمارش سلولهای خونی اغلب در ابتدا ناشی از خود لوسمی است. افراد ممکن است در طول بخش اول درمان به دلیل شیمی درمانی بدتر شوند اما احتمالاً با از بین رفتن سلولهای سرطانی خون و بهبود سلولهای طبیعی در مغز استخوان، بهبود خواهند یافت.
اکثر عوارض جانبی معمولاً پس از پایان درمان از بین میروند. اغلب راههایی برای کاهش این عوارض وجود دارد. به عنوان مثال، داروهایی برای کمک به پیشگیری یا کاهش تهوع و استفراغ تجویز میشود. داروهای دیگری که به عنوان فاکتورهای رشد شناخته میشوند میتوانند برای کمک به افزایش تعداد سلولهای خونی تجویز شوند.
سندرم لیز شدن تومور (Tumor lysis syndrome): این عارضه جانبی شیمی درمانی میتواند در کودکانی که قبل از درمان تعداد زیادی سلول لوسمی در بدن داشتند، اتفاق بیفتد. هنگامی که شیمی درمانی این سلولها را میکشد، این سلولها پاره میشوند و محتویات خود را در جریان خون آزاد میکنند. این امر میتواند کلیهها را تحت تأثیر قرار دهد زیرا آنها قادر به خارج کردن همه این مواد از بدن نیستند. مقدار زیاد مواد معدنی خاص نیز میتواند بر قلب و سیستم عصبی تأثیر بگذارد. با اطمینان از دریافت مایعات زیادی در طول درمان و داروهای خاصی مانند بی کربنات (bicarbonate)، آلوپورینول (allopurinol) و راسبوریکاز (rasburicase) که به بدن کمک میکند تا از شر این مواد خلاص شود، میتوان از ایجاد این مشکل جلوگیری کرد.
برخی از داروهای شیمی درمانی میتوانند عوارض جانبی خاص دیگری نیز داشته باشند. مثلا:
- وین کریستین میتواند به اعصاب آسیب برساند که میتواند منجر به بی حسی، سوزن سوزن شدن یا ضعف در دستها یا پاها شود (معروف به نوروپاتی محیطی یا peripheral neuropathy).
- L-Asparaginase و PEG-L-asparaginase میتوانند خطر لخته شدن خون را افزایش دهند.
برخی از داروهای شیمی درمانی نیز میتوانند عوارض جانبی دیر هنگام یا طولانی مدتی مانند تأثیر بر رشد و تکامل، تأثیرات بر باروری در مراحل بعدی زندگی یا افزایش خطر ابتلا به سرطان دیگری (اغلب AML) را ایجاد کنند.
حتماً از پزشک یا پرستار فرزندتان در مورد عوارض جانبی خاصی که باید مراقب آن باشید و اینکه چه کاری میتوانید برای کمک به کاهش این عوارض انجام دهید، سوال بپرسید.
شیمی درمانی که مستقیماً در مایع مغزی نخاعی (CSF) در اطراف مغز و نخاع (معروف به شیمی درمانی داخل نخاعی یا intrathecal chemotherapy) انجام میشود، میتواند عوارض جانبی خاص خود را داشته باشد، اگرچه این موارد رایج نیستند. شیمی درمانی داخل نخاعی ممکن است در برخی از کودکان باعث اختلال در تفکر یا حتی تشنج شود.
داروهای درمانی هدفمند (Targeted Therapy Drugs) برای لوسمی دوران کودکی
در سالهای اخیر داروهای جدیدی ساخته شده است که بخشهای خاصی از سلولهای سرطانی را هدف قرار میدهند. این داروهای هدفمند متفاوت از داروهای شیمی درمانی استاندارد عمل میکنند. آنها را میتوان به جای یا همراه با شیمی درمانی در برخی شرایط استفاده کرد. این داروها عوارض جانبی متفاوتی با شیمی درمانی دارند. برخی از داروهای هدفمند میتوانند در بروز برخی از لوسمیهای دوران کودکی مفید باشند.
مهارکنندههای BCR-ABL برای CML (و برخی موارد ALL)
تقریباً همه کودکان مبتلا به لوسمی میلوئیدی مزمن (CML) دارای یک کروموزوم غیر طبیعی در سلولهای لوسمی خود هستند که به کروموزوم فیلادلفیا معروف است. این کروموزومها دارای یک جهش ژنی خاص به نام BCR-ABL هستند که به رشد سلولهای سرطان خون کمک میکند.
داروهای هدفمند معروف به مهارکنندههای تیروزین کیناز (TKIs)، مانند ایماتینیب (Gleevec)، داساتینیب (Sprycel) و nilotinib (Tasigna) به سلولهایی حمله میکنند که دارای جهش ژن BCR-ABL هستند. این داروها در کنترل سرطان خون برای مدت طولانی در اکثر کودکان بسیار موثر هستند، اگرچه هنوز مشخص نیست که آیا این داروها میتوانند به درمان CML کمک کنند یا خیر.
تعداد کمی از کودکان مبتلا به لوسمی لنفوسیتی حاد (ALL) نیز کروموزوم فیلادلفیا را در سلولهای لوسمی خود دارند. مطالعات نشان داده اند که نتیجه روند درمان آنها زمانی بهبود مییابد که یکی از این داروهای هدفمند همراه با شیمی درمانی توسط آنها مصرف شود. این داروها روزانه و به صورت قرص مصرف میشوند.
عوارض جانبی احتمالی این داروها شامل اسهال، حالت تهوع، درد عضلانی، خستگی و زوائد پوستی است. این عوارض عموماً خفیف هستند. یک عارضه جانبی رایج، تورم در اطراف چشمها یا در دستها یا پاها است که ممکن است در اثر اثرات دارو بر قلب ایجاد شود. سایر عوارض جانبی احتمالی شامل کاهش تعداد گلبولهای قرمز و پلاکت در هنگام شروع درمان است. این داروها همچنین ممکن است رشد کودک را کند کنند، به خصوص اگر قبل از بلوغ استفاده شوند.
گمتوزوماب اوزوگامایسین (Gemtuzumab ozogamicin یا Mylotarg) برای AML
این درمان هدفمند یک آنتی بادی مونوکلونال (یک پروتئین ایمنی ساخته دست بشر) است که به یک داروی شیمی درمانی مرتبط میباشد. آنتی بادی مانند یک سیگنال محلی عمل میکند و داروی شیمی درمانی را به سلولهای سرطان خون میرساند، جایی که وارد سلولها میشود و زمانی که آنها سعی میکنند به سلولهای جدید تقسیم شوند، آنها را میکشد.
این دارو را میتوان برای درمان برخی از کودکان مبتلا به لوسمی میلوئید حاد (AML) در شرایط مختلف استفاده کرد:
- میتوان از آن به عنوان بخشی از درمان اولیه AML همراه با شیمی درمانی استفاده کرد.
- اگر لوسمی عود کند یا دیگر به درمان پاسخ ندهد، میتوان آن را به تنهایی (معمولاً به خودی خود) برای بیمار تجویز کرد.
این دارو به صورت انفوزیون داخل ورید (IV) به فرد داده میشود. هنگامی که به عنوان بخشی از اولین درمان استفاده میشود، معمولاً یک بار در مرحله القاء و یک بار در طول تثبیت (تشدید) تزریق میشود. هنگامی که برای درمان AML که عود کرده است یا هنوز در حال رشد است استفاده میشود، معمولاً به صورت 3 دوز و 3 روز بین هر دوز تجویز میشود.
شایع ترین عوارض جانبی عبارتند از تب، تهوع و استفراغ، سطوح پایین سلولهای خونی (با افزایش خطر عفونت، خونریزی و خستگی)، تورم و زخم در دهان، یبوست، زوائد پوستی و سردرد.
عوارض جانبی کمتر شایع اما جدی تر میتواند شامل موارد زیر باشد:
- آسیب شدید کبد، از جمله بیماری انسداد وریدی (انسداد وریدها در کبد یا veno-occlusive disease)
- واکنشهای حین انفوزیون (مشابه واکنش آلرژیک). به احتمال زیاد به کودک شما قبل از هر انفوزیون دارو داده میشود تا از این امر جلوگیری کند.
- عفونتهای جدی یا تهدید کننده زندگی، به ویژه در افرادی که قبلا پیوند سلولهای بنیادی انجام داده اند.
- تغییرات در ریتم قلب
بسیاری از داروهای هدفمند دیگر اکنون برای درمان AML در بزرگسالان مورد استفاده قرار میگیرند و برخی از آنها اکنون در آزمایشات بالینی برای استفاده توسط کودکان نیز آزمایش میشوند.
عوامل تمایزی برای APL
لوسمی پرومیلوسیتیک حاد (APL) از جهات مهمی با سایر زیرگروههای AML متفاوت است. سلولهای لوسمی در APL (به نام بلاست) دارای تغییرات ژنی خاصی هستند که مانع از بلوغ آنها به گلبولهای سفید طبیعی میشود. داروهایی به نام عوامل تمایز (differentiation agents) میتوانند به بلوغ (تمایز) بلاستها به گلبولهای سفید طبیعی کمک کنند. دو مورد از این داروها را میتوان برای درمان APL استفاده کرد:
- آل ترانس رتینوئیک اسید (ATRA، ترتینوئین یا All-trans-retinoic acid)
- تری اکسید آرسنیک (Arsenic trioxide یا ATO)
ATRA نوعی ویتامین A است که معمولاً بخشی از درمان اولیه APL میباشد. این دارو یا همراه با شیمی درمانی یا همراه با ATO به بیمار داده میشود. همچنین میتوان از آن در مراحل بعدی درمان نیز استفاده کرد.
عوارض جانبی ATRA میتواند شامل موارد زیر باشد:
- سردرد
- تب
- خشکی پوست و دهان
- زوائد پوستی
- پاهای متورم
- زخم در دهان یا گلو
- خارش
- چشمهای تحریک شده
همچنین میتواند سطح چربی خون (مانند کلسترول و تری گلیسیرید) را افزایش دهد. در حین استفاده از این دارو اغلب نتایج آزمایش خون کبد غیر طبیعی میشود. این عوارض اغلب با قطع دارو از بین میروند.
تری اکسید آرسنیک (ATO) میتواند به روشی مشابه ATRA در بیماران مبتلا به APL عمل کند. میتوان آن را با ATRA در درمان اولیه APL تجویز کرد اما در درمان APL که پس از درمان با ATRA همراه با شیمی درمانی عود میکند نیز مفید است.
بیشتر عوارض جانبی ATO خفیف است و میتواند شامل موارد زیر باشد:
- احساس خستگی
- حالت تهوع
- استفراغ
- اسهال
- شکم درد
- آسیب عصبی (نوروپاتی) که منجر به بی حسی و گزگز در دستها و پاها میشود.
ATO همچنین میتواند باعث ایجاد مشکلاتی در ریتم قلب شود که گاهی اوقات میتوانند جدی باشند.
هر دوی این داروها میتوانند یک عارضه جانبی جدی به نام سندرم تمایز (differentiation syndrome که قبلاً سندرم رتینوئیک اسید (retinoic acid syndrome) نامیده میشد) ایجاد کنند. این سندروم زمانی اتفاق میافتد که سلولهای لوسمی مواد شیمیایی خاصی را در خون آزاد میکنند. این حالت اغلب در طی دو هفته اول درمان و در بیمارانی که تعداد گلبولهای سفید خون بالایی دارند، دیده میشود.
علائم میتواند شامل تب، مشکلات تنفسی به دلیل تجمع مایع در ریهها و اطراف قلب، فشار خون پایین، آسیب کلیه و تجمع شدید مایع در سایر نقاط بدن باشد. در حالی که سندرم تمایز میتواند جدی باشد، اغلب میتوان آن را با قطع دارو و مصرف یک داروی استروئیدی مانند دگزامتازون برای مدتی درمان کرد.
ایمونوتراپی (Immunotherapy) برای لوسمی کودکان
ایمونوتراپی استفاده از داروها برای کمک به سیستم ایمنی بدن خود بیمار است که سلولهای سرطانی را شناسایی و از بین ببرد. انواع مختلفی از ایمونوتراپی برای استفاده در برابر لوسمی دوران کودکی در حال مطالعه است و برخی از آنها اکنون در حال استفاده هستند.
درمان با سلول T با گیرنده آنتی ژن کایمریک (CAR)
برای این درمان، سلولهای ایمنی به نام سلولهای T از خون کودک برداشته میشوند و به طور ژنتیکی در آزمایشگاه تغییر داده میشوند تا گیرندههای خاصی (به نام گیرندههای آنتی ژن کایمریک یا CAR) روی سطح آنها وجود داشته باشد. این گیرندهها میتوانند به پروتئینهای سلولهای لوسمی متصل شوند. سلولهای T سپس در آزمایشگاه تکثیر میشوند و به خون کودک بازگردانده میشوند، جایی که میتوانند سلولهای سرطان خون را پیدا کرده و به آنها حمله کنند.
(Kymriah) Tisagenlecleucel
این یک نوع درمان با سلولهای T CAR است که پروتئین CD19 را روی سلولهای سرطان خون خاص هدف قرار میدهد. میتوان از این نوع درمان برای درمان لوسمی لنفوبلاستیک حاد دوران کودکی (ALL) استفاده کرد که پس از درمان عود کرده است یا دیگر به درمان پاسخ نمیدهد.
برای انجام این روند درمانی، سلولهای T از خون کودک طی فرآیندی به نام لوکفرزیس (leukapheresis) خارج میشوند. خون از طریق یک خط IV از بدن خارج شده و به دستگاهی میرود که سلولهای T را حذف میکند. سپس خون باقی مانده به بدن باز میگردد. این کار معمولاً چند ساعت طول میکشد و ممکن است نیاز به تکرار داشته باشد. سپس سلولها منجمد شده و به آزمایشگاه فرستاده میشوند و در آن جا به سلولهای CAR T تبدیل شدت و تکثیر میشوند. این روند ممکن است چند هفته طول بکشد.
برای انجام این روند درمانی، کودک معمولاً برای چند روز شیمی درمانی میشود تا این کار به آماده سازی بدن کمک کند. سپس سلولهای CAR T به داخل ورید تزریق میشوند.
در اکثر کودکانی که این درمان را انجام دادهاند، سرطان خون دیگر طی چند ماه پس از درمان قابل تشخیص نیست، اگرچه هنوز مشخص نیست که آیا این بدان معناست که آنها درمان شدهاند یا خیر.
عوارض جانبی احتمالی
این نوع درمان میتواند عوارض جانبی جدی یا حتی تهدید کننده زندگی به همراه داشته باشد، به همین دلیل است که باید در یک مرکز پزشکی که تیم آنها در این مورد آموزش دیده اند، انجام شود.
سندرم آزاد سازی سیتوکین (CRS یا Cytokine release syndrome): CRS زمانی اتفاق میافتد که سلولهای T مواد شیمیایی (سیتوکینها) را آزاد میکنند که سیستم ایمنی را تقویت میکنند. این اتفاق میتواند در عرض چند روز تا چند هفته پس از درمان اتفاق بیفتد و میتواند تهدید کننده زندگی باشد. علائم بروز این اتفاق میتواند شامل موارد زیر باشد:
- تب و لرز شدید
- مشکل در تنفس
- تهوع، استفراغ، و یا اسهال شدید
- درد شدید عضلانی یا مفصلی
- احساس سرگیجه یا سبکی سر
مشکلات سیستم عصبی: این دارو میتواند اثرات جدی بر روی سیستم عصبی داشته و منجر به علائمی مانند موارد زیر شود:
- سردرد
- تغییرات در هوشیاری
- سردرگمی یا آشفتگی
- تشنج
- مشکل در صحبت کردن و درک کردن
- از دست دادن تعادل
سایر عوارض جانبی جدی: سایر عوارض جانبی ممکن است شامل موارد زیر باشند:
- عفونتهای جدی
- تعداد کم سلولهای خونی که میتواند خطر عفونت، خستگی و کبودی یا خونریزی را افزایش دهد.
بسیار مهم است که هر گونه عوارض جانبی را فوراً به تیم مراقبتهای پزشکی گزارش دهید زیرا اغلب داروهایی وجود دارند که میتوانند به درمان آنها کمک کنند.
آنتی بادیهای مونوکلونال (Monoclonal antibodies)
آنتی بادیها پروتئینهایی هستند که توسط سیستم ایمنی بدن برای کمک به مبارزه با عفونتها ساخته میشوند. نسخههای دست ساز این پروتئینها که آنتیبادیهای مونوکلونال نامیده میشوند را میتوان برای حمله به یک هدف خاص، مانند پروتئینهای روی سطح سلولهای سرطانی خون، طراحی کرد.
(Blincyto) Blinatumomab
Blinatumomab نوع خاصی از آنتی بادی مونوکلونال است زیرا میتواند همزمان به 2 پروتئین مختلف متصل شود. بخشی از بلیناتوماب به پروتئین CD19 که در سلولهای B یافت میشود، میچسبد. بخش دیگری به CD3 متصل میشود، پروتئینی که در سلولهای ایمنی به نام سلولهای T یافت میشود. این دارو با اتصال به هر دوی این پروتئینها، سلولهای سرطانی و سلولهای ایمنی را به هم نزدیک میکند که به سیستم ایمنی کمک میکند تا به سلولهای سرطانی حمله کند.
این دارو برای درمان برخی از انواع ALL سلول B، معمولاً پس از استفاده از شیمی درمانی استفاده میشود. در ورید (IV) به صورت انفوزیون مداوم طی 28 روز به بیمار داده میشود. این کار ممکن است بعد از 2 هفته استراحت تکرار شود. به دلیل برخی عوارض جانبی جدی که اغلب در چند نوبت اول تجویز آن رخ میدهد، کودک معمولاً نیاز دارد حداقل در 2 سیکل اول در چند روز اول در بیمارستان بماند.
شایع ترین عوارض جانبی عبارتند از تب، سردرد، تورم پا و دست، حالت تهوع، لرزش، زوائد پوستی، یبوست و سطح پایین پتاسیم خون.
همچنین میتواند باعث کاهش تعداد گلبولهای سفید خون شود که خطر ابتلا به عفونتهای جدی را افزایش میدهد.
این دارو همچنین میتواند باعث بروز مشکلات سیستم عصبی مانند تشنج، مشکل در صحبت کردن یا تکلم، غش کردن، گیجی و از دست دادن تعادل شود.
برخی از کودکان ممکن است در حین انفوزیون واکنشهای جدی داشته باشند (شبیه به یک واکنش آلرژیک). علائم میتواند شامل احساس سبکی سر یا سرگیجه (به دلیل فشار خون پایین)، سردرد، حالت تهوع، تب یا لرز، تنگی نفس و یا خس خس سینه باشد. به کودک شما قبل از هر انفوزیون دارو داده میشود تا از این امر جلوگیری کند.
گمتوزوماب اوزوگامایسین (Gemtuzumab ozogamicin یا Mylotarg)
این آنتی بادی مونوکلونال که میتواند برای درمان لوسمی میلوئید حاد (AML) استفاده شود، به روشی متفاوت عمل میکند. این موضوع در «داروهای درمانی هدفمند برای لوسمی کودکان» توضیح داده شده است.
انواع دیگر ایمونوتراپی نیز برای استفاده در برابر لوسمی در حال بررسی است.
شیمی درمانی با دوز بالا و پیوند سلولهای بنیادی برای لوسمی دوران کودکی
پیوند سلولهای بنیادی (SCT) (همچنین به عنوان پیوند مغز استخوان نیز شناخته میشود) گاهی اوقات میتواند برای کمک به بهبود شانس درمان سرطان خون در دوران کودکی استفاده شود. SCT به پزشکان اجازه میدهد حتی از دوزهای بالاتری از شیمی درمانی نسبت به آنچه که یک کودک به طور معمول تحمل میکند، استفاده کنند.
شیمی درمانی با دوز بالا، مغز استخوان را از بین میبرد، جایی که سرطان خون شروع میشود اما همچنین سلولهای خونی جدید تشکیل میشوند. این اتفاق میتواند منجر به عفونتهای تهدید کننده زندگی، خونریزی و سایر مشکلات ناشی از تعداد کم سلولهای خونی شود. پیوند سلولهای بنیادی پس از شیمی درمانی برای بازیابی سلولهای بنیادی خون ساز در مغز استخوان انجام میشود.
سلولهای بنیادی خون ساز مورد استفاده برای پیوند میتوانند از خون یا از مغز استخوان به دست آیند. گاهی اوقات از سلولهای بنیادی خون بند ناف نوزاد استفاده میشود.
پیوند سلولهای بنیادی آلوژنیک (Allogeneic stem cell transplant)
برای لوسمیهای دوران کودکی، نوع پیوند مورد استفاده به عنوان پیوند سلولهای بنیادی آلوژنیک شناخته میشود. در این نوع پیوند، سلولهای بنیادی خون ساز از فرد دیگری اهدا میشود.
نوع بافت دهنده (که به عنوان نوع HLA نیز شناخته میشود) باید تا حد امکان با نوع بافت بیمار مطابقت داشته باشد تا از بروز خطر مشکلات عمده در پیوند جلوگیری شود. نوع بافت بر اساس مواد خاصی در سطح سلولهای بدن است. هرچه تطابق بافت بین اهدا کننده و گیرنده نزدیکتر باشد، سلولهای پیوندی شانس بیشتری برای «پی.ند خوردن» و شروع ساخت سلولهای خونی جدید دارند.
اهدا کننده معمولاً یک برادر یا خواهر با بافتی مشابه با بیمار است. به ندرت، یک اهدا کننده میتواند غیرمرتبط با HLA باشد – غریبهای که داوطلبانه سلولهای بنیادی خون ساز خود را اهدا کرده است. گاهی اوقات از سلولهای بنیادی بند ناف استفاده میشود. این سلولهای بنیادی از خون تخلیه شده از بند ناف و جفت پس از تولد نوزاد و بریده شدن بند ناف به دست میآیند. (این خون سرشار از سلولهای بنیادی است.) منبع این سلولهای بنیادی هرچه باشد، آنها منجمد شده و تا زمانی که برای پیوند مورد نیاز باشند ذخیره میشوند.
زمانی که ممکن است از پیوند سلولهای بنیادی استفاده شود
لوسمی لنفوسیتی حاد (ALL): در ALL، SCT ممکن است در کودکان موجود در برخی از گروههای پرخطر استفاده شود که احتمال بازگشت لوسمی آنها پس از شیمی درمانی اولیه (القایی) بیشتر است. در این مورد، پیوند پس از شیمی درمانی القایی که لوسمی را در مرحله بهبودی قرار میدهد، انجام میشود.
اگر لوسمی به درمان اولیه به خوبی پاسخ ندهد یا اگر بلافاصله پس از بهبودی عود کند (برگردد)، SCT ممکن است یک گزینه باشد. مشخص نیست که آیا SCT باید برای کودکانی استفاده شود که ALL آنها دیرتر (مانند بیش از 6 ماه یا یک سال) پس از اتمام شیمی درمانی اولیه عود میکند یا خیر. این کودکان اغلب با یک دوره دیگر شیمی درمانی با دوز استاندارد بهبود مییابند.
SCT همچنین ممکن است برای کودکان مبتلا به برخی از اشکال کمتر شایع ALL توصیه شود، مانند آنهایی که لوسمی آنها کروموزوم فیلادلفیا دارند یا آنهایی که دارای ALL سلول T هستند که به درمان اولیه به خوبی پاسخ نمیدهند.
لوسمی حاد میلوژن (AML): از آن جایی که AML بیشتر از ALL عود میکند، اگر کودک بیمار، برادر یا خواهری با همان نوع بافت داشته باشد، ممکن است SCT بلافاصله پس از بهبودی AML (پس از درمان اولیه شیمی درمانی) توصیه شود. اهدای سلولهای بنیادی برای پیوند این امر به ویژه در مواردی که خطر عود بسیار بالایی وجود داشته باشد صادق است (مانند برخی از زیررگروههای AML یا زمانی که تغییرات ژنی یا کروموزومی خاصی در سلولهای لوسمی وجود دارد). هنوز بحثهایی در مورد اینکه کدام کودکان مبتلا به AML به این نوع درمان فشرده نیاز دارند، وجود دارد.
اگر بیماری یک کودک مبتلا به AML بعد از اولین دور شیمی درمانی استاندارد عود کند، اکثر پزشکان به محض اینکه کودک دوباره به مرحله بهبودی بازگردد، SCT را توصیه میکنند.
در هر صورت، مهم است که لوسمی قبل از پیوند سلولهای بنیادی در حال بهبود باشد. در غیر این صورت احتمال بازگشت سرطان خون بیشتر است.
لوسمیهای دیگر: SCT همچنین ممکن است بهترین شانس را برای درمان برخی از انواع کمتر شایع لوسمی دوران کودکی، مانند لوسمی میلومونوسیتی نوجوانان (JMML) و لوسمی میلوژن مزمن (CML) ارائه دهد.
برای CML، احتمالاً در ابتدا داروهای جدیدتر درمان هدفمند برای اکثر کودکان استفاده میشوند اما پیوند ممکن است در برخی مواقع مورد نیاز باشد.
نکات کاربردی
پیوند سلولهای بنیادی یک درمان پیچیده است که میتواند عوارض جانبی تهدید کننده زندگی ایجاد کند. اگر پزشکان فکر میکنند که فرزند شما میتواند از پیوند بهرهمند شود، بهترین مکان برای انجام این کار در یک مرکز سرطان است که کارکنان آن در مورد این عمل و مدیریت دوره بهبودی تجربه دارند.
پیوند سلولهای بنیادی اغلب نیاز به بستری طولانی مدت در بیمارستان دارد و میتواند بسیار گران و پر هزینه باشد. حتی اگر پیوند تحت پوشش بیمه شما باشد، هزینههای مشترک یا سایر هزینههای شما به راحتی میتواند به هزاران دلار برسد. مهم است که بدانید بیمهگر شما چه چیزی را قبل از پیوند پوشش میدهد تا ایدهای در مورد آن چه که ممکن است مجبور به پرداخت باشید، داشته باشید.
حتماً قبل از پیوند با پزشک کودک خود صحبت کنید تا در مورد عوارض جانبی احتمالی دراز مدت کودکتان بدانید.
مطالعه صدها مطلب علمی در حوزه بیولوژی
آرشیو جدیدترین خبرهای روز دنیای بیولوژی
مترجم: فاطمه فریادرس




