بیماری ها
لوسمی لنفوسیتی حاد (ALL یا Acute Lymphocytic Leukemia)
لوسمی حاد لنفوسیتی (ALL) چیست؟سرطان زمانی شروع میشود که سلولهای بدن شروع به رشد خارج از کنترل میکنند. انواع مختلفی از سرطان وجود دارد. تقریباً سلولها در هر قسمت از بدن میتوانند به سرطان تبدیل شوند.لوسمیها (Leukemias) سرطانهایی هستند که از سلولهایی شروع میشوند که به طور معمول به انواع مختلف سلولهای خونی تبدیل میشوند. اغلب، لوسمی در اشکال اولیه گلبولهای سفید شروع میشود اما برخی از لوسمیها در انواع دیگر سلولهای خونی نیز آغاز میشوند.
انواع مختلفی از لوسمی وجود دارد که عمدتاً بر اساس حاد بودن (سریع الرشد بودن) یا مزمن (رشد کندتر) و بسته به اینکه در سلولهای میلوئید یا سلولهای لنفاوی شروع میشوند، تقسیم میشوند. دانستن نوع خاص سرطان خون به پزشکان کمک میکند تا وضعیت پیش روی (چشم انداز) هر فرد را بهتر پیش بینی کرده و بهترین درمان را برای وی انتخاب کنند.
لوسمی لنفوسیتی حاد (ALL) لوسمی لنفوبلاستیک حاد (acute lymphoblastic leukemia) نیز نامیده میشود. “حاد” به این معنی است که سرطان خون میتواند به سرعت پیشرفت کند و اگر درمان نشود، احتمالاً ظرف چند ماه کشنده خواهد بود. “لنفوسیتی” به این معنی است که از اشکال اولیه (نابالغ) لنفوسیتها – نوعی گلبول سفید – ایجاد میشود.
ALL در مغز استخوان (بخش داخلی نرم برخی از استخوانها، جایی که سلولهای خونی جدید ساخته میشوند) شروع میشود. اغلب، سلولهای لوسمی نسبتاً سریع به خون حمله میکنند. آنها همچنین گاهی اوقات میتوانند به سایر قسمتهای بدن، از جمله غدد لنفاوی، کبد، طحال، سیستم عصبی مرکزی (مغز و نخاع) و بیضهها (در مردان) گسترش یابند. برخی از سرطانها نیز میتوانند از این اندامها شروع شده و سپس به مغز استخوان سرایت کنند اما این سرطانها دیگر سرطان خون نیستند.
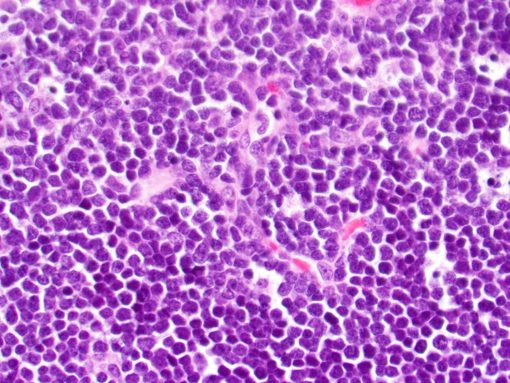
انواع دیگر سرطان که در لنفوسیتها شروع میشوند به عنوان لنفوم (لنفوم غیر هوچکین یا لنفوم هوچکین) شناخته میشوند. در حالی که لوسمیها مانند ALL عمدتاً بر مغز استخوان و خون تأثیر میگذارند، لنفومها عمدتاً غدد لنفاوی یا سایر اندامها را تحت تأثیر قرار میدهند (اما ممکن است مغز استخوان را نیز درگیر کنند). گاهی اوقات تشخیص اینکه سرطان لنفوسیتها، سرطان خون است یا لنفوم دشوار است. معمولاً اگر حداقل 20 درصد از مغز استخوان از لنفوسیتهای سرطانی (به نام لنفوبلاست (lymphoblasts) یا فقط بلاست (blasts)) تشکیل شده باشد، این بیماری لوسمی در نظر گرفته میشود.
مغز استخوان، خون و بافت لنفاوی طبیعی
برای درک لوسمی، دانستن اطلاعاتی در مورد خون و سیستم لنفاوی به شما کمک میکند.
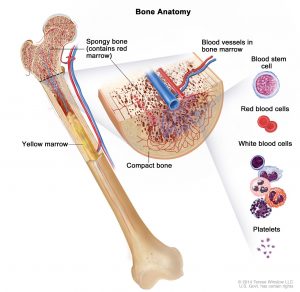
مغز استخوان (Bone marrow)
مغز استخوان بخش داخلی نرم برخی از استخوانها است. از سلولهای خون ساز، سلولهای چربی و بافتهای حمایت کننده تشکیل شده است. بخش کوچکی از سلولهای سازنده خون را سلولهای بنیادی خون تشکیل میدهند.
در داخل مغز استخوان، سلولهای بنیادی خون یک سری تغییرات را برای ساخت سلولهای خونی جدید انجام میدهند. در طی این فرآیند، سلولها به یکی از 3 نوع اصلی از انواع سلولهای خونی تبدیل میشوند:
- سلولهای قرمز خون (Red blood cells)
- پلاکتها (Platelets)
- گلبولهای سفید خون (White blood cells)
سلولهای قرمز خون
گلبولهای قرمز خون (RBC) اکسیژن را از ریهها به سایر بافتهای بدن حمل میکنند و دی اکسید کربن را به ریهها برمیگردانند تا از بدن خارج شود.
پلاکتها
پلاکتها در واقع قطعات سلولی هستند که توسط نوعی سلول در مغز استخوان به نام مگاکاریوسیت (megakaryocyte) ساخته میشوند. پلاکتها در بستن سوراخهای رگهای خونی ناشی از بریدگی یا کبودی حائز اهمیت هستند.
گلبولهای سفید خون
گلبولهای سفید (WBC) به بدن در مبارزه با عفونتها کمک میکنند. انواع اصلی WBCها شامل لنفوسیتها (lymphocytes)، گرانولوسیتها (granulocytes) و مونوسیتها (monocytes) هستند.
لنفوسیتها سلولهای اصلی هستند که بافت لنفاوی – بخش عمدهای از سیستم ایمنی – را تشکیل میدهند. بافت لنفاوی در غدد لنفاوی، تیموس، طحال، لوزهها و آدنوئیدها (adenoids) یافت میشود و در سراسر دستگاه گوارش و تنفس و مغز استخوان پراکنده است.
لنفوسیتها از سلولهایی به نام لنفوبلاست توسعه پیدا میکنند تا به سلولهای بالغ و مبارزه کننده با عفونت تبدیل شوند. 2 نوع اصلی لنفوسیت وجود دارد:
- لنفوسیتهای B (سلولهای B): سلولهای B با ساخت پروتئینهایی به نام آنتی بادی (antibody) به محافظت از بدن کمک میکنند. آنتیبادیها به میکروبها (باکتریها، ویروسها و قارچها) در بدن میچسبند و به سیستم ایمنی کمک میکنند تا آنها را از بین ببرد.
- لنفوسیتهای T (سلولهای T): انواع مختلفی از سلولهای T وجود دارد که هر کدام وظیفه خاصی دارند. برخی از سلولهای T میتوانند مستقیماً میکروبها را از بین ببرند، در حالی که برخی دیگر در تقویت یا کند کردن فعالیت سایر سلولهای سیستم ایمنی نقش دارند.
ALL از اشکال اولیه لنفوسیتها ایجاد میشود. این سرطان میتواند در سلولهای B اولیه یا سلولهای T در مراحل مختلف بلوغ شروع شود.
گرانولوسیتها WBCهایی هستند که گرانولهایی – لکههایی که که در زیر میکروسکوپ قابل مشاهده هستند – در آنها وجود دارد. این گرانولها حاوی آنزیمها و سایر موادی هستند که میتوانند میکروبهایی مانند باکتریها را از بین ببرند. 3 نوع گرانولوسیت – نوتروفیلها (neutrophils)، بازوفیلها (basophils) و ائوزینوفیلها (eosinophils) – با اندازه و رنگ گرانولهایشان از هم متمایز میشوند.
مونوسیتها (Monocytes) همچنین به محافظت از بدن در برابر باکتریها کمک میکنند. پس از حدود یک روز گردش خون، مونوسیتها وارد بافتهای بدن میشوند تا به ماکروفاژ (macrophages) تبدیل شوند که میتواند با احاطه و هضم، برخی میکروبها را از بین ببرد.
آمارهای کلیدی برای لوسمی لنفوسیتی حاد (ALL)
برآوردهای انجمن سرطان آمریکا برای لوسمی لنفوسیتی حاد (ALL) در ایالات متحده برای سال 2022 (شامل کودکان و بزرگسالان) عبارتند از:
- حدود 6660 مورد جدید ALL (3740 مورد در مردان و 2920 در زنان)
- حدود 1560 مرگ ناشی از ALL (880 مورد در مردان و 680 در زنان)
خطر ابتلا به ALL در کودکان کمتر از 5 سال بیشتر است. این خطر سپس تا اواسط دهه 20 سالگی به آرامی کاهش مییابد و پس از 50 سالگی دوباره به آرامی شروع به افزایش میکند. به طور کلی، حدود 4 مورد از هر 10 مورد ALL در بزرگسالان رخ میدهد.
ALL یک سرطان شایع نیست و کمتر از نیمی از یک درصد از کل سرطانها در ایالات متحده را تشکیل میدهد. میانگین خطر ابتلا به ALL در طول زندگی یک فرد در حدود 1 در 1000 است. این خطر در مردان کمی بیشتر از زنان و در سفید پوستان بیشتر از آمریکاییهای آفریقایی تبار است.
بیشتر موارد ALL در کودکان رخ میدهد اما بیشترین مرگ و میر ناشی از ALL (حدود 4 مورد از 5 مورد) در بزرگسالان دیده میشود. کودکان ممکن است به دلیل تفاوت در ماهیت ALL در دوران کودکی و بزرگسالی، تفاوت در روند درمان (بدن کودکان اغلب بهتر از بزرگسالان با درمان تهاجمی مقابله کند) یا ترکیبی از این موارد، بهتر از بزرگسالان عمل میکنند.
علائم و نشانههای لوسمی لنفوسیتی حاد (ALL)
لوسمی لنفوسیتی حاد (ALL) میتواند علائم و نشانههای مختلفی ایجاد کند. بیشتر این موارد در همه انواع ALL رخ میدهند اما برخی از آنها در زیر گروههای خاصی از ALL رایجتر هستند.
علائم ناشی از تعداد کم سلولهای خونی
بیشتر علائم و نشانههای ALL نتیجه کمبود سلولهای خونی طبیعی است که زمانی اتفاق میافتد که سلولهای سرطانی خون، سلولهای خون ساز طبیعی در مغز استخوان را از بین میبرند. این کمبودها در آزمایشات خون خود را نشان میدهند اما میتوانند علائمی از جمله موارد زیر را به همراه داشته باشند:
- احساس خستگی
- احساس ضعف
- احساس سرگیجه یا سبکی سر
- تنگی نفس
- پوست رنگ پریده
- عفونتهایی که از بین نمیروند یا باز میگردند
- کبودی (یا لکههای کوچک قرمز یا بنفش) روی پوست
- خونریزی مانند خونریزی مکرر یا شدید بینی، خونریزی لثه، یا خونریزی شدید قاعدگی در زنان
علائم عمومی
اغلب بیماران مبتلا به ALL نیز چندین علامت غیر اختصاصی دارند. این موارد میتواند شامل موارد زیر باشد:
- کاهش وزن
- تب
- تعریق شبانه
- از دست دادن اشتها
البته اینها فقط علائم ALL نیستند و بیشتر در اثر عواملی غیر از سرطان خون ایجاد میشوند.
تورم در شکم
سلولهای لوسمی ممکن است در کبد و طحال انباشته شده و بزرگتر شوند. این پدیده ممکن است به صورت پری یا تورم شکم یا احساس سیری پس از صرف مقدار کمی غذا مشاهده شود. دندههای پایینی معمولاً این اندامها را میپوشانند اما وقتی اندامها بزرگ میشوند، پزشک میتواند آنها را حس کند.
بزرگ شدن غدد لنفاوی
سرطانیهایی که به غدد لنفاوی نزدیک به سطح بدن (مانند دو طرف گردن، کشاله ران، یا در نواحی زیر بغل) گسترش یافتهاند، ممکن است به صورت تودههایی در زیر پوست مشاهده شوند. غدد لنفاوی داخل قفسه سینه یا شکم نیز ممکن است متورم شوند اما این گرهها تنها با آزمایشهای تصویر برداری مانند سی تی اسکن یا ام آر آی قابل تشخیص هستند.
درد استخوان یا مفصل
گاهی اوقات سلولهای لوسمی در نزدیکی سطح استخوان یا داخل مفصل ایجاد میشوند که میتواند منجر به درد استخوان یا مفصل شود.
سرایت به سایر اندامها
در موارد غیر رایج، ALL به سایر اندامها گسترش مییابد:
- اگر ALL به مغز و نخاع سرایت کند، میتواند باعث سردرد، ضعف، تشنج، استفراغ، مشکل در تعادل، ضعف یا بی حسی عضلات صورت یا تاری دید شود.
- ALL ممکن است در داخل قفسه سینه پخش شود، جایی که میتواند باعث تجمع مایع و مشکل در تنفس شود.
- به ندرت، ALL ممکن است به پوست، چشمها، بیضهها، تخمدانها، کلیهها یا سایر اندامها سرایت کند.
علائم ناشی از تیموس بزرگ و متورم شده
زیرگروه سلولهای T در ALL اغلب تیموس را که اندام کوچکی در وسط قفسه سینه پشت جناغ (استخوان سینه) و جلوی نای (windpipe) است، تحت تاثیر قرار میدهد. تیموس بزرگ شده میتواند روی نای فشار بیاورد که خود این اتفاق میتواند منجر به سرفه یا مشکل در تنفس شود.
superior vena cava (SVC)، سیاهرگ بزرگی که خون را از سر و بازوها به سمت قلب میبرد، از کنار تیموس عبور میکند. اگر تیموس بزرگ شده باشد، ممکن است بر روی SVC فشار بیاورد و باعث شود خون در وریدها دچار “بازگشت” شود. این پدیده به عنوان سندرم SVC شناخته میشود که خود میتواند باعث باعث رخ دادن علائمی همچون موارد زیر شود:
- تورم در صورت، گردن، بازوها و بالای سینه (گاهی اوقات با رنگ قرمز مایل به آبی)
- سردرد
- سرگیجه
- تغییر در هوشیاری اگر بر مغز تأثیر بگذارد
چه چیزی باعث ابتلا به لوسمی لنفوسیتی حاد (ALL) میشود؟
برخی از افراد مبتلا به لوسمی لنفوسیتی حاد (ALL) دارای یک یا چند عامل خطرزا شناخته شده هستند اما بسیاری از آنها چنین عواملی را دارا نیستند. حتی زمانی که فردی دارای یک یا چند عامل خطرزا باشد، تشخیص اینکه آیا واقعاً این عوامل باعث سرطان خون شده است یا خیر، بسیار سخت است.
پیشرفت بزرگی در درک اینکه چگونه تغییرات خاصی در DNA سلولهای طبیعی مغز استخوان میتواند باعث تبدیل آنها به سلولهای سرطانی خون شود، حاصل شده است. DNA درون سلولهای ما، ژنهای ما را میسازد که عملکرد سلولهای ما را کنترل میکنند. ما تمایل داریم شبیه والدین خود باشیم زیرا آنها منبع DNA ما هستند. اما ژنهای ما چیزهایی بیشتر از ظاهر ما را تحت تأثیر میگذارند.
برخی از ژنها زمان رشد سلولهای ما، تقسیم برای ساختن سلولهای جدید و مرگ در زمان مناسب را کنترل میکنند:
- ژنهای خاصی که به رشد، تقسیم یا زنده ماندن سلولها کمک میکنند، انکوژن (oncogene) نامیده میشوند.
- ژنهایی که رشد و تقسیم سلولی را تحت کنترل نگه میدارند یا باعث مرگ سلولها در زمان مناسب میشوند، ژنهای سرکوب کننده تومور (tumor suppressor genes) نامیده میشوند.
هر بار که یک سلول به 2 سلول جدید تقسیم میشود، باید یک کپی جدید از کروموزومهای خود (رشتههای بلند DNA) بسازد.
این فرآیند کامل نیست و ممکن است خطاهایی در آن رخ دهد که بر ژنهای درون کروموزومها تأثیر بگذارد. سرطانها (از جمله ALL) میتوانند در اثر جهشها (تغییرات) ایجاد شوند که انکوژنها را فعال میکنند یا ژنهای سرکوبکننده تومور را خاموش میکنند. این نوع تغییرات میتوانند سلولهای مغز استخوان را از فرآیند بالغ شدن که به طور طبیعی در آنها رخ میدهد دور کرده یا به رشد خارج از کنترل سلولها کمک کنند.
جهش در بسیاری از ژنهای مختلف را میتوان در سلولهای ALL یافت اما تغییرات بزرگتر در یک یا چند کروموزوم نیز رایج است. اگرچه این تغییرات شامل قطعات بزرگتری از DNA است اما اثرات آنها احتمالاً به دلیل تغییرات فقط در یک یا چند ژن است که در آن قسمت از کروموزوم وجود دارد. چندین نوع تغییر کروموزوم ممکن است در سلولهای ALL یافت شود:
جابجایی (Translocations) شایع ترین نوع تغییر در کروموزومها است که میتواند منجر به سرطان خون شود. جابجایی به این معنی است که DNA از یک کروموزوم جدا شده و به کروموزوم دیگری متصل میشود. نقطهای روی کروموزوم که در آن شکستگی رخ میدهد میتواند بر ژنهای مجاور تأثیر بگذارد – برای مثال میتواند انکوژنها را روشن کند یا ژنهایی را که به طور معمول به بلوغ سلول کمک میکنند، خاموش کند.
شایع ترین جابجایی در ALL در بزرگسالان به عنوان کروموزوم فیلادلفیا (Philadelphia chromosome) شناخته میشود که مبادله ای از DNA بین کروموزومهای 9 و 22 است که به اختصار (22;9) tنامیده میشود. بسیاری از جابجاییهای دیگری که کمتر رایج هستند نیز میتوانند رخ دهند، از جمله آنهایی که بین کروموزومهای 4 و 11، (11;4) t، یا 8 و 14، (14;8) tهستند.
سایر تغییرات کروموزومی مانند حذف (از بین رفتن بخشی از کروموزوم یا deletion) و وارونگی (بازآرایی DNA در قسمتی از کروموزوم یا inversion) نیز گاهی در سلولهای ALL یافت میشود، اگرچه کمتر رایج هستند. در بسیاری از موارد ALL، تغییرات ژنی که منجر به لوسمی میشود مشخص نیستند.
پزشکان در تلاش هستند تا دریابند که چرا این تغییرات رخ میدهند و چگونه هر یک از آنها ممکن است منجر به ایجاد سرطان خون شوند. اما انواع مختلفی از ALL وجود دارد و حتی در یک زیر گروه، همه موارد ALL دارای تغییرات ژنی یا کروموزومی یکسانی نیستند. برخی از تغییرات شایعتر از سایرین هستند و به نظر میرسد که برخی تأثیر بیشتری بر وضعیت آتی فرد نسبت به سایرین دارند.
تغییرات ژنی ارثی در مقابل تغییرات ژنی اکتسابی
برخی از افراد مبتلا به انواع خاصی از سرطان، جهشهای DNA را از والدین به ارث برده اند که خطر ابتلا به این بیماری را در آنها افزایش میدهد. اگرچه گاهی اوقات این اتفاق در مورد ALL رخ میدهد، مانند برخی از سندرمهای ژنتیکی ذکر شده در عوامل خطرزا برای لوسمی حاد لنفوسیتی (ALL)، اما جهشهای ارثی علت شایع ALL نیستند.
معمولاً جهشهای DNA مربوط به ALL در طول زندگی فرد به دست میآیند، نه اینکه ارثی باشند. آنها ممکن است ناشی از علل بیرونی مانند قرار گرفتن در معرض تشعشعات یا مواد شیمیایی سرطان زا باشند اما در بیشتر موارد دلیل بروز آنها مشخص نیست. بسیاری از این تغییرات ژنی احتمالاً فقط رویدادهای تصادفی هستند که گاهی اوقات در داخل سلول اتفاق میافتند، بدون اینکه علت خارجی داشته باشند. این تغییرات میتوانند با افزایش سن ایجاد شوند که ممکن است به توضیح اینکه چرا ALL در بزرگسالان با افزایش سن افراد شایعتر میشود کمک کند.
زیر انواع لوسمی لنفوسیتی حاد (ALL)
سیستمهای مختلفی برای طبقه بندی ALL به زیر گروهها استفاده شده است.
در دهه 1970، گروهی از متخصصان لوسمی فرانسوی، آمریکایی و بریتانیایی (FAB) ALL را بر اساس روشی که سلولهای لوسمی پس از رنگآمیزی معمول زیر میکروسکوپ مشاهده شدند، به 3 زیرگروه (L1، L2 و L3) تقسیم کردند. این سیستم که به عنوان طبقه بندی FAB شناخته میشود، تا حد زیادی جایگزین شده است، زیرا آزمایشات آزمایشگاهی جدیدتر، اکنون به پزشکان اجازه میدهد تا ALL را با دقت بیشتری طبقه (سطح) بندی کنند.
پزشکان دریافتهاند که آزمایشهای سیتوژنتیک (cytogenetic)، فلوسیتومتری (flow cytometry) و سایر آزمایشهای آزمایشگاهی اطلاعات دقیقتری را در مورد زیر گروه ALL و آینده بیمار ارائه میدهند. این آزمایشها به تقسیم ALL به گروهها بر اساس تغییرات ژن و کروموزوم در سلولهای لوسمی کمک میکند.
سیستم سازمان جهانی بهداشت (WHO) که اخیراً در سال 2016 به روز شده است، شامل برخی از این عوامل برای طبقه بندی بهتر ALL میباشد. سیستم WHO ALL را به چند گروه تقسیم میکند:
ALL سلول B
ALL سلول B با ناهنجاریهای ژنتیکی خاص (تغییرات ژنی یا کروموزومی)
- ALL سلول B با هیپودیپلوئیدی (hypodiploidy ، سلولهای لوسمی کمتر از 44 کروموزوم دارند [سلولهای طبیعی دارای 46 کروموزوم هستند])
- ALL سلول B با هیپردیپلوئیدی (hyperdiploidy، سلولهای لوسمی بیش از 50 کروموزوم دارند)
- ALL سلول B با جابجایی بین کروموزومهای 9 و 22 (کروموزوم فیلادلفیا که ژن جوش خورده BCR-ABL1 را ایجاد میکند)
- سلول B ALL با جابجایی بین کروموزوم 11 و کروموزوم دیگر
- ALL سلول B با جابجایی بین کروموزومهای 12 و 21
- ALL سلول B با جابجایی بین کروموزومهای 1 و 19
- ALL سلول B با جابجایی بین کروموزومهای 5 و 14
- سلول B ALL با تقویت (کپی بیش از حد) بخشی از کروموزوم 21 (iAMP21)*
- ALL سلول B با جابهجاییهایی که شامل تیروزین کینازها یا گیرندههای سیتوکین میشوند (همچنین به عنوان «ALL مشابه BCR-ABL1» نیز شناخته میشوند)*
ALL سلولT
- لوسمی لنفوبلاستیک پیش ساز سلول T اولیه (Early T-cell precursor lymphoblastic leukemia)*
* هنوز مشخص نیست که آیا شواهد کافی مبنی بر اینکه این گروه منحصر به فرد است (به این معنی که هنوز یک “دسته موقتی” است) وجود دارد یا خیر.
لوسمیهای حاد با ویژگیهای مختلط (Mixed lineage acute leukemias)
تعداد کمی از لوسمیهای حاد دارای ویژگیهای لنفوسیتی و میلوئیدی هستند. گاهی اوقات سلولهای لوسمی دارای هر دو صفت میلوئیدی و لنفوسیتی در سلولهای مشابه هستند. در موارد دیگر، فرد ممکن است برخی از سلولهای لوسمی با ویژگیهای میلوئیدی و برخی دیگر با ویژگیهای لنفوسیتی داشته باشد. این نوع لوسمیها را میتوان لوسمی با ویژگیهای مختلط، لوسمی تمایز نیافته حاد (acute undifferentiated leukemia)، یا لوسمی حاد فنوتیپ مختلط (MPAL) نامید.
عوامل خطرزا برای لوسمی لنفوسیتی حاد (ALL)
عامل خطرزا چیزی است که شانس ابتلا به بیماری مانند سرطان را افزایش میدهد. برخی از عوامل خطرزا، مانند سیگار کشیدن، قابل کنترل هستند. سایر موارد، مانند سن یا سابقه خانوادگی فرد، قابل تغییر نیستند.
اما داشتن یک عامل خطرزا یا حتی چندین عامل به این معنی نیست که قطعاً به این بیماری مبتلا خواهید شد. بسیاری از افرادی که به این بیماری مبتلا میشوند ممکن است عوامل خطرزا شناخته شده کمی داشته باشند یا اصلاً چنین عواملی در آنها وجود نداشته باشد.
تنها تعداد انگشت شماری از عوامل خطرزا شناخته شده برای لوسمی لنفوسیتی حاد (ALL) وجود دارد.
قرارگیری در معرض تشعشع
قرار گرفتن در معرض سطوح بالای تابش یک عامل خطرزا برای لوسمی ALL و حاد میلوئیدی (AML) است. به عنوان مثال، بازماندگان بمب اتمی ژاپنی در معرض خطر ابتلا به لوسمی حاد بودند.
درمان سرطان با پرتو درمانی نیز خطر ابتلا به سرطان خون را افزایش میدهد، اگرچه این موضوع برای AML بیشتر از ALL صدق میکند. اگر شیمی درمانی و پرتو درمانی به طور همزمان استفاده شوند، به نظر میرسد خطر بیشتر باشد.
خطرات احتمالی لوسمی ناشی از قرار گرفتن در معرض سطوح پایین تابش، مانند آزمایشهای تصویر برداری پزشکی مانند اشعه ایکس یا سی تی اسکن، به خوبی شناخته نشده است. قرار گرفتن در معرض چنین تشعشعی، به ویژه در اوایل زندگی، ممکن است خطر ابتلا به سرطان خون را افزایش دهد، اما این پدیده کاملا مشخص نیست. اگر احتمال ابتلا افزایش یافته باشد، این افزایش احتمالاً کوچک است اما برای ایمن بودن، بیشتر پزشکان سعی میکنند تا حد امکان قرار گرفتن در معرض تابش را در این آزمایشها، به ویژه برای کودکان و زنان باردار، محدود کنند.
قرار گرفتن در معرض مواد شیمیایی خاص
خطر ALL ممکن است با قرار گرفتن در معرض داروهای شیمی درمانی خاص و برخی مواد شیمیایی دیگر از جمله بنزن (benzene) افزایش یابد. بنزن در بسیاری از صنایع برای تولید محصولات دیگر استفاده میشود و همچنین در دود سیگار و برخی از چسبها، محصولات پاک کننده، مواد شوینده، لوازم هنری و پاک کنندههای رنگ نیز وجود دارد.
قرار گرفتن در معرض مواد شیمیایی قوی تر با افزایش خطر AML نسبت به ALL مرتبط است.
عفونتهای ویروسی خاص
عفونت با لنفوم سلول T انسانی یا ویروس لوسمی-1 (HTLV-1) میتواند باعث ایجاد نوع نادری از ALL سلول T شود. بیشتر موارد ابتلا به این نوع در ژاپن و منطقه کارائیب رخ میدهد. این بیماری در ایالات متحده رایج نیست.
همچنین در آفریقا، ویروس اپشتین بار (EBV) با لنفوم بورکیت (Burkitt lymphoma) و به نوعی از ALL مرتبط است. در ایالات متحده، EBV اغلب باعث مونونوکلئوز عفونی (infectious mononucleosis) میشود. همچنین این ویروس با نوعی لنفوم مرتبط است که میتواند پس از پیوند سلولهای بنیادی رخ دهد (معروف به اختلال لنفوپرولیفراتیو پس از پیوند (post-transplant lymphoproliferative disorder) یا PTLD).
برخی از سندرمهای ژنتیکی
به نظر نمیرسد که ALL خود دارای یک جزء ارثی قوی باشد. یعنی به نظر نمیرسد این بیماری در خانوادهها وجود داشته باشد، بنابراین اگر یکی از اعضای خانواده (به غیر از دوقلوهای همسان) به این بیماری مبتلا باشد، خطر ابتلا به آن برای سایر افراد خانواده افزایش نمییابد.
اما برخی از سندرمهای ژنتیکی وجود دارد (که برخی از آنها میتواند از والدین به ارث برسد) که به نظر میرسد خطر ابتلا به ALL را افزایش میدهند. این سندرومها شامل:
- سندرم داون (Down syndrome)
- سندرم کلاین فلتر (Klinefelter syndrome)
- کم خونی فانکونی (Fanconi anemia)
- سندرم بلوم (Bloom syndrome)
- آتاکسی تلانژکتازی (Ataxia-telangiectasia)
- نوروفیبروماتوز (Neurofibromatosis)
- سندرم Li-Fraumeni
سن
احتمال بروز ALL در کودکان و بزرگسالان بالای 50 سال بیشتر است.
نژاد یا قومیت
ALL در سفید پوستان بیشتر از آمریکاییهای آفریقایی تبار شایع است اما دلایل این پدیده مشخص نیست.
جنسیت
ALL در مردان کمی بیشتر از زنان رایج است. دلیل این امر نیز نامعلوم است.
داشتن یک دو قلو یکسان مبتلا به ALL
برای فردی که یک دو قلو همسان دارد و او در سال اول زندگی به ALL مبتلا شده است، خطر ابتلا به ALL افزایش مییابد.
عوامل خطرزا نامشخص، اثبات نشده یا بحث برانگیز
عوامل دیگری که برای پیوند احتمالی به ALL مورد مطالعه قرار گرفته اند، عبارتند از:
- قرار گرفتن در معرض میدانهای الکترومغناطیسی (مانند زندگی در نزدیکی خطوط برق یا استفاده از تلفن همراه)
- قرار گرفتن در محل کار حاوی گازوئیل، بنزین، آفت کشها و برخی مواد شیمیایی دیگر
- سیگار کشیدن
- قرار گرفتن در معرض رنگ مو
تاکنون هیچ یک از این عوامل به طور قطعی با ALL مرتبط نبوده اند اما تحقیقات در این زمینهها ادامه دارد.
آیا لوسمی لنفوسیتی حاد (ALL) میتواند زودتر تشخیص داده شود؟
برای بسیاری از انواع سرطان، یافتن زود هنگام بیماری، درمان را آسانتر میکند. انجمن سرطان آمریکا آزمایشهای غربالگری را برای تشخیص زود هنگام برخی سرطانها در افرادی که بدون هیچ علامتی هستند، توصیه میکند.
اما در حال حاضر هیچ آزمایش خاصی برای تشخیص زود هنگام لوسمی لنفوسیتی حاد (ALL) توصیه نمیشود. بهترین راه برای تشخیص زود هنگام سرطان خون این است که هر گونه علائم یا نشانههای احتمالی سرطان خون فوراً به پزشک گزارش شود.
در رابطه با افرادی که در معرض خطر ابتلا به ALL هستند:
برخی از افراد به دلیل یک اختلال ژنتیکی مانند سندرم داون یا به دلیل اینکه قبلاً با داروهای شیمی درمانی خاص یا پرتو درمانی تحت درمان قرار گرفته بودند، در معرض خطر بیشتری برای ابتلا به ALL (یا سایر لوسمیها) هستند. اکثر پزشکان توصیه میکنند که این افراد معاینات پزشکی دقیق و منظم داشته باشند. اگرچه خطر ابتلا به سرطان خون در بین افراد جمعیت عمومی بیشتر است اما همچنان این احتمال برای اکثر این افراد بسیار کم است.
آزمایشات لوسمی لنفوسیتی حاد (ALL)
برخی علائم و نشانهها میتوانند نشان دهند که ممکن است فرد مبتلا به لوسمی لنفوسیتی حاد (ALL) باشد اما آزمایشهایی برای تایید این تشخیص لازم است.
تاریخچه پزشکی و معاینه فیزیکی
اگر علائم و نشانههایی دارید که نشان میدهد ممکن است سرطان خون داشته باشید، پزشک میخواهد تاریخچه پزشکی کاملی از جمله مدت زمانی که علائم داشتهاید و اگر احتمالاً در معرض هر چیزی قرار گرفتهاید که یک عامل خطر محسوب میشود را دریافت کند.
در طول معاینه فیزیکی، پزشک احتمالاً بر روی هر غده لنفاوی بزرگ شده، مناطق دارای خونریزی یا کبودی یا علائم احتمالی عفونت تمرکز خواهد کرد. چشمها، دهان و پوست با دقت بررسی میشوند و ممکن است یک معاینه کامل سیستم عصبی انجام شود. شکم شما برای تشخیص بزرگ شدن طحال یا کبد بررسی میشود.
اگر دلیلی وجود داشته باشد که فکر کنید سطوح پایین سلولهای خونی ممکن است باعث علائم شما شود (کم خونی، عفونت، خونریزی یا کبودی و غیره)، پزشک به احتمال زیاد آزمایش خون را برای بررسی تعداد سلولهای خونی شما تجویز میکند. همچنین ممکن است به یک متخصص هماتولوژی ارجاع داده شوید، پزشکی که در بیماریهای خونی (از جمله سرطان خون) تخصص دارد.
آزمایشهایی که برای تشخیص و طبقه بندی ALL استفاده میشوند
اگر پزشک شما فکر میکند که شما ممکن است سرطان خون داشته باشید، برای اطمینان باید نمونههایی از سلولهای خون و مغز استخوان شما را بررسی کند. سایر نمونههایی مانند بافت و سلولهای شما نیز ممکن است برای کمک به درمان از شما گرفته شوند.
آزمایشات خون
نمونه خون برای آزمایشهای ALL عموماً از ورید (سیاهرگ) بازو گرفته میشود.
شمارش کامل خون (CBC) و اسمیر خون محیطی (peripheral blood smear): CBC تعداد گلبولهای قرمز، گلبولهای سفید و پلاکتها را اندازه گیری میکند. این آزمایش اغلب همراه با یک بازه اختلافی انجام میشود که به تعداد انواع مختلف گلبولهای سفید خون نگاه میکند. این آزمایشات اغلب اولین آزمایشاتی است که بر روی بیماران مشکوک به ابتلا به مشکلات خونی انجام میشود.
برای اسمیر خون محیطی (گاهی اوقات فقط اسمیر نامیده میشود)، یک قطره خون روی یک اسلاید مالیده میشود و سپس زیر میکروسکوپ آن را نگاه میکنند تا ببیند سلولها چگونه به نظر میرسند. تغییر در تعداد و ظاهر سلولها اغلب به تشخیص سرطان خون کمک میکند.
اکثر بیماران مبتلا به ALL دارای تعداد زیادی گلبول سفید نابالغ به نام لنفوبلاست (یا فقط بلاست) در خون خود هستند و گلبولهای قرمز یا پلاکت کافی ندارند. لنفوبلاستها به طور معمول در خون یافت نمیشوند و مانند گلبولهای سفید طبیعی و بالغ عمل نمیکنند.
اگرچه این یافتهها ممکن است نشان دهنده سرطان خون باشد، این بیماری معمولاً بدون بررسی نمونهای از سلولهای مغز استخوان تشخیص داده نمیشود.
آزمایشات شیمیایی خون: آزمایشات شیمیایی خون مقدار برخی مواد شیمیایی را در خون اندازه گیری میکند اما برای تشخیص سرطان خون استفاده نمیشود. در بیمارانی که قبلاً به ALL مبتلا هستند، این آزمایشها میتوانند به تشخیص مشکلات کبدی یا کلیوی ناشی از انتشار سلولهای لوسمی یا عوارض جانبی برخی داروهای شیمی درمانی کمک کنند. این آزمایشات همچنین به تعیین اینکه آیا برای اصلاح سطوح پایین یا بالای برخی از مواد معدنی در خون نیاز به درمان است یا خیر، کمک میکند.
آزمایشهای انعقادی: آزمایشهای انعقاد خون ممکن است برای اطمینان از لخته شدن درست خون انجام شود.
آزمایشات مغز استخوان
سرطان خون از مغز استخوان شروع میشود، بنابراین بررسی مغز استخوان برای سلولهای سرطان خون بخش مهمی از تشخیص آن است.
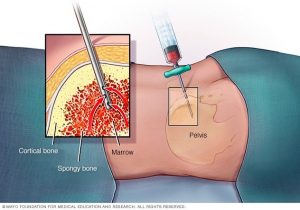
آسپیراسیون (aspiration) و بیوپسی (biopsy یا نمونه برداری) مغز استخوان: نمونههای مغز استخوان با آسپیراسیون مغز استخوان و بیوپسی به دست میآیند – آزمایشهایی که معمولاً همزمان انجام میشوند. نمونهها معمولاً از پشت استخوان لگن (hip) گرفته میشوند، اگرچه در برخی موارد ممکن است از جناغ (استخوان سینه) یا استخوانهای دیگر نیز نمونه برداری شود.
در آسپیراسیون مغز استخوان، روی یک میز (به پهلو یا روی شکم) دراز میکشید. پس از تمیز کردن پوست روی لگن، پزشک با تزریق یک بی حس کننده موضعی، پوست و سطح استخوان را بی حس میکند که ممکن است باعث سوختن یا سوزش مختصری شود. سپس یک سوزن نازک و تو خالی به استخوان وارد میشود و از یک سرنگ برای مکیدن مقدار کمی از مغز استخوان مایع استفاده میشود. حتی با استفاده از داروی بیهوشی، اکثر بیماران هنوز در هنگام برداشتن مغز استخوان کمی درد دارند.
بیوپسی مغز استخوان معمولاً درست بعد از آسپیراسیون انجام میشود. یک تکه کوچک از استخوان و مغز آن را با یک سوزن کمی بزرگ تر که به طرف پایین و به داخل استخوان فشار داده میشود، برداشته میشود. با بی حسی موضعی، اکثر بیماران فقط مقداری فشار و کشش از بیوپسی را احساس میکنند اما برخی ممکن است درد مختصری را نیز احساس کنند. پس از انجام بیوپسی، برای کمک به جلوگیری از خونریزی، به محل فشار وارد میشود.
این آزمایشات مغز استخوان برای کمک به تشخیص سرطان خون استفاده میشود. آنها همچنین ممکن است بعداً دوباره انجام شوند تا مشخص شود که آیا لوسمی به درمان پاسخ میدهد یا خیر.
تستهای آزمایشگاهی برای تشخیص و طبقه بندی ALL استفاده میشود
یک یا چند مورد از آزمایشهای آزمایشگاهی زیر ممکن است بر روی نمونهها برای تشخیص AML و یا تعیین زیر نوع خاص ALL انجام شود.
معاینات معمول با میکروسکوپ: نمونههای مغز استخوان (و گاهی اوقات خون) توسط پاتولوژیست (پزشک متخصص در آزمایشهای آزمایشگاهی) با میکروسکوپ بررسی میشوند و ممکن است توسط هماتولوژیست یا انکولوژیست بیمار (پزشک متخصص سرطان و بیماریهای خونی) بررسی شوند.
پزشکان به اندازه، شکل و سایر ویژگیهای گلبولهای سفید خون در نمونهها نگاه میکنند تا آنها را به انواع خاصی دسته بندی کنند.
یک عامل کلیدی این است که آیا سلولها بالغ به نظر میرسند (مانند سلولهای خونی طبیعی) یا نابالغ (بدون ویژگیهای سلولهای خونی طبیعی). نابالغ ترین سلولها لنفوبلاست (یا فقط بلاست) نامیده میشوند.
تعیین اینکه چند درصد از سلولهای مغز استخوان بلاست هستند، اهمیت ویژه ای دارد. تشخیص ALL به طور کلی مستلزم آن است که حداقل 20 درصد از سلولهای مغز استخوان بلاست باشند. در شرایط عادی، بلاستها بیش از 5 درصد از سلولهای مغز استخوان را تشکیل نمیدهند.
گاهی اوقات فقط شمارش و نگاه کردن به سلولها منجر به تشخیص قطعی نمیشود و آزمایشهای آزمایشگاهی دیگری مورد نیاز است.
سیتوشیمی (Cytochemistry): در آزمایشهای سیتوشیمی، سلولها روی یک لام قرار میگیرند و در معرض مواد شیمیایی (رنگها) قرار میگیرند که فقط با برخی از انواع سلولهای سرطانی خون واکنش نشان میدهند. این رنگها باعث تغییرات رنگی میشوند که در زیر میکروسکوپ قابل مشاهده است و میتواند به پزشک کمک کند تا نوع سلولهای موجود را تعیین کند. به عنوان مثال، نوعی رنگ بخشی از سلولهای لوسمی میلوئید حاد (AML) را سیاه میکند اما هیچ تاثیری بر سلولهای ALL ندارد.
فلوسیتومتری (Flow cytometry) و ایمونوهیستوشیمی (immunohistochemistry): هم برای فلوسیتومتری و هم برای ایمونوهیستوشیمی، نمونههای سلولی با آنتی بادیهایی تیمار میشوند که پروتئینهایی هستند که فقط به پروتئینهای خاصی روی سلولها میچسبند. در ایمونوهیستوشیمی، سلولها زیر میکروسکوپ بررسی میشوند تا بررسی کنند که آیا آنتیبادیها به آنها چسبیدهاند یا نه (یعنی آنها پروتئینها را دارند)؛ در حالی که برای فلوسیتومتری از دستگاه خاصی استفاده میشود.
این آزمایشها برای ایمونوفنوتایپ (immunophenotype) – طبقهبندی سلولهای لوسمی بر اساس پروتئینهای موجود بر روی سطح یا درون سلولها – استفاده میشوند. این نوع آزمایش برای تعیین نوع دقیق لوسمی بسیار مفید است. این آزمایش برای تشخیص سرطان خون، اغلب روی سلولهای مغز استخوان انجام میشود اما میتوان آن را روی سلولهای خون، غدد لنفاوی و سایر مایعات بدن نیز انجام داد.
برای ALL، این تستها اغلب برای کمک به تعیین زیر شاخه دقیق در افرادی که قبلاً بر اساس آزمایشهای دیگر تشخیص داده شده است که ALL دارند، استفاده میشوند.
آزمایشات کروموزومی
این آزمایشها کروموزومها (رشتههای بلند DNA) درون سلولها را بررسی میکنند. سلولهای طبیعی انسان حاوی 23 جفت کروموزوم (بستههای DNA) هستند. در ALL، سلولها گاهی اوقات تغییرات کروموزومی دارند. شناخت این تغییرات میتواند به شناسایی انواع خاصی از ALL کمک کند و میتواند در تعیین چشم انداز بیمار و پاسخ احتمالی به برخی از درمانها مهم باشد. به همین دلیل، آزمایش کروموزوم بخشی استاندارد از روند پیش رو برای ALL است.
شایع ترین تغییر کروموزومی در ALL جابجایی است که در آن، 2 کروموزوم مقداری از DNA خود را تعویض میکنند، به طوری که بخشی از یک کروموزوم به بخشی از کروموزوم متفاوت متصل میشود. شایع ترین تغییر کروموزوم در ALL بزرگسالان، جابجایی است که منجر به کوتاه شدن کروموزوم 22 (به نام کروموزوم فیلادلفیا) میشود. حدود 1 نفر از هر 4 بزرگسال مبتلا به ALL این ناهنجاری را در سلولهای لوسمی خود دارند. این تغییر به ویژه مهم است زیرا میتواند با داروهای خاصی مورد هدف قرار گیرد.
سیتوژنتیک (Cytogenetics): برای این آزمایش، سلولها در ظروف آزمایشگاهی رشد داده میشوند تا زمانی که شروع به تقسیم کنند. سپس کروموزومها زیر میکروسکوپ بررسی میشوند تا هرگونه تغییری را تشخیص دهند.
از آن جایی که شروع تقسیم سلولها زمان میبرد، آزمایش سیتوژنتیک اغلب حدود 2 تا 3 هفته طول میکشد.
همه تغییرات کروموزومی را نمیتوان در زیر میکروسکوپ مشاهده کرد. اغلب سایر آزمایشات آزمایشگاهی میتوانند به یافتن این تغییرات کمک کنند.
هیبریداسیون در محل فلورسنت (FISH): هیبریداسیون در محل فلورسنت روش دیگری برای بررسی کروموزومها و ژنها است. این آزمایش از رنگهای فلورسنت ویژه ای استفاده میکند که فقط به ژنهای خاص یا قسمتهایی از کروموزومهای خاص متصل میشوند. FISH میتواند اکثر تغییرات کروموزومی (مانند جابهجاییها) را که در زیر میکروسکوپ در آزمایشهای سیتوژنتیک استاندارد قابل مشاهده است و همچنین برخی از تغییرات بسیار کوچک را پیدا کند که با آزمایشهای سیتوژنتیک معمولی قابل مشاهده نیستند.
FISH را میتوان در نمونههای معمولی خون یا مغز استخوان استفاده کرد. از آن جایی که سلولها برای این آزمایش نیازی به تقسیم ندارند، میتوان از آن برای مشاهده سلولهای بافتهای دیگر مانند نمونههای غدد لنفاوی نیز استفاده کرد. این روش بسیار دقیق است و معمولاً میتواند در عرض چند روز نتیجه دهد. اما از آنجایی که FISH فقط تغییرات ژنی خاصی را آزمایش میکند (و به طور کلی کروموزومها را بررسی نمیکند)، بهتر است به دنبال تغییراتی باشید که بر اساس نوع سرطان خون افراد مهم هستند.
واکنش زنجیرهای پلیمراز (PCR): این یک آزمایش DNA بسیار حساس است که میتواند تغییرات ژنی و کروموزومی خاصی را که بسیار کوچک هستند، تشخیص دهد که با میکروسکوپ قابل مشاهده نیست، حتی اگر سلولهای سرطان خون بسیار کمی در نمونه وجود داشته باشد. مانند FISH، برای یافتن تغییرات ژنی خاص و نه برای بررسی کلی کروموزومها استفاده میشود.
اگر سلولهای لوسمی تغییر ژنی (یا کروموزومی) خاصی داشته باشند، پس از درمان میتوان از PCR برای یافتن تعداد کمی از سلولهای سرطانی خون که ممکن است با میکروسکوپ قابل مشاهده نباشد، استفاده کرد.
سایر آزمایشات مولکولی و ژنتیکی
انواع جدیدتر آزمایشات آزمایشگاهی نیز میتواند بر روی نمونهها انجام شود تا به دنبال ژن خاص یا سایر تغییرات در سلولهای لوسمی باشد.
پونکسیون کمری (تپ ستون فقرات یا Lumbar puncture)
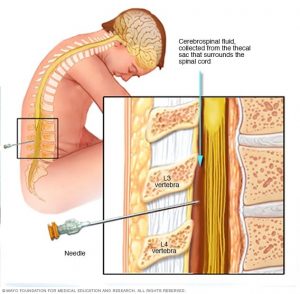
ALL میتواند به ناحیه اطراف مغز و نخاع گسترش یابد. برای بررسی این گسترش، پزشکان نمونه ای از مایع را از آن ناحیه (مایع مغزی نخاعی یا CSF) برای آزمایش بر میدارند.
ممکن است برای این آزمایش به پهلو دراز بکشید یا بنشینید. پزشک ابتدا ناحیه ای را در قسمت پایین کمر روی ستون فقرات بی حس میکند. سپس یک سوزن کوچک و توخالی بین استخوانهای ستون فقرات و در ناحیه اطراف نخاع قرار داده میشود تا مقداری مایع نخاعی برداشته شود.
پونکسیون کمری همچنین میتواند برای قرار دادن داروهای شیمی درمانی در CSF استفاده شود تا از گسترش لوسمی به نخاع و مغز جلوگیری شده یا به درمان آنها کمک کرد.
بیوپسی غدد لنفاوی
یک غدد لنفاوی یا بخشی از یک غدد لنفاوی اغلب برای کمک به تشخیص لنفوم برداشته میشود اما در مورد سرطان خون به ندرت به این کار نیاز است زیرا تشخیص معمولاً با بررسی خون و مغز استخوان انجام میشود.
در این روش، جراح پوست را برش میدهد تا تمام یا بخشی از غدد لنفاوی را بردارد. اگر گره درست در زیر پوست باشد، این یک عمل ساده است که اغلب با بیحسی موضعی انجام میشود، اما اگر گره در داخل قفسه سینه یا شکم باشد، از بیهوشی عمومی برای خواباندن شما در طول بیوپسی استفاده میشود.
هنگامی که کل غدد لنفاوی برداشته میشود، بیوپسی غدد لنفاوی excisional نامیده میشود. اگر تنها بخشی از غدد لنفاوی برداشته شود، بیوپسی غدد لنفاوی incisional نامیده میشود.
تستهای تصویر برداری
تستهای تصویر برداری از اشعه ایکس، امواج صوتی، میدانهای مغناطیسی یا ذرات رادیو اکتیو برای ایجاد تصاویری از داخل بدن استفاده میکنند. لوسمی معمولاً تومور ایجاد نمیکند، بنابراین آزمایشهای تصویر برداری به اندازه سایر انواع سرطان مفید نیستند. در صورتی که تصور شود سرطان فراتر از مغز استخوان و خون گسترش یافته است، آزمایشات تصویر برداری ممکن است در افراد مبتلا به ALL انجام شود تا به تعیین وسعت بیماری کمک کند. آنها همچنین ممکن است برای جستجوی عفونت یا سایر اختلالات نیز انجام شوند.
اشعه ایکس (X-rays)
اگر پزشک مشکوک به وجود عفونت ریه باشد، ممکن است عکس برداری با اشعه ایکس از قفسه سینه انجام شود. همچنین ممکن است عکس برداری برای جستجوی غدد لنفاوی بزرگ شده در قفسه سینه انجام شوند.
توموگرافی کامپیوتری (CT) اسکن
سی تی اسکن از اشعه ایکس برای ایجاد تصاویر دقیق و مقطعی از بدن شما استفاده میکند.
این آزمایش میتواند نشان دهد که آیا غدد لنفاوی یا اندامهای بدن شما بزرگ شده اند یا خیر. این تست معمولاً برای تشخیص ALL لازم نیست اما اگر پزشک مشکوک باشد که سلولهای سرطانی خون در اندامی مانند طحال شما رشد میکنند، ممکن است این کار نیز انجام شود.
گاهی اوقات نیز آزمایشی که سی تی اسکن را با اسکن PET (توموگرافی گسیل پوزیترون) ترکیب میکند (PET/CT scan) انجام میشود. این آزمایش اغلب برای بیماران مبتلا به ALL مورد نیاز نیست.
اسکن تصویر برداری رزونانس مغناطیسی (MRI)
اسکن MRI با استفاده از امواج رادیویی و آهنرباهای قوی به جای اشعه ایکس، تصاویر دقیقی از بدن میسازد. آنها در بررسی کردن به مغز و نخاع بسیار مفید هستند. این آزمایش ممکن است در صورتی انجام شود که سوراخ کمری سلولهای لوسمی را در CSF پیدا کند، یا اگر فردی علائمی داشته باشد که میتواند به این معنی باشد که ALL به ناحیه اطراف مغز گسترش یافته است.
سونوگرافی (Ultrasound)
از سونوگرافی میتوان برای مشاهده غدد لنفاوی نزدیک سطح بدن یا جستجوی اندامهای متورم شده داخل شکم مانند کلیهها، کبد و طحال استفاده کرد. در صورت نیاز میتوان از آن برای مشاهده بیضهها نیز استفاده کرد. انجام این آزمایش آسان است و از تشعشع استفاده نمیکند.
رسیدگیهای درمانی
به طور کلی، درمان لوسمی لنفوسیتی حاد به مراحل جداگانه تقسیم میشود:
- درمان القایی (Induction therapy): هدف از مرحله اول درمان، از بین بردن بیشتر سلولهای سرطانی خون در خون و مغز استخوان و بازگرداندن تولید طبیعی سلولهای خونی است.
- درمان تحکیمی (consolidation therapy): این مرحله از درمان که درمان پس از بهبودی (post-remission therapy) نیز نامیده میشود، با هدف از بین بردن لوسمی باقی مانده در بدن است.
- درمان نگهدارنده (Maintenance therapy): مرحله سوم درمان از رشد مجدد سلولهای سرطانی خون جلوگیری میکند. درمانهای مورد استفاده در این مرحله معمولاً با دوزهای بسیار پایینتر در مدت زمان طولانی و اغلب در طول سالها تجویز میشوند.
- درمان پیشگیرانه برای نخاع (Preventive treatment to the spinal cord): در طول هر مرحله از درمان، افراد مبتلا به لوسمی لنفوسیتی حاد ممکن است درمان اضافی برای از بین بردن سلولهای لوسمی واقع در سیستم عصبی مرکزی دریافت کنند. در این نوع درمان، داروهای شیمی درمانی اغلب مستقیماً به مایعی که نخاع را در بر میگیرد، تزریق میشود.
بسته به وضعیت شما، مراحل درمان لوسمی لنفوسیتی حاد میتواند دو تا سه سال طول بکشد.
روند درمانی ممکن است شامل موارد زیر باشد:
- شیمی درمانی (Chemotherapy): شیمی درمانی که از داروها برای کشتن سلولهای سرطانی استفاده میکند، معمولاً به عنوان یک درمان القایی برای کودکان و بزرگسالان مبتلا به لوسمی لنفوسیتی حاد استفاده میشود. از داروهای شیمی درمانی نیز میتوان در مراحل تثبیت و نگهداری استفاده کرد.
- درمان هدفمند (Targeted therapy): درمانهای دارویی هدفمند بر روی ناهنجاریهای خاص موجود در سلولهای سرطانی تمرکز دارند. با مسدود کردن این ناهنجاریها، درمانهای دارویی هدفمند میتوانند باعث مرگ سلولهای سرطانی شوند.
سلولهای لوسمی شما آزمایش میشوند تا بررسی شود آیا درمان هدفمند ممکن است برای شما مفید باشد یا خیر. درمان هدفمند را میتوان به تنهایی یا در ترکیب با شیمی درمانی برای درمان القایی، درمان تحکیمی یا درمان نگهدارنده استفاده کرد.
- پرتو درمانی (Radiation therapy): پرتو درمانی از پرتوهای پرقدرت مانند اشعه ایکس یا پروتونها برای از بین بردن سلولهای سرطانی استفاده میکند. اگر سلولهای سرطانی به سیستم عصبی مرکزی گسترش یافته باشند، پزشک ممکن است پرتو درمانی را توصیه کند.
- پیوند مغز استخوان (Bone marrow transplant): پیوند مغز استخوان که به عنوان پیوند سلولهای بنیادی (stem cell transplant) نیز شناخته میشود، ممکن است به عنوان درمان تثبیت کننده یا در صورت وقوع برای درمان سرطانی که مجددا عود کرده است، استفاده شود. این روش به افراد مبتلا به لوسمی اجازه میدهد تا مغز استخوان سالم را با جایگزین کردن مغز استخوان لوسمیک با مغز استخوان بدون لوسمی یک فرد سالم، بازسازی کند.
پیوند مغز استخوان با دوزهای بالای شیمی درمانی یا پرتو درمانی برای از بین بردن هر نوع مغز استخوان مولد لوسمی آغاز میشود. سپس مغز استخوان از یک اهدا کننده سازگار با فرد بیمار (پیوند آلوژنیک یا allogeneic transplant) جایگزین میشود.
- مهندسی سلولهای ایمنی برای مبارزه با سرطان خون: یک درمان تخصصی به نام گیرنده آنتی ژن کایمریک (CAR) – سلول T (himeric antigen receptor (CAR)-T cell therapy)، سلولهای T بدن شما را که با میکروبها مبارزه میکنند، مهندسی میکند تا با سرطان مبارزه کنند و دوباره آنها را به بدن شما تزریق میکند.
سلول درمانی CAR-T ممکن است یک گزینه برای کودکان و بزرگسالان جوان باشد. ممکن است برای درمان تحکیمی یا برای درمان سرطان عود کرده استفاده شود.
- آزمایشات بالینی: آزمایشهای بالینی روشهایی برای آزمایش کردن درمانهای جدید سرطان یا بررسی روشهای جدید استفاده از درمانهای موجود قبلی هستند. در حالی که آزمایشهای بالینی به شما یا فرزندتان فرصتی میدهد تا آخرین درمان سرطان را امتحان کنید، ممکن است مزایا و خطرات درمانی نامشخص باشد. در مورد مزایا و خطرات آزمایشات بالینی با پزشک خود صحبت کنید.
روندهای درمانی برای افراد مسن
افراد مسن، مانند افراد بزرگ تر از 65 سال، معمولاً عوارض ناشی از درمان بیشتری را تجربه میکنند. بزرگسالان مسن تر به طور کلی وضعیت بدتری نسبت به کودکانی دارند که برای لوسمی لنفوسیتی حاد درمان میشوند.
گزینههای پیش روی خود را با پزشکتان در میان بگذارید. بر اساس سلامت کلی و اهداف و ترجیحات شما، ممکن است تصمیم بگیرید که برای سرطان خون خود تحت کدام روند درمانی قرار بگیرید.
برخی از افراد ممکن است تصمیم بگیرند که از درمان سرطان چشم پوشی کنند و در عوض روی رسیدگیهای درمانی تمرکز کنند که علائم آنها را بهبود میبخشد و به آنها کمک میکند تا از زمان و عمر باقی مانده خود بهترین استفاده را ببرند.
مطالعه صدها مطلب علمی در حوزه بیولوژی
آرشیو جدیدترین خبرهای روز دنیای بیولوژی
مترجم: فاطمه فریادرس