اطلاعات عمومی، ویکی ژن
ایمونولیپوزوم تراپی چیست؟
مقدمهای بر ایمونولیپوزوم تراپی
لیپوزومها وزیکولهای کروی شکلی هستند که از دولایه فسفولیپیدی تشکیل شدهاند و میتوانند برای کپسوله کردن و تحویل انواع داروها استفاده شوند. آنها با قطع مصنوعی یک غشای فسفولیپیدی ایجاد شده و باعث میشوند که یک شکل کروی برای حفظ فعل و انفعالات آبدوست ایجاد شود.
لیپوزومها میتوانند مولکولهایی را در داخل خود حمل کنند که آبگریز یا آبدوست هستند، زیرا به ترتیب با لایههای دوتایی تعامل میکنند یا در هسته باقی میمانند. ایمونولیپوزومها زمانی تشکیل میشوند که آنتی بادیها یا قطعات آنتی بادی به سطح لیپوزومها کونژوگه میشوند تا امکان تحویل هدفمند محتوای لیپوزوم را فراهم کنند.
به این ترتیب، آنتیبادیهایی که اختصاصی بودن به گیرندههای سطحی منحصر به فرد سرطان را نشان میدهند، میتوانند برای تحویل داروهای شیمیدرمانی بهگونهای استفاده شوند که سمیت ناشی از درمانهای شیمیدرمانی داخل وریدی را محدود کند.
ایمونولیپوزومها
تحویل داروی لیپوزومی قبلاً به اندازه لیپوزوم متکی بود. لیپوزومهای کوچکتر به دلیل نفوذپذیری اضافی عروق اطراف بافتهای آسیبدیده و ملتهب احتمال بیشتری برای رسیدن به بافت مورد نظر داشتند. این هدفگیری محدود به این معنی بود که داروها اغلب از لیپوزومها در بافتهای دیگر آزاد میشدند و باعث ایجاد سمیت سیستمیک مشابه با درمان سنتی شیمیدرمانی داخل وریدی برای بیماران سرطانی میشد.
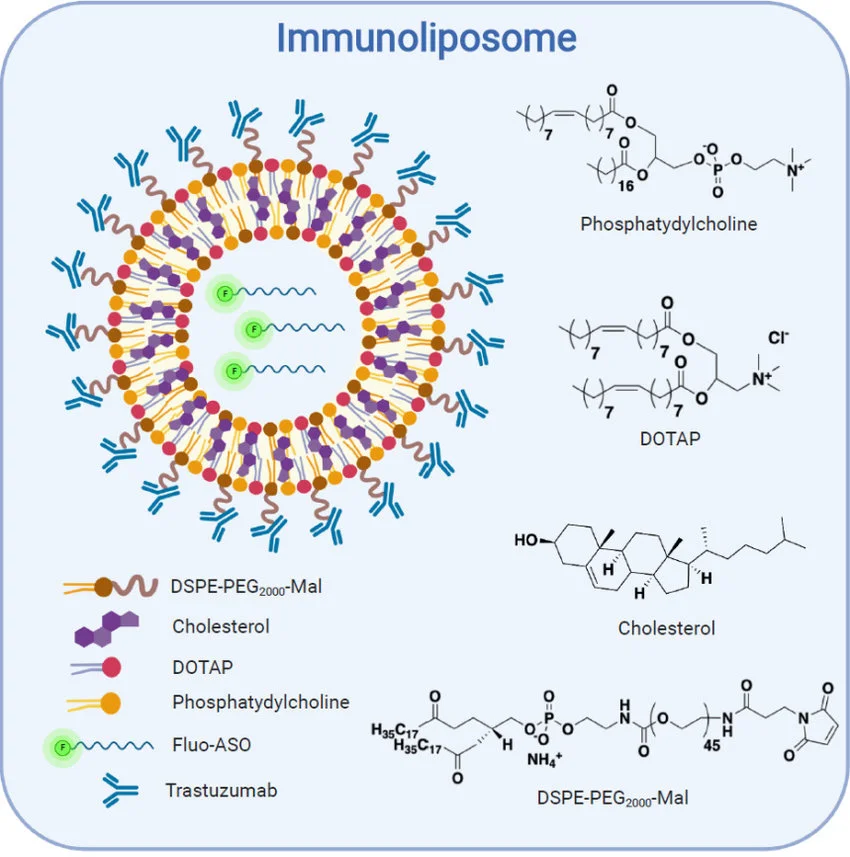
برای افزایش پایداری لیپوزومها و افزایش نیمه عمر آنها در جریان خون، پلیمری به نام پلی اتیلن گلیکول (PEG) اضافه میشود. این لیپوزومها به عنوان لیپوزومهای پگیله شناخته میشوند و کمتر در معرض اپسونیزاسیون و در نتیجه فاگوسیتوز هستند.
در حالی که پگیلاسیون احتمال رسیدن لیپوزومها به بافت بیمار را افزایش میدهد، ویژگی آنها را افزایش نمیدهد و هنوز هم احتمال زیادی برای انتشار داروی غیر اختصاصی وجود دارد. یک راه حل برای این موضوع افزودن پادتنها یا قطعات آنتی بادی است که ایمونولیپوزومهای اختصاصی آنتی ژن ایجاد میکند.
آنتیبادیها قبلاً به ساختار دولایه لیپوزومها کونژوگه شدهاند. با این حال، افزودن PEG اطراف ساختار، در دسترس بودن آنتیبادی و بنابراین ظرفیت اتصال را محدود میکند. برای کاهش این مشکل، آنتیبادیها و قطعات آنتیبادی را میتوان به انتهای خارجی زنجیرههای PEG کونژوگه کرد و از قرار گرفتن آنها برای اتصال اطمینان حاصل کرد.
آنتی بادیها و قطعات مورد استفاده در توسعه ایمونولیپوزوم مخصوص آنتی ژنهای سطحی هستند که توسط انواع خاصی از سلولها ارائه میشوند و به ایمونولیپوزوم اجازه میدهند مستقیماً با سلولهای هدف ترکیب شده و محتویات دارویی آنها را به روشی کنترل شده آزاد کنند.
رهاسازی دارو در داخل رخ میدهد. این امر به دلیل عملکرد اندوسیتی طبیعی سلولها به دنبال اتصال گیرنده است. ایمونولیپوزوم و محتویات آن در یک وزیکول به نام اندوزوم به داخل سلول آورده میشود، جایی که دولایه لیپوزوم هضم شده و محتویات آن در سیتوزول آزاد میگردد.
هدف گیری آنتی ژن به دلیل تفاوت در سطوح بیان آنتی ژنهای خاص بر روی سلولهای بافتهای بیمار، امکان تحویل داروهای خاص هر بیماری را میدهد. در بیماریهای التهابی، سلولهای اندوتلیال مولکولهای چسبنده مختلفی مانند سلکتینها و اینتگرینها را برای کمک به فرآیند اکستراوازاسیون ارائه میکنند.
این مولکولهای چسبنده، از جمله مولکول چسبنده بین سلولی 1 (ICAM-1) میتوانند توسط آنتی بادیهای خاص مورد هدف قرار گیرند و به درمان بیماریهایی مانند آرتریت روماتوئید کمک کنند. این هدفگیری منجر به انتشار موضعی دارو با سمیت کم به دلیل بیان بیش از حد ICAM-1 در محلهای آرتریت و سطوح پایین بیان آن در بافت سالم میشود.
استفاده از ایمونولیپوزومها در درمان سرطان
در حالی که برای توسعه درمان بیماریهای التهابی مهم هستند، ایمونولیپوزومها همچنین یک بخش امیدوارکننده از تحقیقات در درمان سرطان هستند. سلولهای سرطانی به دلیل جهشهای ژنتیکی که دارند، غالباً یا آنتیژنهای جدید، معروف به نئوآنتیژنها، یا مقادیری از آنتیژنهای سطحی نرمال را بیان میکنند. این بدان معنی است که این آنتی ژنها میتوانند برای هدف قرار دادن سلولهای سرطانی با ویژگی بالا مورد استفاده قرار گیرند.
یکی از نمونههای پروتئینی که بیش از حد در سرطان سینه بیان میشود، گیرنده ۲ فاکتور رشد اپیدرمی انسانی (HER2) است. این پروتئینی است که در حدود 20 درصد موارد سرطان سینه بیش از حد بیان میشود و آن را به یک هدف مناسب برای تحقیقات درمانی تبدیل میکند.
یک نسخه انسانی از یک آنتی بادی مونوکلونال موش، معروف به rhuMAb HER2 یا trastuzumab، ساخته شده است که میتواند به طور خاص دامنه خارج سلولی HER2 را هدف قرار دهد. قطعاتی از این آنتی بادی ضد HER2 که به یک لیپوزوم کونژوگه شده است توانستهاند به طور انتخابی به سلولهای سرطانی پستان متصل شوند و دوکسوروبیسین محصور شده ایمونولیپوزوم (یک داروی رایج شیمی درمانی) را بدون سمیت به سلولهای غیر جهش یافته تحویل دهند.
استفاده از ایمونولیپوزومها، در این مورد، بسیار مفید است، زیرا دوکسوروبیسین بسیار سیتوتوکسیک است و در صورت استفاده داخل وریدی منجر به عوارض جانبی مانند ریزش مو، حالت تهوع و ایجاد سمیت در قلب میشود.
HER2 تنها یک هدف بالقوه برای هدف گیری ایمونولیپوزومی در درمان سرطان است. علاوه بر این، کارآزماییهای بالینی در حال مطالعه اثر هدف قرار دادن گیرنده فاکتور رشد اپیدرمی (EGFR) در سرطان سینه، گلیوما و سرطان کولورکتال هستند و دوباره از دوکسوروبیسین به عنوان داروی محصور شده استفاده میکنند. قطعه اتصال دهنده آنتی ژن (Fab) یک آنتی بادی به نام Cetuximab برای رساندن داروهای ایمونولیپوزومی با موفقیت به سلولهای سرطان روده بزرگ استفاده شده است.

پتانسیل برای درمانهای ایمونولیپوزوم در آینده
درمان ایمونولیپوزوم برای سرطان در حال حاضر بسیار گسترده نیست. این امر بیشتر به دلیل هزینه توسعه درمان میباشد. با این حال، به دلیل ارتباط قابل توجهی که بین سطوح بیان بیش از حد آنتی ژن و هدفگیری موفق دارو در بافتهای سرطانی نشان داده شده است، تحویل داروی ایمونولیپوزوم ممکن است به بخش رایجتری از درمانهای شخصی سرطان تبدیل شود.
به طور کلی، داروهای فردمحور سرطان به دلیل عواملی مانند طول درمان، کاهش سرطانهای عودکننده و کاهش بروز و شدت عوارض جانبی، مقرون به صرفهتر است. این به این دلیل است که درمانهای فردمحور بر جهشهای ژنتیکی و بیان پروتئینهای مرتبط با سرطان در نمونهبرداری از تومورها تمرکز میکنند و به درمانها امکان میدهند ترجیحاً بر اساس اثربخشی پیشبینیشده انتخاب شوند.
همچنین زمینهای برای استفاده از بسیاری از آنتی بادیهای دیگر برای هدف گیری ایمونولیپوزوم وجود دارد؛ مانند آنتی بادیهایی که در ایمونوتراپی سرطان استفاده میشوند و انواع و شدت سرطانهایی را که میتوان به این روش درمان کرد، گسترش میدهد.
همچنین بخوانید:
- ایمونوفنوتایپینگ در فلوسایتومتری
- ایمونوسیتوفلورسنت و آشنایی با فلوسایتومتری
- روش های ایمونولوژی و سرولوژی در آزمایشگاه تشخیص طبی
- کاربرد های ایمونوانفورماتیک
- ایمونوپرسیپیتاسیون (Immunoprecipitation)
مترجم: شقایق مرتاضی