تکنیک ها
تست کلیگر آیرون آگار (تست KIA): اساس، محیط کشت، روش، نتایج، موارد استفاده
هدف تست KIA
تمایز باسیلهای گرم منفی رودهای بر اساس تولید سولفید هیدروژن و تخمیر دکستروز و لاکتوز.
اساس تست KIA
تست کلیگلر آیرون آگار (تست KIA) به جهت ایجاد تمایز بین اعضای خاصی از انتروباکتریاسه با نشان دادن تولید سولفید هیدروژن و تخمیر دکستروز و لاکتوز استفاده میشود. کلیگلر آگار مورد استفاده برای آزمایش، شامل کازئین و پپتونهای گوشتی (میت پپتونها) است که ترکیبات نیتروژندار و اسیدهای آمینه، ویتامینهای لازم برای رشد باکتریها را تأمین میکند.
این محیط شامل دو منبع کربوهیدرات، دکستروز و لاکتوز است و همچنین حاوی فنل قرمز به عنوان شاخصی برای تخمیر کربوهیدرات است. استفاده از دو قند میتواند به تمایز ارگانیسمها تنها بر اساس تخمیر دکستروز از آنهایی که لاکتوز را نیز تخمیر میکنند، کمک میکند. اما غلظت دکستروز در محیط یکدهم غلظت لاکتوز است.
تخمیر کنندههای غیر لاکتوز در ابتدا در نتیجه تخمیر دکستروز در قسمت سطح شیبدار (slant) و عمق (butt) باعث ایجاد رنگ زرد میشوند. غلظت دکستروز تنها یک درصد است و بنابراین به سرعت از بین میرود. هنگامی که دکستروز محیط تخلیه میشود، واکنش به شرایط قلیایی باز میگردد که به دلیل اکسیداسیون اسیدها، بخش سطحی به رنگ قرمز در میآید. اما در بخش عمقی محیط تغییر رنگی رخ نمیدهد و محیط اسیدی (به رنگ زرد) باقی میماند.
ارگانیسمهای تخمیر لاکتوز، در سطح و عمق، باعث ایجاد رنگ زرد در سطح و عمق میشوند. در قسمت سطح هیچ بازگشتی به رنگ قرمز وجود نخواهد داشت؛ زیرا اسید کافی برای حفظ pH اسیدی در شرایط هوازی تولید میشود. غیر تخمیر کنندهها سطح و عمق قرمز رنگ ایجاد میکنند. تولید H2S منجر به سیاه شدن محیط میشود که این امر هم در سراسر عمق و هم در تشکیل حلقه سیاه در نزدیکی عمق مشهود است. تولید گاز به وسیله وجود حباب یا ترک در محیط نشان داده میشود.
محیط کشت استفاده شده
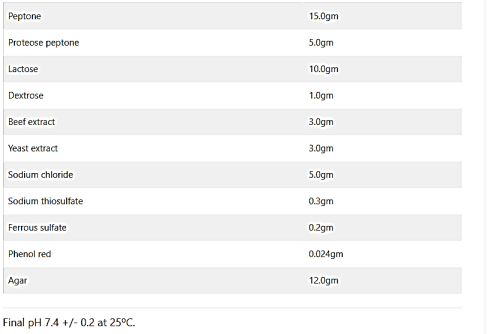
کلیگر آیرون آگار
مراحل تست KIA
- با یک سوزن تلقیح مستقیم،KIA را با ضربه توسط نیدل از مرکز محیط به سمت عمق لوله و سپس بیرون کشیدن سریع سوزن از سطح، تلقیح کنید.
- لولهها را در شرایط هوازی با درپوش شل در دمای ۳۷-۳۵ درجه سانتیگراد به مدت ۲۴-۱۸ ساعت انکوبه کنید و واکنش محیط را بررسی کنید.
نتایج تست کلیگر آیرون آگار

تخمیر کربوهیدرات
برای سطح شیب دار و عمق
- تست مثبت: زرد (اسیدی)
- تست منفی: قرمز (قلیایی)
برای بخش عمقی
- تست مثبت: زرد
- تست منفی: قرمز
- سطح قرمز/ عمق زرد: دکستروز مثبت، لاکتوز منفی
- سطح زرد/ عمق زرد: دکستروز مثبت، لاکتوز مثبت
- سطح قرمز/ عمق قرمز: دکستروز منفی، لاکتوز منفی
تولید H2S
- تست مثبت: رسوب یا رنگ سیاه در سرتاسر محیط یا در محل اتصال سطح به عمق
- تست منفی: عدم گسترش رنگ سیاه
تولید گاز
- تست مثبت: وجود حباب یا ترک در محیط
- تست منفی: عدم وجود حباب یا ترک در محیط
محدودیتهای تست کلیگر آیرون آگار
- این محیط حاوی هیچ بازدارنده یا مهارکنندهای نیست، بنابراین انواع بسیاری از ارگانیسمهای مختلف ممکن است در آن رشد کنند.
- نتیجه را در بازه زمانی ۱۸-۲۴ ساعت بخوانید و تفسیر کنید. بررسی آن در کمتر از ۱۸ ساعت ممکن است منجر به تفسیر اشتباه شود؛ زیرا کربوهیدرات تخمیر شده ممکن است اسید کافی برای تغییر شناساگر فنل رد تولید نکرده باشد. همچنین واکنشی که بیش از بازه زمانی ۲۴ ساعته خوانده شود ممکن است به دلیل استفاده از پپتون که منجر به قلیایی شدن pH محیط میشود، اشتباه تفسیر شود.
- تولید H2S در عمق ممکن است اسیدیته تولید شده را بپوشاند.
- شاخص شناساگر H2S موجود در KIA چندان حساس نیست و بنابراین برخی از باسیلهای گرم منفی H2S مثبت، ممکن است H2S در KIA تولید نکنند.
- در طول انکوباسیون، لولهها باید به طور شل بسته شوند، زیرا در لولههای با درپوش محکم، واکنش اسیدی که صرفاً توسط تخمیر دکستروز ایجاد میشود، قسمت سطح شیب دار را نیز درگیر میکند.
کنترل کیفیت تست KIA
اشریشیا کلی ATCC 25922 ، سطح زرد/ عمق زرد، H2S (-)، گاز (+)
سودوموناس آئروژینوزا ATCC 27853 ، سطح قرمز /عمق قرمز، H2S (-) ، گاز(-)
سالمونلا انتریکا سرووار تیفی موریوم ATCC 14028، سطح قرمز / عمق زرد، H2S (+)، گاز (+)
مطالعه بیشتر:
آگار ستریماید (Cetrimide Agar): ترکیب، اساس، کاربردها، آماده سازی و مورفولوژی کلنی
مترجم: مریم محجوب




