مقدمهای بر تومورهای استرومال دستگاه گوارش
سرطان زمانی شروع میشود که سلولهای بدن شروع به رشد خارج از کنترل میکنند. سلولها تقریباً در هر قسمت از بدن میتوانند به سرطان تبدیل شوند و سپس به سایر قسمتهای بدن گسترش یابند.
تومورهای استرومال دستگاه گوارش (GISTs) سرطانهای غیر معمولی هستند که در سلولهای خاصی در دیواره دستگاه گوارش (GI) که به نام دستگاه گوارش نیز شناخته میشود، شروع میشوند. برای درک GISTها، دانستن هر چیزی در مورد ساختار و عملکرد دستگاه گوارش به شما کمک میکند.
نحوه عملکرد دستگاه گوارش (gastrointestinal tract یا GI)
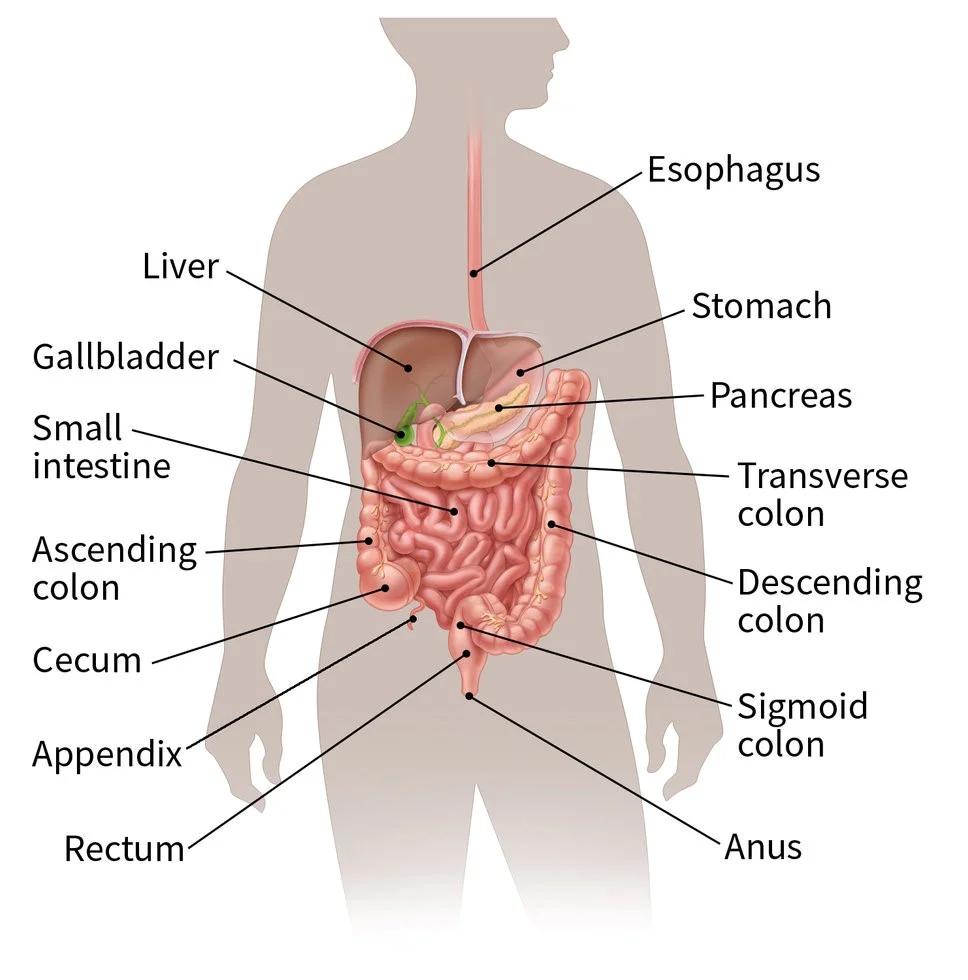
دستگاه گوارش غذا را برای دریافت انرژی پردازش کرده و بدن را از شر مواد زائد جامد خلاص میکند. پس از جویدن و بلعیده شدن، غذا از مری عبور میکند. مری درست در زیر دیافراگم (نوار نازک ماهیچه ای زیر ریهها) به معده میپیوندد.
معده (stomach) عضوی کیسه مانند است که با مخلوط کردن غذا با شیره معده به فرآیند گوارش کمک میکند. سپس غذا و شیره معده در روده کوچک تخلیه میشود. روده کوچک که حدود 6 متر طول دارد، به تجزیه غذا ادامه میدهد و بیشتر مواد مغذی را وارد جریان خون میکند.
روده کوچک (small intestine) به روده بزرگ (large intestine) میپیوندد که اولین قسمت آن کولون است، لوله ای عضلانی به طول حدود 1.5 متر. روده بزرگ آب و مواد مغذی معدنی را از مواد غذایی باقی مانده جذب میکند. مواد زائد باقی مانده پس از این فرآیند (مدفوع) به رکتوم (rectum) میرود و در آن جا ذخیره میشود تا از طریق مقعد از بدن خارج شود.
تومورهای استرومال دستگاه گوارش
تومورهای استرومال گوارشی (Gastrointestinal stromal tumors یا GISTs) در اشکال بسیار اولیه سلولهای ویژه در دیواره دستگاه گوارش به نام سلولهای بینابینی کژال (ICCs یا interstitial cells of Cajal) شروع میشوند. ICCها گاهی اوقات “ضربان ساز یا pacemakers” دستگاه گوارش نامیده میشوند زیرا آنها به ماهیچههای دستگاه گوارش سیگنال میدهند تا برای حرکت دادن غذا و مایعات منقبض شوند.
بیش از نیمی از GIST ها از معده شروع میشود. بسیاری از موارد دیگر از روده کوچک شروع میشوند اما GISTها میتوانند در هر نقطه از دستگاه گوارش شروع شوند. تعداد کمی از GIST در خارج از دستگاه گوارش در نواحی مجاور مانند امنتوم (omentum، لایه پیش بند مانندی از بافت چربی که بر روی اندامهای شکم آویزان است) یا صفاق (peritoneum، پوشش نازک روی اندامها و دیوارههای داخل شکم) شروع میشوند.
به نظر میرسد برخی از GISTها بسیار بیشتر از سایرین در نواحی دیگر رشد کرده یا به سایر قسمتهای بدن گسترش مییابند. پزشکان به عوامل خاصی برای کمک به تشخیص احتمال رشد و گسترش سریع GIST نگاه میکنند، مانند:
- اندازه تومور
- جایی که در دستگاه گوارش قرار دارد
- سلولهای تومور با چه سرعتی تقسیم میشوند (سرعت میتوزی آنها که در مبحث تستهای تومورهای استرومال گوارشی توضیح داده شده است)
- سایر سرطانهای دستگاه گوارش
GISTها مشابه سایر انواع سرطانهای شایع تر دستگاه گوارش که از انواع دیگر سلولها ایجاد میشوند، نیستند.
سرطانها میتوانند در هر جایی از دستگاه گوارش – از مری تا مقعد – رخ دهند. بیشتر سرطانهایی که از دستگاه گوارش شروع میشوند، از جمله بیشتر سرطانهای مری، سرطان معده و سرطان روده بزرگ و راست روده، از سلولهای غده ای شروع میشوند که تقریباً تمام دستگاه گوارش را پوشانده اند. سرطانهایی که در این سلولها ایجاد میشوند، آدنوکارسینوم (adenocarcinomas) نامیده میشوند.
سرطانها همچنین میتوانند از سلولهای سنگفرشی شروع شوند که سلولهای مسطحی هستند که برخی از قسمتهای دستگاه گوارش مانند قسمت بالایی مری و انتهای مقعد را پوشانده اند. سرطانهایی که از این سلولها شروع میشوند، کارسینوم سلول سنگفرشی (squamous cell carcinomas) نامیده میشوند.
دستگاه گوارش همچنین دارای سلولهای عصبی غدد درون ریز است. این سلولها دارای برخی ویژگیهای مشترک با سلولهای عصبی هستند اما ویژگیهای مشترک دیگری نیز با سلولهای تولید کننده هورمون (غدد درون ریز) دارند. سرطانهایی که از این سلولها ایجاد میشوند، تومورهای عصبی غدد درون ریز (neuroendocrine tumors یا NETs) نامیده میشوند. این سرطانها در دستگاه گوارش نادر هستند. تومورهای کارسینوئید نمونه ای از تومورهای عصبی غدد درون ریز هستند که در دستگاه گوارش یافت میشوند.
سایر انواع نادر سرطان در دستگاه گوارش شامل انواع مختلف سارکوم بافت نرم (soft tissue sarcomas) است، مانند:
- لیومیوسارکوم (Leiomyosarcomas): سرطان سلولهای ماهیچه صاف
- آنژیوسارکوم (Angiosarcomas): سرطان سلولهای عروق خونی
- تومورهای بدخیم غلاف عصبی محیطی (MPNSTs یا Malignant peripheral nerve sheath tumors): سرطان سلولهایی که از اعصاب حمایت و محافظت میکنند.
GIST با سایر انواع سرطانهای دستگاه گوارش متفاوت است. آنها در انواع مختلف سلولها شروع میشوند، به انواع مختلف روشهای درمانی نیاز دارند و پیش آگهی (وضعیت آتی) متفاوتی دارند. به همین دلیل است که پزشکان باید دریابند که آیا فرد مبتلا به تومور در دستگاه گوارش دارای GIST، دارای نوع دیگری از سرطان یا شرایط غیر سرطانی دیگری نیز است.
آمار کلیدی برای تومورهای استرومال دستگاه گوارش
تومورهای استرومال دستگاه گوارش (GISTs) شایع نیستند و تعداد دقیق افرادی که هر ساله با این تومورها تشخیص داده میشوند مشخص نیست. تا اواخر دهه 1990، اطلاعات زیادی در مورد این تومورها وجود نداشت (و پزشکان راههای خوبی برای شناسایی آنها با آزمایشات آزمایشگاهی نداشتند)، بنابراین بسیاری از آنها در نهایت به عنوان انواع دیگر سرطانها طبقه بندی شدند.
برآوردهای فعلی برای تعداد کل موارد GIST که هر سال در ایالات متحده تشخیص داده میشوند، از حدود 4000 تا حدود 6000 متغیر است.
این تومورها میتوانند در هر جایی از دستگاه گوارش شروع شوند اما اغلب در معده (حدود 60 درصد) یا روده کوچک (حدود 35 درصد) رخ میدهند. سایر موارد بیشتر در مری، کولون و رکتوم یافت میشوند. تعداد کمی نیز در شکم خارج از دستگاه گوارش ایجاد میشود.
GISTs بیشتر در افراد بالای 50 سال یافت میشود. این تومورها در افراد جوان تر از 40 سال نادر هستند اما میتوانند در افراد با هر سنی ایجاد شوند.
علائم و نشانههای تومورهای استرومال دستگاه گوارش
بیشتر تومورهای استرومال دستگاه گوارش (GIST) در دیواره معده یا روده کوچک ایجاد میشوند. این تومورها اغلب در فضای خالی داخل دستگاه گوارش (GI) رشد میکنند، بنابراین ممکن است فوراً علائمی ایجاد نکنند، مگر اینکه در یک مکان خاص باشند یا به اندازه خاصی برسند.
تومورهای کوچک ممکن است هیچ علامتی ایجاد نکنند و زمانی که پزشک در حال بررسی مشکل دیگری است به طور تصادفی پیدا میشوند. این تومورهای کوچک اغلب به کندی رشد میکنند.
علائم مربوط به از دست دادن خون
- GISTها معمولا تومورهای شکننده ای هستند که میتوانند به راحتی خونریزی کنند. در واقع، آنها اغلب در مواردی یافت میشوند که باعث خونریزی در دستگاه گوارش میشوند. علائم و نشانههای این خونریزی به سرعت وقوع و محل قرارگیری تومور بستگی دارد.
- خونریزی شدید در مری یا معده ممکن است باعث شود فرد خون بالا بیاورد. هنگامی که خون به بالا پرتاب میشود، ممکن است تا حدی هضم شود، بنابراین ممکن است مانند تفاله قهوه به نظر برسد.
- خونریزی شدید در معده یا روده کوچک میتواند حرکات روده (مدفوع) را سیاه و قیری کند.
- خونریزی شدید در روده بزرگ احتمالاً مدفوع را با خون قابل مشاهده قرمز میکند.
- اگر خونریزی آهسته باشد، اغلب باعث نمیشود که فرد خون بالا بیاورد یا در مدفوع خود تغییری مشاهده کند. با گذشت زمان، خونریزی آهسته میتواند منجر به کاهش تعداد گلبولهای قرمز خون (کم خونی) شود که میتواند باعث احساس خستگی و ضعف در فرد شود.
- خونریزی از دستگاه گوارش میتواند بسیار جدی باشد. اگر هر یک از این علائم یا علائم را دارید، فورا به پزشک مراجعه کنید.
سایر علائم احتمالی GIST
سایر علائم GISTمیتواند شامل موارد زیر باشد:
- درد شکم (Abdominal)
- وجود توده یا تورم در شکم
- تهوع و استفراغ
- احساس سیری بعد از خوردن مقدار کمی غذا
- از دست دادن اشتها
- کاهش وزن
- مشکلات بلع (برای تومورهای مری)
برخی از تومورها به اندازه ای بزرگ میشوند که مانع عبور غذا از معده یا روده شوند. به این حالت انسداد (obstruction) میگویند و میتواند باعث درد شدید شکم و استفراغ شود.
از آن جا که GISTها اغلب شکننده هستند، گاهی اوقات ممکن است پاره شوند که میتواند منجر به ایجاد سوراخ (perforation) در دیواره دستگاه گوارش شود. این حالت همچنین میتواند منجر به درد شدید شکم شود. ممکن است در این مواقع نیاز به جراحی اورژانسی باشد.
اگرچه بسیاری از علائم احتمالی GISTs (مانند درد شکم و حالت تهوع) میتواند ناشی از چیزهایی غیر از سرطان باشد اما اگر این علائم را دارید، به خصوص اگر بیش از چند روز طول بکشد، مراجعه به پزشک ضروری است.
علت تومورهای استرومال دستگاه گوارش چیست؟
محققان دقیقاً نمیدانند چه چیزی باعث بروز بیشتر تومورهای استرومال دستگاه گوارش (GIST) میشود. اما پیشرفتهای زیادی در یادگیری این که چگونه تغییرات خاصی در DNAمیتواند باعث تبدیل سلولهای طبیعی به سلولهای سرطانی شود، حاصل شده است.
DNA ماده شیمیایی موجود در سلولهای ما است که ژنهای ما را میسازد که عملکرد سلولهای ما را کنترل میکند. ما معمولا شبیه والدین خود هستیم زیرا آنها منبع DNA ما هستند. اما DNA چیزی بیش از ظاهر ما را تحت تأثیر قرار میدهد.
برخی از ژنها زمان رشد و تقسیم سلولها به سلولهای جدید را کنترل میکنند:
- ژنهای خاصی که به رشد، تقسیم و زنده ماندن سلولها کمک میکنند، انکوژن (oncogene) نامیده میشوند.
- ژنهایی که به طور معمول رشد سلولی را تحت کنترل نگه میدارند، اشتباهات DNA را ترمیم میکنند یا باعث میشوند سلولها در زمان مناسب بمیرند، ژنهای سرکوبگر تومور (tumor suppressor genes) نامیده میشوند.
- سرطانها میتوانند ناشی از تغییرات DNA باشند که انکوژنها را روشن نگه میدارد یا ژنهای سرکوب کننده تومور را خاموش میکند. این نوع تغییرات ژنی میتواند منجر به رشد خارج از کنترل سلولها شود.
تغییرات ژنی که میتواند منجر به GIST شود
تغییرات ژنی که منجر به بروز اکثر GIST میشوند اکنون درک شده اند اما هنوز مشخص نیست که چرا این تغییرات رخ میدهند. هیچ عامل خطرزای محیطی یا مرتبط با سبک زندگی برای GIST وجود ندارد. برخی از تغییرات ژنی که منجر به GIST میشوند ممکن است دلایلی داشته باشند که هنوز پیدا نشده اند اما بسیاری از این تغییرات ممکن است فقط رویدادهای تصادفی باشند که گاهی در داخل سلولها اتفاق میافتند و متأسفانه منجر به سرطان میشوند.
تعداد کمی از خانوادهها دارای GIST هستند که ناشی از یک جهش ژنی است که از والدین به فرزند منتقل میشود. (به مبحث فاکتورهای خطرزای تومور استرومال گوارشی مراجعه کنید.) اما بیشتر جهشهای ژنی مربوط به GIST ها ارثی نیستند. این تغییرات بدون هیچ دلیل مشخصی رخ میدهد و اکتسابی (acquired) یا پراکنده (sporadic) نامیده میشود.
تغییرات در ژنهای KIT یا PDGFRA
در اکثر افراد مبتلا به GIST، سلولهای سرطانی تغییری در انکوژن KIT دارند. این ژن سلولها را به سمت ساخت پروتئین KIT (همچنین به عنوان CD117) هدایت میکند که باعث رشد و تقسیم سلولها میشود.
معمولاً ژن KIT در سلولهای بینابینی Cajal (ICCs) غیر فعال است که سلولهای دیوارههای دستگاه گوارش هستند که GIST از آنها رشد میکنند. ژن KIT تنها در صورتی فعال است که نیاز به ICCهای بیشتری وجود داشته باشد.
اما در بیشتر GIST ژن KIT جهش یافته است. همیشه فعال است، بنابراین سلولها همیشه در حال رشد و تقسیم هستند.
در حدود 5 تا 10 درصد از GISTها، سلولهای سرطانی دارای جهش در ژن PDGFRA هستند که باعث میشود سلولها بیش از حد پروتئین PDGFRA بسازند. این حالت همان اثر KIT را روی سلولها دارد.
اکثر GISTها تغییراتی در ژن KIT یا PDGFRA دارند، اما نه هر دو.
سایر تغییرات ژنی
تعداد کمی از GISTها، به ویژه آنهایی که در کودکان هستند، در هیچ یک از این ژنها تغییری ندارند. بسیاری از این تومورها تغییراتی در یکی از ژنهای SDH دارند. محققان هنوز در تلاشند تا مشخص کنند چه تغییرات ژنی دیگری میتواند منجر به این سرطانها شود.
از آن جایی که پزشکان در مورد تغییرات ژن و پروتئین در سلولهای GIST اطلاعات بیشتری کسب کرده اند، توانسته اند از این اطلاعات برای کمک به تشخیص و درمان این سرطانها استفاده کنند. (به مبحث درمان هدفمند برای تومورهای استرومال گوارشی مراجعه کنید.)
عوامل خطرزا تومور استرومال گوارشی
عامل خطرزا هر چیزی است که احتمال ابتلای فرد به بیماری مانند سرطان را افزایش دهد. سرطانهای مختلف عوامل خطرزا متفاوتی دارند. برخی از عوامل خطرزا مانند سیگار کشیدن را میتوان تغییر داد. موارد دیگر، مانند سن یا سابقه خانوادگی فرد، قابل تغییر نیستند.
اما داشتن یک عامل خطرزا یا حتی چندین عامل به این معنی نیست که فرد به این بیماری مبتلا میشود. بسیاری از افرادی که به این بیماری مبتلا میشوند ممکن است عوامل خطرزا شناخته شده کمی داشته باشند یا اصلا چنین عواملی را نداشته باشند.
در حال حاضر، عوامل خطرزا بسیار کمی برای تومورهای استرومال دستگاه گوارش (GISTs) وجود دارد.
سن بیشتر
این تومورها میتوانند در افراد با هر سنی ایجاد شوند اما در افراد کمتر از 40 سال نادر هستند و در افراد بالای 50 سال شایع ترند.
به ارث بردن برخی از سندرمهای ژنتیکی
بیشتر GISTها پراکنده هستند (ارثی نیستند) و هیچ علت مشخصی ندارند. اگرچه در موارد نادر، GIST در چندین عضو یک خانواده یافت شده است. این اعضای خانواده یک جهش (تغییر) ژنی را به ارث برده اند که میتواند منجر به GIST شود.
سندرم GIST خانوادگی اولیه (Primary familial GIST syndrome): این یک بیماری نادر و ارثی است که منجر به افزایش خطر ابتلا به GIST میشود. افراد مبتلا به این سندرم در سنین پایینتر از زمانی که این بیماری معمولاً رخ میدهد، به GIST مبتلا میشوند. همچنین احتمال بیشتری وجود دارد که بیش از یک GIST داشته باشند.
اغلب، این سندرم توسط یک ژن غیر طبیعی KIT ایجاد میشود که از والدین به فرزند منتقل میشود. این همان ژنی است که در اکثر GISTهای پراکنده جهش یافته (تغییر مییابد). (به مبحث چه چیزی باعث ایجاد تومورهای استرومال گوارشی میشود، مراجعه کنید) افرادی که این ژن غیر طبیعی را از والدین به ارث برده اند آن را در تمام سلولهای خود دارند، در حالی که افراد مبتلا به GIST پراکنده، فقط آن را در سلولهای سرطانی دارند.
در موارد کمتری، تغییر در ژن PDGFRA باعث این سندرم ژنتیکی میشود. (نقص در ژن PDGFRA نیز در درصد کمی از GISTهای پراکنده یافت میشود.)
گاهی اوقات افراد مبتلا به سندرم GIST خانوادگی دارای لکههای پوستی مانند لکههایی هستند که در بیماران مبتلا به نوروفیبروماتوز دیده میشود. قبل از اینکه آزمایشهایی برای ژنهای KIT و PDGFRA در دسترس قرار گیرد، برای برخی از این افراد به اشتباه تصور میشد که نوروفیبروماتوز دارند.
نوروفیبروماتوز نوع 1 (بیماری فون رکلینگهاوزن یا von Recklinghausen disease): این بیماری به دلیل نقص در ژن NF1 ایجاد میشود. این تغییر ژن ممکن است از والدین به ارث برسد اما در برخی موارد این تغییر قبل از تولد، بدون اینکه ارثی باشد، رخ میدهد.
افراد مبتلا به این سندرم اغلب دارای بسیاری از تومورهای عصبی خوش خیم (غیر سرطانی) هستند که نوروفیبروم (neurofibromas) نامیده میشوند که از جوانی شروع میشود. این تومورها در زیر پوست و در سایر قسمتهای بدن ایجاد میشوند. این افراد همچنین معمولاً دارای لکههای قهوهای یا برنزه روی پوست هستند (که به آن لکههای کافهآو لایت یا café au lait spots میگویند).
افراد مبتلا به NF1 در معرض خطر بیشتری برای GISTs (اغلب در روده کوچک) و همچنین برخی دیگر از انواع سرطان هستند.
سندرم کارنی استراتاکیس (Carney-Stratakis syndrome): افراد مبتلا به این بیماری ارثی نادر در معرض خطر افزایش GISTs (بیشتر در معده) و همچنین تومورهای عصبی به نام پاراگانگلیوما (paragangliomas) هستند. GIST اغلب زمانی ایجاد میشود که این افراد در سنین نوجوانی یا 20 سالگی خود هستند. همچنین احتمال بیشتری وجود دارد که بیش از یک GIST داشته باشند.
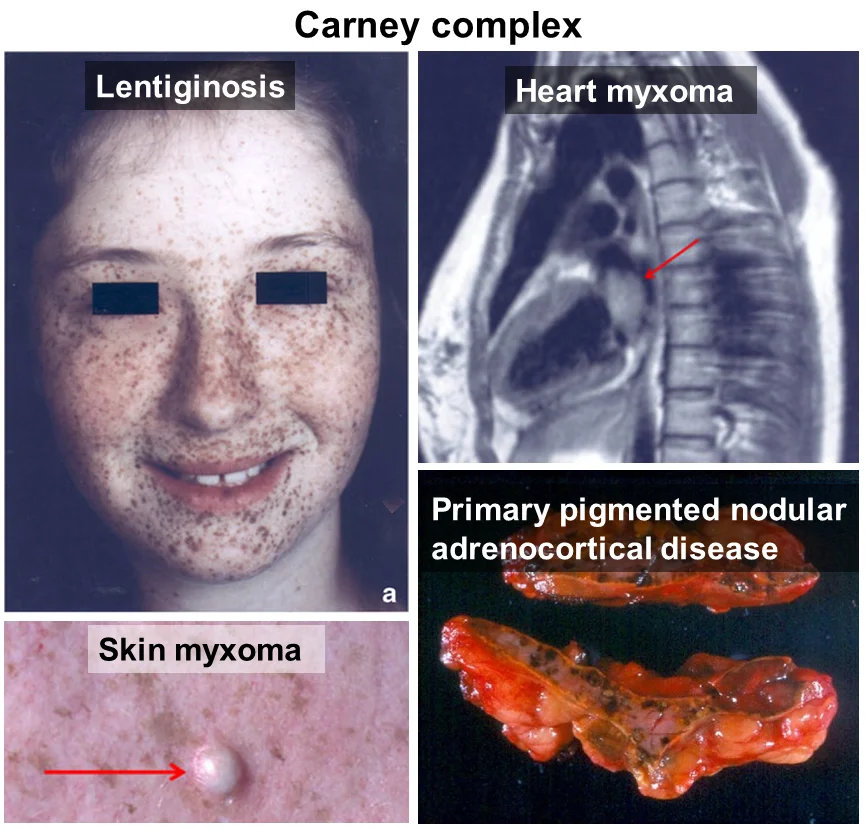
این سندرم به دلیل تغییر در یکی از ژنهای SDH (سوکسینات دهیدروژناز یا succinate dehydrogenase) ایجاد میشود که از والدین به فرزند منتقل میشود.
آیا میتوان تومورهای استرومال دستگاه گوارش را زود تشخیص داد؟
غربالگری، آزمایش بیماریهایی مانند سرطان در افرادی است که هیچ علامتی ندارند. آزمایشهای غربالگری میتوانند برخی از انواع سرطان را در مراحل اولیه پیدا کنند، زمانی که روند درمان به احتمال زیاد مؤثر است. اما در حال حاضر هیچ آزمایش غربالگری موثری برای تومورهای استرومال دستگاه گوارش (GISTs) وجود ندارد، بنابراین انجام آزمایشات معمول بر روی افراد بدون هیچ علامتی توصیه نمیشود.
بسیاری از GISTها به دلیل علائمی که فرد دارد پیدا میشوند اما برخی از GISTها ممکن است زودتر به طور تصادفی پیدا شوند. گاهی أوقات آنها در معاینه برای مشکل دیگری مانند در طول کولونوسکوپی برای جستجوی سرطان کولورکتال دیده میشوند. به ندرت، GIST ممکن است در آزمایش تصویر برداری، مانند اسکن توموگرافی کامپیوتری (computed tomography یا CT) که به دلیل دیگری انجام میشود، دیده شود. برخی از GIST نیز ممکن است به طور اتفاقی (غیر منتظره) در طی جراحی شکم برای مشکل دیگری پیدا شوند.
آزمایشات برای تومورهای استرومال دستگاه گوارش
تومورهای استرومال دستگاه گوارش (GISTs) اغلب به این دلیل یافت میشوند که فرد دارای علائم یا نشانههایی است.
برخی دیگر در طول امتحانات یا آزمایشات برای مشکلات دیگر یافت میشوند. اما این علائم یا آزمایشهای اولیه معمولاً برای اطمینان از اینکه فرد دارای GIST یا نوع دیگری از تومور گوارشی (GI) است کافی نیست. اگر فرد مشکوک به تومور دستگاه گوارش باشد، باید آزمایشهای بیشتری برای تأیید وجود آن انجام دهد.
سابقه پزشکی و معاینه فیزیکی
پزشک از شما سوالاتی در مورد سابقه پزشکیتان از جمله علائم، عوامل خطرزای احتمالی، سابقه خانوادگی و سایر شرایط پزشکی خواهد پرسید.
پزشک شما را معاینه فیزیکی میکند تا اطلاعات بیشتری در مورد علائم احتمالی تومور دستگاه گوارش، مانند وجود توده در شکم یا سایر مشکلات سلامتی به دست آورد.
اگر دلیلی برای مشکوک بودن به GIST یا نوع دیگری از تومور GI وجود داشته باشد، پزشک آزمایشهای تصویر برداری یا معاینات آندوسکوپی را برای کمک به کشف سرطان یا چیز دیگری انجام میدهد. اگر به پزشک مراقبتهای اولیه خود مراجعه میکنید، ممکن است به یک متخصص، مانند یک متخصص گوارش (پزشکی که بیماریهای دستگاه گوارش را درمان میکند) ارجاع داده شود.
اگر GIST یافت شود، احتمالاً آزمایشهای بیشتری برای کمک به تعیین مرحله (وسعت) سرطان خواهید داشت.
تستهای تصویر برداری
در آزمایشهای تصویر برداری از اشعه ایکس، میدانهای مغناطیسی یا مواد رادیو اکتیو برای ایجاد تصاویری از داخل بدن استفاده میشود. تستهای تصویر برداری به دلایل مختلفی انجام میشود، از جمله:
برای کمک به کشف اینکه آیا یک منطقه مشکوک ممکن است سرطانی باشد یا خیر
برای اینکه بفهمید سرطان چقدر گسترش یافته است
برای کمک به تعیین اینکه آیا روند درمان موثر بوده است یا خیر
برای جستجوی نشانههایی مبنی بر بازگشت سرطان
اکثر افرادی که فکر میکنند تومور دستگاه گوارش دارند یک یا چند مورد از این آزمایشها را انجام میدهند.
اسکن توموگرافی کامپیوتری (CT یا Computed tomography)
سی تی اسکن از اشعه ایکس برای ایجاد تصاویر دقیق و مقطعی از بدن شما استفاده میکند. برخلاف اشعه ایکس معمولی، سی تی اسکن تصاویر دقیقی از بافتهای نرم بدن ایجاد میکند.
سی تی اسکن میتواند در بیمارانی که GIST دارند (یا ممکن است داشته باشند) برای یافتن محل و اندازه تومور و همچنین برای مشاهده اینکه آیا تومور به سایر قسمتهای بدن سرایت کرده است یا خیر، مفید باشد.
در برخی موارد، از سی تی اسکن نیز میتوان برای هدایت سوزن بیوپسی به سمت سرطان مشکوک استفاده کرد. با این حال، اگر تومور ممکن است GIST باشد (به دلیل خطر خونریزی و احتمال افزایش خطر گسترش تومور)، این کار میتواند خطرناک باشد، بنابراین، این نوع بیوپسیها معمولاً تنها در صورتی انجام میشوند که نتیجه ممکن است بر تصمیم گیری در مورد روند درمان تأثیر بگذارد. (مبحث بیوپسی را در ادامه مطالعه کنید.)
اسکن تصویر برداری رزونانس مغناطیسی (MRI یا Magnetic resonance imaging)
مانند سی تی اسکن، اسکن ام آر آی تصاویر دقیقی از بافتهای نرم بدن نشان میدهد. اما در اسکن MRI به جای اشعه ایکس از امواج رادیویی و آهنرباهای قوی استفاده میشود.
اسکن MRI گاهی اوقات میتواند در افراد مبتلا به GIST برای کمک به یافتن وسعت سرطان در شکم مفید باشد اما معمولاً سی تی اسکن کافی است. MRI همچنین میتواند برای بررسی سرطانی که ممکن است عود کرده باشد (عود کرده) یا گسترش یافته باشد (متاستاز یا metastasized) به اندامهای دور دست، به ویژه در مغز یا ستون فقرات، استفاده شود.
اشعه ایکس باریم (Barium x-rays)
اشعه ایکس باریم به اندازه گذشته مورد استفاده قرار نمیگیرد. آنها تا حد زیادی با CT/MRI و آندوسکوپی جایگزین شده اند (حالتی که پزشک در واقع به داخل مری، معده و روده شما با یک محدوده فیبر نوری باریک نگاه میکند – ادامه مطلب را مطالعه کنید).
برای این نوع اشعه ایکس، از مایع گچی حاوی باریم برای پوشاندن پوشش داخلی مری، معده و روده استفاده میشود. این امر باعث میشود که قسمتهای غیر طبیعی پوشش در اشعه ایکس راحتتر دیده شوند. این آزمایشها گاهی اوقات برای تشخیص تومورهای دستگاه گوارش استفاده میشوند اما ممکن است برخی از تومورهای روده کوچک را نادیده بگیرند.
احتمالاً از شب قبل از آزمون ناشتا باشید. اگر روده بزرگ شما در حال معاینه است، ممکن است لازم باشد از ملینها و/یا تنقیه برای پاکسازی روده شب قبل یا صبح روز معاینه استفاده کنید.
بلع باریم (Barium swallow)
این اغلب اولین آزمایشی است که در صورت داشتن مشکل در بلع انجام میشود. برای این آزمایش، مایعی حاوی باریم مینوشید تا پوشش داخلی مری را بپوشاند. سپس طی چند دقیقه بعد یک سری عکس برداری با اشعه ایکس گرفته میشود.
سری فوقانی GI
این آزمایش شبیه به بلع باریم است، با این تفاوت که عکس برداری با اشعه ایکس پس از اینکه باریم زمان لازم برای پوشاندن معده و قسمت اول روده کوچک را داشت، انجام میشود. برای بررسی مشکلات در بقیه قسمتهای روده کوچک، میتوان در چند ساعت آینده با عبور باریم عکسهای اشعه ایکس بیشتری گرفت. به این عمل رهگیری روده کوچک (small bowel follow-through) میگویند.
انتروکلایز (Enteroclysis)
یک لوله نازک از دهان یا بینی، به پایین مری و از طریق معده به ابتدای روده کوچک عبور میکند. باریم همراه با ماده ای از طریق لوله فرستاده میشود که هوای بیشتری در روده ایجاد میکند و باعث انبساط آنها میشود. سپس اشعه ایکس از روده گرفته میشود. این آزمایش میتواند تصاویر بهتری از روده باریک نسبت به روش پیگیری روده کوچک (small bowel follow-through) ارائه دهد، اما همچنین ناراحت کننده تر است.

تنقیه باریم (Barium enema)
این آزمایش (همچنین به عنوان سری GI پایین یا lower GI series شناخته میشود) برای بررسی سطح داخلی روده بزرگ (کولون و رکتوم) استفاده میشود. برای این آزمایش، محلول باریم از طریق یک لوله کوچک و قابل انعطاف که در مقعد قرار داده میشود، در حالی که روی میز اشعه ایکس دراز کشیده اید.
اغلب، هوا از طریق لوله به داخل دمیده میشود تا باریم را به سمت دیواره روده بزرگ فشار دهد و سطح داخلی را بهتر بپوشاند. این تنقیه باریم کنتراست هوا (air-contrast barium enema) یا باریم تنقیه دو کنتراست (double-contrast barium enema) نامیده میشود. ممکن است از شما خواسته شود برای کمک به انتشار باریم و همچنین برای دریافت نماهای مختلف از روده، موقعیت خود را تغییر دهید. سپس یک یا چند مجموعه عکس اشعه ایکس گرفته میشود.
اسکن توموگرافی گسیل پوزیترون (PET)
برای اسکن PET، نوعی قند کمی رادیو اکتیو به شما تزریق میشود که عمدتاً در سلولهای سرطانی جمع میشود. سپس از یک دوربین مخصوص برای ایجاد تصویری از مناطق پرتوزا در بدن استفاده میشود. تصویر مانند سی تی اسکن یا ام آر آی دقیق نیست اما اسکن PETمیتواند به دنبال گسترش احتمالی سرطان در تمام نواحی بدن به طور همزمان باشد.
در حال حاضر بسیاری از مراکز دارای دستگاههایی هستند که میتوانند همزمان PET و CT اسکن (PET/CT scan) را انجام دهند. این کار به پزشک اجازه میدهد تا مناطقی را که در اسکن PET “روشن میشوند” با جزئیات بیشتری ببیند.
اسکن PETمیتواند برای بررسی GIST مفید باشد، به خصوص اگر نتایج اسکن CT یا MRI واضح نباشد. این آزمایش همچنین میتواند برای جستجوی مناطق احتمالی که ممکن است سرطان در آن گسترش یافته باشد برای کمک به تعیین اینکه آیا جراحی گزینه مناسبی است، استفاده شود.
اسکن PET همچنین میتواند در یافتن اینکه آیا یک درمان دارویی مؤثر است یا خیر، مفید باشد زیرا اغلب میتواند سریع تر از CT یا MRI پاسخ دهد. اسکن معمولا چند هفته پس از شروع دارو انجام میشود. اگر دارو مؤثر باشد، تومور دیگر قند رادیو اکتیو را جذب نمیکند. اگر تومور همچنان قند را جذب کند، پزشک ممکن است تصمیم بگیرد که درمان دارویی شما را تغییر دهد.
آندوسکوپی (Endoscopy)
برای انجام آندوسکوپی، پزشک یک آندوسکوپ (لوله ای با نور منعطف با یک دوربین فیلم برداری کوچک در انتهای بدن) قرار میدهد تا پوشش داخلی دستگاه گوارش (GI) را ببیند. در صورت یافتن نواحی غیر طبیعی، میتوان قطعات کوچک را از طریق آندوسکوپ بیوپسی (برداشت) کرد. نمونههای بیوپسی زیر میکروسکوپ بررسی میشوند تا مشخص شود که آیا سرطان دارند و اگر چنین است، بیماری چه نوع سرطانی است.
GISTها اغلب در زیر سطح (مخاط) پوشش داخلی دستگاه گوارش قرار دارند. این میتواند دیدن آنها را با آندوسکوپی سخت تر از تومورهای رایج دستگاه گوارش که معمولاً از مخاط شروع میشود، کند. در صورت وجود GIST، پزشک ممکن است تنها یک برآمدگی زیر سطح نرمال صاف را ببیند. بیوپسی GISTهایی که زیر مخاط هستند نیز از طریق آندوسکوپ سخت تر است. این یکی از دلایلی است که بسیاری از GISTها قبل از جراحی تشخیص داده نمیشوند.
اگر تومور از پوشش داخلی دستگاه گوارش شکسته باشد و در آندوسکوپی به راحتی قابل مشاهده باشد، احتمال انتشار GIST به سایر قسمتهای بدن بیشتر است.
آندوسکوپی فوقانی (Upper endoscopy)
آندوسکوپ از دهان و گلو عبور داده میشود تا به پوشش داخلی مری، معده و قسمت اول روده کوچک نگاه کند. نمونههای بیوپسی ممکن است از هر ناحیه غیر طبیعی گرفته شود.
آندوسکوپی فوقانی را میتوان در یک بیمارستان، در یک مرکز جراحی سرپایی یا در مطب پزشک انجام داد. معمولاً از طریق یک خط وریدی (IV) دارو به شما داده میشود تا قبل از معاینه شما را خواب آلود و بیهوش کند. خود معاینه معمولاً 10 تا 20 دقیقه طول میکشد اما در صورت مشاهده تومور یا نمونه برداری از ناحیه ممکن است بیشتر طول بکشد. اگر دارویی برای خواب آلودگی شما تجویز میشود، احتمالاً به کسی که میشناسید نیاز خواهید داشت که شما را به خانه برساند (نه فقط یک تاکسی یا سرویس اشتراک سواری).
این آزمایش با نام EGD (مخفف ازوفاگوگاسترودئودنوسکوپی یا esophagogastroduodenoscopy) نیز شناخته میشود.
کولونوسکوپی (آندوسکوپی تحتانی یا Colonoscopy)
در کولونوسکوپی، نوعی آندوسکوپ به نام کولونوسکوپ از طریق مقعد و به داخل روده بزرگ وارد میشود. این کار به پزشک اجازه میدهد تا به پوشش داخلی راست روده و کولون نگاه کند و نمونههای بیوپسی را از هر ناحیه غیر طبیعی بگیرد.
برای مشاهده خوب داخل روده بزرگ، باید قبل از آزمایش آن را تمیز کرد. پزشک دستورالعملهای خاصی را به شما خواهد داد. ممکن است لازم باشد یک روز یا بیشتر قبل از آزمایش یک رژیم غذایی خاص را دنبال کنید. همچنین ممکن است مجبور شوید عصر قبل مقدار زیادی ملین مایع بنوشید، به این معنی که زمان زیادی را در دستشویی خواهید گذراند.
کولونوسکوپی را میتوان در یک بیمارستان، در یک مرکز جراحی سرپایی یا در مطب پزشک انجام داد. احتمالاً به شما داروی داخل وریدی (IV) داده میشود تا در طول عمل احساس آرامش و خواب آلودگی داشته باشید. در موارد کمتر، ممکن است به شما بیهوشی عمومی داده شود تا شما را به خواب عمیق بکشاند. معاینه معمولاً 15 تا 30 دقیقه طول میکشد اما در صورت مشاهده تومور و یا بیوپسی ممکن است بیشتر طول بکشد. از آن جایی که دارو برای خواب آلودگی شما تجویز میشود، احتمالاً به کسی که میشناسید نیاز خواهید داشت که شما را به خانه برساند (نه فقط یک تاکسی یا سرویس اشتراک سواری).
آندوسکوپی کپسولی (Capsule endoscopy)
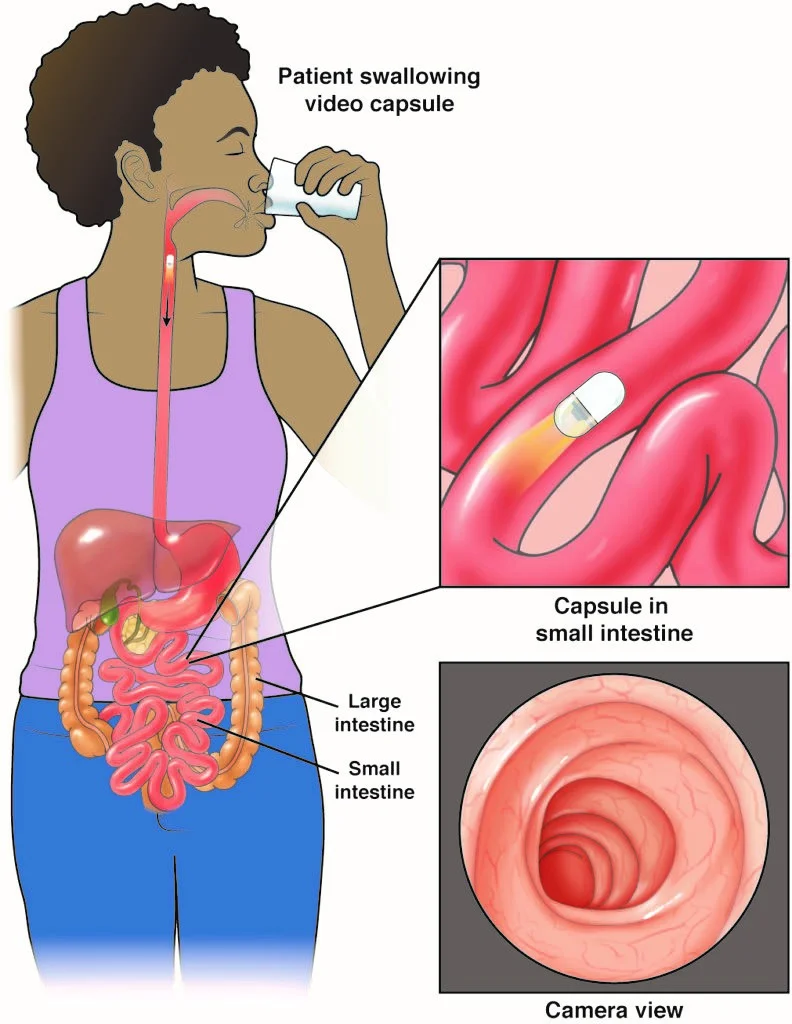
نه آندوسکوپی فوقانی و نه کولونوسکوپی نمیتوانند به تمام نواحی روده کوچک برسند. آندوسکوپی کپسولی یکی از راههای بررسی روده کوچک است.
این روش در واقع از آندوسکوپ استفاده نمیکند. در عوض، شما یک کپسول (به اندازه یک قرص ویتامین بزرگ) را میبلعید که حاوی یک منبع نور و یک دوربین کوچک است.
مانند یک قرص، همانطور که کپسول در روده حرکت میکند (معمولاً حدود 8 ساعت)، هزاران عکس میگیرد. این تصاویر به صورت الکترونیکی به دستگاهی که دور کمر شما بسته میشود، منتقل میشود. سپس میتوان تصاویر را در رایانه بارگیری کرد، جایی که پزشک میتواند آنها را به صورت ویدیو مشاهده کند. کپسول در طی یک حرکت عادی روده از بدن خارج شده و دور ریخته میشود.
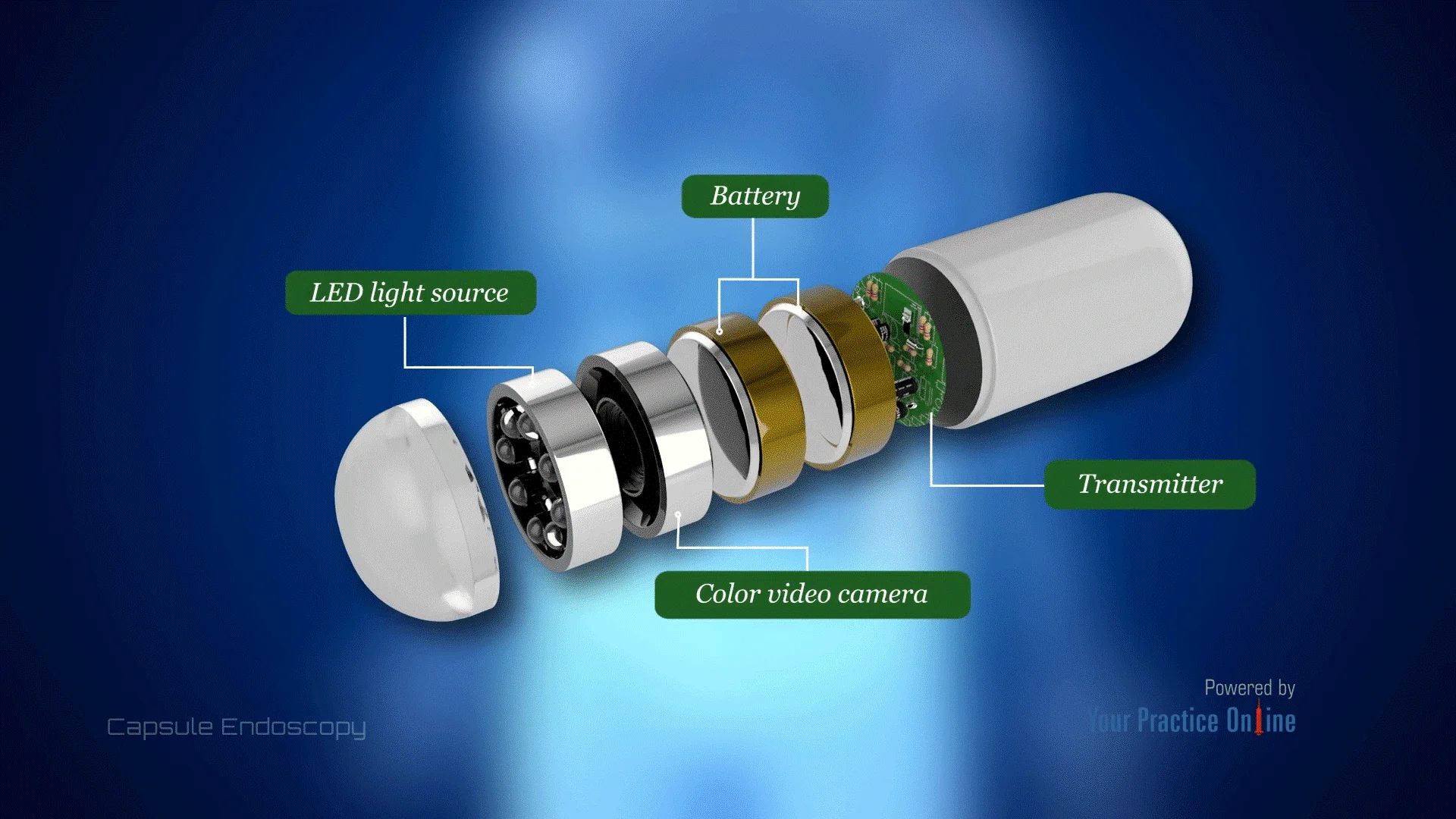
این آزمایش نیازی به آرام بخش ندارد – شما میتوانید فعالیتهای عادی روزانه خود را در حین حرکت کپسول از طریق دستگاه گوارش ادامه دهید. این تکنیک هنوز نسبتاً جدید است و بهترین راههای استفاده از آن هنوز در حال مطالعه است. یکی از معایب آن این است که هر ناحیه غیر طبیعی که دیده میشود را نمیتوان در طول آزمایش بیوپسی کرد.
انتروسکوپی با بالون دوبل (آندوسکوپی یا Double balloon enteroscopy)
این روش دیگری برای نگاه کردن به روده کوچک است. روده کوچک بیش از حد طولانی است و دارای انحناهای زیادی است که نمیتوان با آندوسکوپی منظم به خوبی آن را بررسی کرد. اما این روش با استفاده از یک آندوسکوپ مخصوص که از 2 لوله ساخته شده است، این مشکلات را برطرف میکند.
به شما داروی داخل وریدی (IV) برای کمک به آرام کردن شما داده میشود یا حتی بیهوشی عمومی (به طوری که شما در خواب هستید). سپس بسته به اینکه قسمت خاصی از روده کوچک برای بررسی وجود دارد یا خیر، آندوسکوپ از طریق دهان یا مقعد وارد میشود.
به محض اینکه وارد روده کوچک شد، لوله داخلی که دوربین در انتهای آن قرار دارد، حدود یک فوت به جلو کشیده میشود زیرا پزشک به دیواره روده نگاه میکند. سپس یک بالون در انتهای آندوسکوپ باد میشود تا آن را لنگر بیاندازد. سپس لوله بیرونی تا نزدیک انتهای لوله داخلی به جلو هل داده میشود و با بالون دوم در جای خود محکم میشود. بالون اول خالی میشود و آندوسکوپ دوباره به جلو میرود. این فرآیند بارها و بارها تکرار میشود و به پزشک اجازه میدهد روده را در یک لحظه ببیند. این آزمون ممکن است ساعتها طول بکشد.
این آزمایش ممکن است همراه با آندوسکوپی کپسولی انجام شود. مزیت اصلی این آزمایش نسبت به آندوسکوپی کپسولی این است که در صورت مشاهده موارد غیر طبیعی، پزشک میتواند نمونه برداری انجام دهد. مانند سایر اشکال آندوسکوپی، از آن جایی که به شما دارو داده میشود تا شما را برای این عمل خواب آلود کند، کسی که میشناسید احتمالاً نیاز دارد که شما را به خانه برساند (نه فقط یک تاکسی یا خدمات اشتراک سواری).
سونوگرافی آندوسکوپی (EUS یا Endoscopic ultrasound)
این یک نوع آزمایش تصویر برداری است که از آندوسکوپ استفاده میکند. اولتراسوند از امواج صوتی برای گرفتن عکس از قسمتهایی از بدن استفاده میکند. برای اکثر معاینات اولتراسوند، یک پروب گرز مانند (به نام مبدل یا transducer) روی پوست قرار میگیرد. کاوشگر امواج صوتی را منتشر میکند و الگوی پژواکهایی را که برمیگردند، تشخیص میدهد.
در EUS، پروب اولتراسوند در نوک آندوسکوپ قرار دارد. این اجازه میدهد تا پروب بسیار نزدیک (یا بالای) تومور در دیواره دستگاه گوارش قرار گیرد. مانند یک اولتراسوند معمولی، کاوشگر امواج صوتی منتشر میکند و سپس پژواکهایی را که به عقب بازمیگردند، تشخیص میدهد. سپس یک کامپیوتر پژواکها را به تصویری از منطقه ای که به آن نگاه میشود، ترجمه میکند.
EUS میتواند برای یافتن مکان دقیق GIST و تعیین اندازه آن استفاده شود. این برای یافتن عمق رشد تومور در دیواره دستگاه گوارش (یا فراتر از آن و به اندام مجاور) مفید است. این آزمایش همچنین میتواند نشان دهد که آیا تومور به غدد لنفاوی مجاور گسترش یافته است یا خیر. همچنین میتوان از آن برای کمک به بیوپسی سوزنی استفاده کرد. (در موارد کمتر، ممکن است به شما بیهوشی عمومی داده شود تا شما را به خواب عمیق بکشاند.) به همین دلیل، احتمالاً نیاز دارید که شخصی را که میشناسید شما را به خانه ببرد (نه فقط یک تاکسی یا سرویس اشتراک سواری).
بیوپسی (Biopsy)
حتی اگر چیزی غیر طبیعی در یک آزمایش تصویر برداری مانند اشعه ایکس باریم یا سی تی اسکن دیده شود، این آزمایشها اغلب نمیتوانند با اطمینان مشخص کنند که آیا ناحیه غیر طبیعی GIST، نوع دیگری از تومور (خوش خیم یا سرطان) است یا برخی شرایط دیگر (مانند عفونت). تنها راه برای دانستن اینکه مطمئنا چه چیزی است، حذف سلولها از ناحیه است. این روش بیوپسی (Biopsy) نامیده میشود. سلولها سپس به آزمایشگاه فرستاده میشوند، جایی که دکتری به نام پاتولوژیست آنها را زیر میکروسکوپ بررسی میکند و ممکن است آزمایشهای دیگری را روی آنها انجام دهد.
همه کسانی که توموری دارند که ممکن است GIST باشد، قبل از درمان نیاز به بیوپسی ندارند. اگر پزشک مشکوک باشد که یک تومور GIST است، بیوپسی معمولاً تنها در صورتی انجام میشود که به تعیین گزینههای درمانی کمک کند. GISTها اغلب تومورهای شکننده ای هستند که تمایل دارند از هم جدا شوند و به راحتی خونریزی کنند. هر نمونه برداری باید بسیار با احتیاط انجام شود زیرا این خطر وجود دارد که بیوپسی ممکن است باعث خونریزی یا احتمالاً افزایش خطر گسترش سرطان شود.
روشهای مختلفی برای بیوپسی تومور دستگاه گوارش وجود دارد.
بیوپسی آندوسکوپی (Endoscopic biopsy)
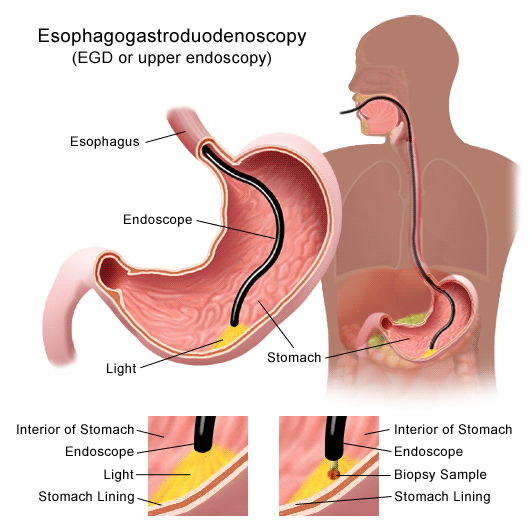
نمونههای بیوپسی را میتوان از طریق آندوسکوپ به دست آورد. هنگامی که یک تومور پیدا شد، پزشک میتواند فورسپس بیوپسی (انبر یا biopsy forceps) را از طریق لوله وارد کند تا نمونه کوچکی از تومور را بگیرد.
حتی اگر نمونه بسیار کوچک باشد، پزشکان اغلب میتوانند تشخیص دقیقی بدهند. با این حال، با GIST، گاهی اوقات فورسپس بیوپسی نمیتواند به اندازه کافی عمیق شود که به تومور برسد زیرا در زیر پوشش داخلی معده یا روده قرار دارد.
خونریزی از GIST پس از بیوپسی نادر است اما میتواند یک مشکل جدی باشد.
دوربین بسیار کوچک است. مانند هر قرص دیگری، کپسول از معده عبور میکند و وارد روده کوچک میشود.
اگر این اتفاق بیفتد، پزشکان گاهی اوقات میتوانند از طریق آندوسکوپ داروهایی را به تومور تزریق کنند تا رگهای خونی را منقبض کرده و خونریزی را متوقف کنند.
بیوپسی سوزنی (Needle biopsy)
بیوپسی همچنین میتواند با استفاده از یک سوزن نازک و توخالی برای برداشتن نمونههای کوچک از ناحیه انجام شود. رایج ترین راه برای انجام این کار در طول سونوگرافی آندوسکوپی است (توضیح داده شده در بالا). پزشک از تصویر اولتراسوند برای هدایت یک سوزن در نوک آندوسکوپ به داخل تومور استفاده میکند. این به عنوان آسپیراسیون با سوزن ظریف با هدایت اولتراسوند آندوسکوپی (endoscopic ultrasound-guided fine needle aspiration یا EUS-FNA) شناخته میشود.
در موارد کمتر، پزشک ممکن است یک سوزن را از طریق پوست و داخل تومور قرار دهد در حالی که توسط یک آزمایش تصویر برداری مانند سی تی اسکن هدایت میشود. این روش به عنوان بیوپسی از راه پوست (percutaneous biopsy.) شناخته میشود.
بیوپسی جراحی (Surgical biopsy)
اگر نتوان نمونهای را از نمونه برداری آندوسکوپی یا سوزنی دریافت کرد، یا اگر نتیجه بیوپسی بر گزینههای درمانی تأثیری نداشت، ممکن است پزشک توصیه کند تا زمان جراحی برای برداشتن تومور منتظر بمانید تا نمونه برداری از آن انجام شود.
اگر جراحی از طریق یک برش (incision) بزرگ در شکم انجام شود، به آن لاپاراتومی (laparotomy) میگویند. گاهی اوقات میتوان از تومور نمونه برداری کرد (یا میتوان تومورهای کوچک را برداشت) با استفاده از یک لوله نازک و نورانی به نام لاپاروسکوپ که به جراح اجازه میدهد از طریق یک برش کوچک، داخل شکم را ببیند. سپس جراح میتواند تومور را با استفاده از ابزارهای جراحی بلند و نازک که از طریق برشهای کوچک دیگر در شکم رد میشود، نمونه برداری کند (یا خارج کند). این به عنوان جراحی لاپاراسکوپی یا سوراخ کلید (keyhole surgery) شناخته میشود.
تستهای آزمایشگاهی نمونههای بیوپسی
هنگامی که نمونههای تومور به دست آمد، یک پاتولوژیست ممکن است تنها با نگاه کردن به سلولها با میکروسکوپ بتواند تشخیص دهد که یک تومور به احتمال زیاد GIST است. اما گاهی ممکن است برای اطمینان به آزمایشات آزمایشگاهی بیشتری نیاز باشد.
ایمونوهیستوشیمی (Immunohistochemistry): برای این آزمایش، بخشی از نمونه با آنتی بادیهای دست ساز درمان میشود که فقط به پروتئین خاصی در سلولها میچسبند. در صورت وجود پروتئین، آنتی بادیها باعث تغییر رنگ میشوند که در زیر میکروسکوپ قابل مشاهده است.
اگر مشکوک به GIST باشد، برخی از پروتئینهایی که اغلب برای آنها آزمایش انجام میشود، KIT (همچنین به عنوان CD117 شناخته میشود) و DOG1 هستند. اکثر سلولهای GIST این پروتئینها را دارند اما سلولهای بسیاری از انواع سرطانهای دیگر این پروتئینها را ندارند، بنابراین آزمایشهای این پروتئینها میتواند به تشخیص اینکه آیا تومور GI یک GIST است یا خیر، کمک میکند. سایر پروتئینها مانند CD34 نیز ممکن است مورد آزمایش قرار گیرند.
آزمایش ژنتیک مولکولی (Molecular genetic testing): آزمایش ممکن است برای جستجوی جهش در ژنهای KIT یا PDGFRA نیز انجام شود زیرا اکثر سلولهای GIST دارای جهش در یکی یا دیگری هستند. همچنین آزمایش برای جهش در این ژنها میتواند کمک کند که آیا داروهای درمانی هدفمند خاصی در درمان سرطان مفید هستند یا خیر.
در موارد کمتر، ممکن است آزمایشهایی برای بررسی تغییرات در ژنهای دیگر، مانند ژنهای SDH انجام شود.
نرخ میتوز (Mitotic rate): اگر GIST تشخیص داده شود، پزشک همچنین به سلولهای سرطانی موجود در نمونه نگاه میکند تا ببیند چه تعداد از آنها به طور فعال به سلولهای جدید تقسیم میشوند. این شاخصه به عنوان نرخ میتوزی (یا شاخص میتوزی) شناخته میشود. نرخ میتوزی کم به این معنی است که سلولهای سرطانی به آرامی رشد میکنند و تقسیم میشوند، در حالی که نرخ بالا به این معنی است که آنها به سرعت رشد میکنند. نرخ میتوز بخش مهمی در تعیین مرحله سرطان است. (به مبحث مراحل تومور استرومای گوارشی مراجعه کنید.)
آزمایشات خون
اگر پزشک شما فکر کند که GIST دارید ممکن است آزمایش خون را تجویز کند.
هیچ آزمایش خونی وجود ندارد که بتواند با اطمینان بگوید که آیا یک فرد GIST دارد یا خیر. اما آزمایش خون گاهی اوقات میتواند به یک تومور احتمالی (یا گسترش آن) اشاره کند. مثلا:
شمارش کامل خون (CBC یا complete blood count) میتواند نشان دهد که تعداد گلبولهای قرمز خون شما پایین است (یعنی اگر کم خون هستید). برخی از افراد مبتلا به GIST ممکن است به دلیل خونریزی از تومور دچار کم خونی شوند.
آزمایشهای غیر طبیعی عملکرد کبد ممکن است به این معنی باشد که GIST به کبد شما سرایت کرده است.
آزمایشهای خون نیز برای بررسی سلامت کلی شما قبل از جراحی یا زمانی که درمانهای دیگری مانند درمان هدفمند انجام میدهید، انجام میشود.
مراحل تومور استرومای دستگاه گوارش و سایر عوامل پیش بینی کننده وضعیت آتی
پس از تشخیص سرطان در فردی، پزشکان سعی میکنند بفهمند که آیا سرطان گسترش یافته است یا خیر و اگر چنین است، تا کجا. این فرآیند که مرحله بندی (staging) نامیده میشود، بر اساس نتایج معاینات فیزیکی و آزمایشهای دیگر است که در مبحث Tests for Gastrointestinal Stromal Tumors توضیح داده شده است.
مرحله سرطان، میزان سرطان در بدن را توصیف میکند. این کار به تعیین اینکه سرطان چقدر جدی است و بهترین روش درمان آن کمک میکند. پزشکان همچنین هنگام صحبت در مورد آمار بقا و زنده مانی از مرحله سرطان استفاده میکنند.
مراحل تومورهای استرومال گوارشی (GIST) از I (1) تا IV (4) متغیر است. به عنوان یک قاعده، هرچه این عدد کمتر باشد، سرطان کمتر گسترش یافته است. عدد بالاتر، مانند مرحله IV، به معنای گسترش بیشتر سرطان است. در یک مرحله، حرف قبل به معنای مرحله پایین تر است. اگرچه تجربه سرطان هر فرد منحصر به فرد است، سرطانهایی که مراحل مشابهی دارند، چشم انداز مشابهی نیز دارند و اغلب به روشی مشابهی نیز درمان میشوند.
سیستم مرحله بندی AJCC TNM
سیستم مرحله بندی که اغلب برای تومورهای GIST استفاده میشود، سیستم TNM کمیته مشترک آمریکایی سرطان (American Joint Committee on Cancer یا AJCC) است. جدید ترین نسخه از سال 2018 قابل اجرا است. این سیستم مرحله بندی بر اساس 4 اطلاعات کلیدی است:
وسعت تومور اصلی (اولیه) (T): اندازه سرطان چقدر است؟
گسترش به غدد لنفاوی مجاور (N): آیا سرطان به غدد لنفاوی مجاور سرایت کرده است؟ (این اتفاق در GIST غیر معمول است.)
گسترش (متاستاز) به نقاط دور دست (M): آیا سرطان به نقاط دور دست بدن گسترش یافته است؟ (شایع ترین محل انتشار کبد، استخوانها، ریهها و لایههای بافتی است که داخل شکم را پوشانده اند.)
نرخ میتوزی: این یک آزمایش آزمایشگاهی است که نشان میدهد سلولهای سرطانی با چه سرعتی در حال رشد و تقسیم هستند. به عنوان کم یا زیاد توصیف میشود. نرخ میتوزیک پایین نتیجه بهتری را پیش بینی میکند.
اعداد یا حروف بعد از T، N و M جزئیات بیشتری در مورد هر یک از این عوامل ارائه میدهند. اعداد بالاتر به معنای پیشرفته تر بودن سرطان است. هنگامی که دسته بندیهای T، N و M یک فرد مشخص شد، این اطلاعات در فرآیندی به نام گروه بندی مرحله ای (stage grouping) ترکیب میشوند تا یک مرحله کلی را تعیین کنند. اگرچه دستههای T، N و Mبرای همه GIST یکسان هستند، بسته به اینکه سرطان از کجا شروع میشود، 2 طرح گروه بندی مرحلهای متفاوت وجود دارد:
معده یا امنتوم (لایه پیش بند مانندی از بافت چربی که بر روی اندامهای شکم آویزان است)
روده کوچک، مری، کولون، رکتوم یا صفاق (لایه ای از بافت که اندامها و دیوارههای شکم را میپوشاند.)
این به این دلیل است که احتمال رشد و انتشار GISTهایی که از معده یا امنتوم شروع میشوند، معمولاً نسبت به GISTهایی که در مکانهای دیگر شروع میشوند، به سایر قسمتهای بدن کمتر است.
مرحله بندی سرطان میتواند پیچیده باشد، بنابراین از پزشک خود بخواهید آن را به گونه ای که شما درک میکنید برای شما توضیح دهد.
میزان بقا و زنده مانی برای تومورهای استرومال دستگاه گوارش
میزان بقا میتواند به شما این ایده را بدهد که چند درصد از افراد مبتلا به همان نوع و مرحله سرطان تا مدت معینی (معمولاً 5 سال) پس از تشخیص هنوز زنده هستند. این اعداد نمیتوانند به شما بگویند که چقدر زنده خواهید مان، اما ممکن است به شما کمک کنند تا درک بهتری از احتمال موفقیت روند درمانتان داشته باشید.
به خاطر داشته باشید که میزان بقا تخمینی است و اغلب بر اساس نتایج قبلی تعداد زیادی از افرادی است که سرطان خاصی داشتند، اما آنها نمیتوانند پیش بینی کنند که در مورد فرد خاصی چه اتفاقی خواهد افتاد. این آمار میتواند گیج کننده باشد و ممکن است شما را به پرسیدن سوالات بیشتری سوق دهد. پزشک شما با وضعیت شما آشناست. از وی بپرسید چگونه این اعداد ممکن است برای شما اعمال شوند.
نرخ بقای نسبی 5 ساله چیست؟
نرخ بقای نسبی، افراد دارای نوع و مرحله تومور استرومال دستگاه گوارش (GIST) را با افراد در کل جمعیت مقایسه میکند. به عنوان مثال، اگر نرخ بقای نسبی 5 ساله برای مرحله خاصی از GISTنود درصد باشد، به این معنی است که افرادی که به آن سرطان مبتلا هستند نسبت به افرادی که آن سرطان را ندارند، به طور متوسط حدود 90 درصد احتمال دارد تا حداقل به مدت 5 سال پس از تشخیص
این اعداد از کجا میآیند؟
انجمن سرطان آمریکا به اطلاعات پایگاه داده SEER* که توسط موسسه ملی سرطان (National Cancer Institute یا NCI) نگهداری میشود، برای ارائه آمار بقای انواع مختلف سرطان متکی است.
پایگاه داده SEER نرخ بقای نسبی 5 ساله GIST در ایالات متحده را بر اساس میزان گسترش سرطان دنبال میکند. با این حال، پایگاه داده SEER سرطانها را بر اساس مراحل AJCC TNM (مرحله 1، مرحله 2، مرحله 3 و غیره) گروه بندی نمیکند. در عوض، سرطانها را به مراحل موضعی، منطقه ای و دور دسته بندی میکند:
موضعی (Localized): سرطان محدود به اندامی است که از آن جا شروع شده است (مثلاً روده کوچک، مری یا معده).
منطقه ای (Regional): سرطان به ساختارهای مجاور رشد کرده یا به غدد لنفاوی مجاور گسترش یافته است.
دور (Distant): سرطان به نقاط دورتر بدن مانند کبد گسترش یافته است.
نرخ بقای نسبی 5 ساله برای GIST
این اعداد بر اساس افراد مبتلا به GIST [روده کوچک، مری، کولون، رکتوم، صفاق، معده، امنتوم] بین سالهای 2011 تا 2017 است.
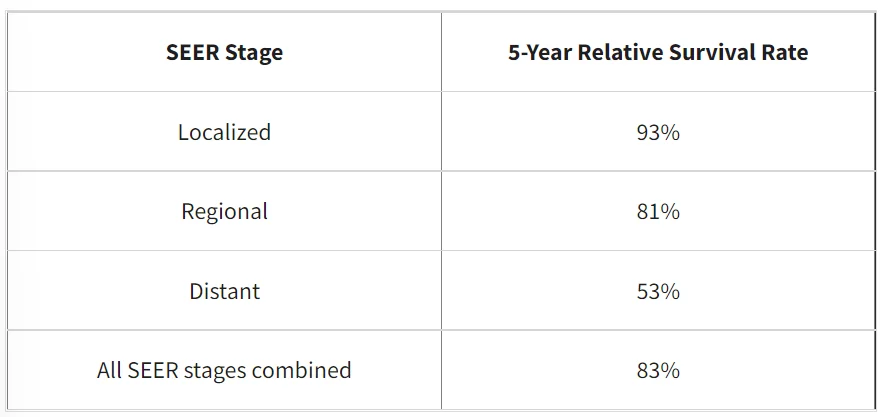
درک اعداد
این اعداد فقط برای مرحله سرطان زمانی که برای اولین بار تشخیص داده میشود، اعمال میشود. اگر سرطان رشد کند، گسترش یابد یا پس از درمان عود کند، بعداً اعمال نمیشوند.
این اعداد همه چیز را در نظر نمیگیرند. میزان بقا بر اساس میزان گسترش سرطان گروه بندی میشوند اما عوامل دیگری مانند سن و سلامت کلی شما، اینکه آیا سرطان میتواند برداشته شود یا خیر و اینکه سرطان چگونه به درمان پاسخ میدهد نیز میتواند بر دیدگاه شما تأثیر بگذارد.
افرادی که اکنون با GIST تشخیص داده میشوند، ممکن است چشم انداز بهتری نسبت به این اعداد داشته باشند. درمانها در طول زمان بهبود یافته اند و این اعداد بر أساس اطلاعات افرادی است که حداقل پنج سال قبل تشخیص داده شده و درمان شده اند.
جراحی برای تومورهای استرومال دستگاه گوارش
جراحی معمولاً روش درمانی اصلی تومورهای استرومال گوارشی (GIST) است که گسترش نیافته اند. هدف از جراحی حذف تمام سرطان است.
نوع جراحی مورد نیاز بستگی به محل و اندازه تومور دارد.
جراحی برای GISTهای کوچک
اگر تومور کوچک باشد، اغلب میتوان آن را همراه با ناحیه کوچکی از بافت طبیعی اطراف آن برداشت. این کار از طریق یک برش (incision) در پوست انجام میشود.
برخلاف بسیاری از سرطانهای دیگر، GIST تقریباً هرگز به غدد لنفاوی گسترش نمییابد، بنابراین معمولاً نیازی به برداشتن غدد لنفاوی مجاور نیست.
برای برخی از سرطانهای کوچک، جراحی سوراخ کلید (لاپاراسکوپی) یک گزینه است. به جای ایجاد یک برش بزرگ در پوست برای برداشتن تومور، از چندین برش کوچک استفاده میشود.
جراح یک لوله نازک و روشن با یک دوربین فیلم برداری کوچک در انتهای آن (لاپاراسکوپ) را از طریق یکی از آنها وارد میکند. این کار به آنها اجازه میدهد داخل شکم را ببینند. سپس از ابزارهای جراحی بلند و نازک از طریق برشهای دیگر برای برداشتن تومور استفاده میشود. از آن جایی که برشها کوچک هستند، بیماران معمولاً سریع تر از این نوع جراحی نسبت به جراحی سنتی که نیاز به برش طولانی تری دارند، بهبود مییابند.
جراحی برای GISTهای بزرگتر
اگر تومور بزرگ باشد یا در اندامهای دیگر رشد کند، جراح ممکن است همچنان بتواند آن را به طور کامل حذف کند. برای انجام این کار، ممکن است لازم باشد بخشهایی از اندامها (مانند بخشی از روده) برداشته شوند. جراح همچنین ممکن است تومورهایی را که در سایر نقاط شکم مانند کبد گسترش یافته اند، حذف کند.
گزینه دیگر برای تومورهایی که بزرگ هستند یا در نواحی مجاور رشد کرده اند ممکن است این باشد که ابتدا داروی هدفمند ایماتینیب (Gleevec) را معمولاً حداقل برای چند ماه مصرف کنید. این روش درمان نئوادجوانت (neoadjuvant treatment) نامیده میشود و اغلب میتواند تومور را کوچک کرده و برداشتن آن را با جراحی آسانتر کند.
جراحی برای GIST متاستاتیک
جراحی یک درمان رایج برای GIST که به سایر قسمتهای بدن گسترش یافته (متاستاز) نیست. داروهای درمان هدفمند معمولاً اولین گزینه برای GIST متاستاتیک هستند. اما اگر بیش از چند تومور متاستاتیک وجود نداشته باشد و آنها به خوبی به درمان هدفمند پاسخ دهند، ممکن است برخی از پزشکان جراحی را برای برداشتن آنها توصیه کنند.
هیچ مطالعه بزرگی برای نشان دادن این که اسن روش چقدر مفید است انجام نشده است اما ممکن است یک گزینه باشد. اگر پزشک شما این جراحی را پیشنهاد میدهد، مطمئن شوید که اهداف و عوارض جانبی احتمالی را درک کرده اید.
اگر تومورها در کبد هستند و برداشتن آنها سخت است، گزینههای دیگر ممکن است شامل انواع مختلف درمانهای موضعی مانند فرسایش (ablation) یا آمبولیزاسیون (embolization) باشد.
انتخاب جراح خود
مهم نیست که چه نوع جراحی انجام میشود، بسیار مهم است که توسط یک جراح با تجربه در درمان GIST انجام شود. GISTها اغلب تومورهای ظریفی هستند و جراحان باید مراقب باشند که پوشش بیرونی اطراف آنها را باز نکنند (معروف به کپسول)، زیرا این کار ممکن است خطر گسترش سرطان را افزایش دهد. GISTها همچنین تمایل دارند رگهای خونی زیادی داشته باشند، بنابراین جراح شما باید مراقب باشد که خونریزی از تومور را کنترل کند.
درمان دارویی هدفمند (Targeted Drug Therapy) برای تومورهای استرومال دستگاه گوارش
برخی از داروها میتوانند پروتئینهای خاصی را در سلولهای تومور استرومال دستگاه گوارش (GIST) هدف قرار دهند که به تقسیم و رشد آنها کمک میکند. این داروهای هدفمند (که گاهی اوقات داروهای دقیق یا precision drugs نامیده میشوند) اغلب در درمان GIST بسیار مفید هستند. آنها متفاوت از داروهای استاندارد شیمی درمانی (chemo) عمل میکنند که معمولاً مفید نیستند.
داروهای هدفمند مورد استفاده برای درمان GIST، مهار کنندههای تیروزین کیناز (tyrosine kinase inhibitors یا TKIs) نامیده میشوند زیرا آنها پروتئینهای تیروزین کیناز مانند KIT و PDGFRA را هدف قرار میدهند.
همه این داروهای هدفمند به صورت قرص معمولاً یک بار در روز مصرف میشوند.
ایماتینیب (Gleevec)
این دارو برای درمان اکثر افراد مبتلا به GIST در برخی موارد استفاده میشود. تومورها را میتوان برای یافتن جهشهای خاصی در ژنهای KIT و PDGFRA قبل از درمان آزمایش کرد که این کار میتواند کمک کند که چقدر احتمال دارد که ایماتینیب مفید باشد. این دارو هر دو پروتئین KIT و PDGFRA را هدف قرار میدهد و توانایی آنها را برای کمک به رشد و تقسیم سلولهای تومور مسدود میکند. در اکثر GISTها، سلولها بیش از حد یکی از این پروتئینها را دارند.
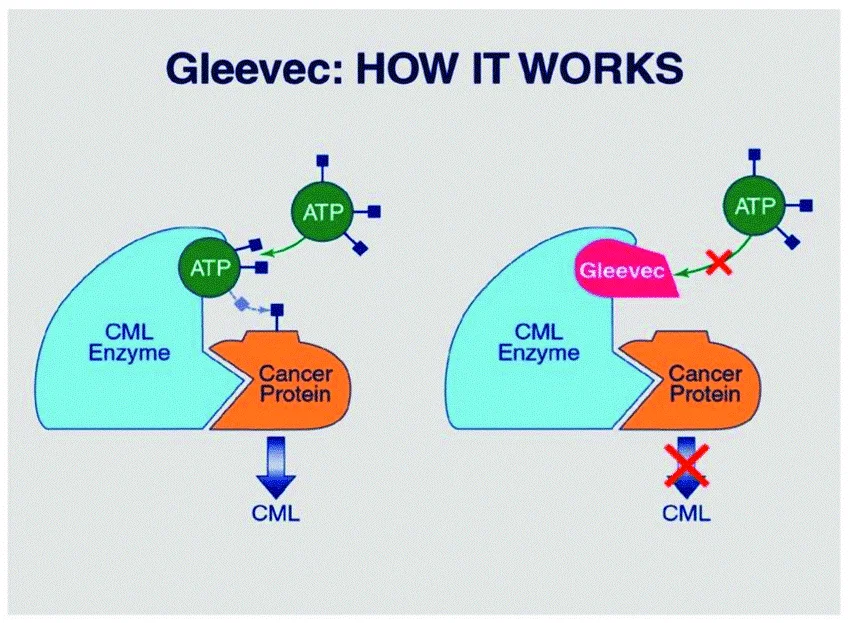
اکثر GISTها هنگام درمان با ایماتینیب کوچک میشوند. برخی دیگر از تومورها حداقل برای مدتی رشد نمیکنند. تعداد کمی از تومورها با این درمان تغییری نمیکنند.
Imatinib میتواند در شرایط مختلف مفید باشد:
اگر GIST به طور کامل توسط جراحی برداشته شده باشد، پزشکان معمولاً مصرف ایماتینیب را برای حداقل یک سال پس از آن توصیه میکنند (مگر اینکه خطر عود سرطان کم باشد). این روش به عنوان درمان کمکی (adjuvant therapy) شناخته میشود. بسیاری از پزشکان در حال حاضر حداقل 3 سال پس از جراحی ایماتینیب را برای بیمارانی که خطر بازگشت تومورهای خود را دارند (بر اساس اندازه تومور، محل و میزان میتوزی) توصیه میکنند.
برای تومورهای بزرگتر که ممکن است برداشتن آنها سخت باشد، ابتدا ایماتینیب ممکن است برای کوچک کردن تومور و تسهیل جراحی استفاده شود. این به عنوان درمان نئوادجوانت شناخته میشود. ایماتینیب اغلب پس از جراحی نیز مجدداً تجویز میشود (معمولاً حداقل برای 2 سال).
ایماتینیب معمولاً درمان انتخابی برای GISTهای پیشرفته است که بیش از حد گسترش یافته اند و با جراحی قابل برداشتن نیستند. اگرچه بعید است که این روش این تومورها را درمان کند اما اغلب میتواند رشد آنها را برای چندین سال کاهش دهد یا کند کند و به افراد کمک کند تا عمر طولانیتری داشته و احساس بهتری داشته باشند. اگر مصرف دارو متوقف شود و تومور دوباره شروع به رشد کند، افزایش دوز ایماتینیب ممکن است به کند کردن رشد برای مدتی کمک کند اما دوزهای بالاتر نیز میتواند عوارض جانبی بیشتری داشته باشد.
عوارض جانبی ایماتینیب میتواند شامل ناراحتی خفیف معده، اسهال، درد عضلانی و زوائد پوستی باشد. اگر دارو همراه با غذا مصرف شود، ناراحتی معده کاهش مییابد. ایماتینیب همچنین میتواند باعث حفظ مایعات در افراد شود.
اغلب این حالت باعث ایجاد مقداری تورم در صورت (دور چشم) یا در مچ پا میشود. این دارو به ندرت میتواند باعث مشکلات شدیدتر مانند تجمع مایع در ریهها یا شکم شود. همچنین میتواند بر عملکرد قلب در برخی افراد نیز تأثیر بگذارد.
یک نگرانی دیگر هنگام استفاده از این دارو برای درمان GISTهای بزرگ این است که این تومورها اغلب رگهای خونی شکننده زیادی دارند. اگر ایماتینیب باعث کوچک شدن سریع تومور شود، میتواند منجر به خونریزی داخلی شود. به همین دلیل، پزشکان در اولین دوره شروع مصرف این دارو، بیماران را با دقت زیر نظر دارند.
سونیتینیب (Sutent)
اگر ایماتینیب دیگر کار نمیکند یا اگر فردی به دلایلی نتواند ایماتینیب را مصرف کند، این دارو میتواند در درمان GIST مفید باشد.
Sunitinib پروتئینهای KIT و PDGFRA و همچنین چندین پروتئین دیگر را که ایماتینیب هدف قرار نمیدهد، هدف قرار میدهد.
Sunitinib معمولاً با کوچک کردن یا کند کردن رشد تومور به برخی افراد کمک میکند. این اتفاق ممکن است به برخی از افراد کمک کند تا عمر طولانی تری داشته باشند.
عوارض جانبی رایج سانیتینیب شامل خستگی، حالت تهوع، اسهال، تحریک دهان و تغییر رنگ پوست و مو است. عوارض جانبی جدی تر میتواند شامل فشار خون بالا، افزایش خطر خونریزی، تورم، مشکلات قلبی و مشکلات جدی کبدی باشد.
Regorafenib (Stivarga)
اگر ایماتینیب و سونیتینیب کار خود را متوقف کنند یا اگر فرد به دلایلی نتواند این داروها را مصرف کند، میتوان از Regorafenib برای درمان GISTهای پیشرفته استفاده کرد. این دارو پروتئینهای زیادی از جمله KIT و PDGFRA را هدف قرار میدهد.
Regorafenib میتواند رشد تومور را کاهش دهد و حتی برخی از تومورها را کوچک کند، اگرچه مشخص نیست که آیا میتواند به افراد کمک کند تا عمر طولانی تری داشته باشند یا خیر.
عوارض جانبی رایج رگورافنیب شامل درد شکم، اسهال، احساس خستگی یا ضعف، تحریک دهان یا گلو، تب، کاهش اشتها و کاهش وزن است. عوارض جانبی کمتر شایع اما جدی تر میتواند شامل عفونت، فشار خون بالا، مشکلات قلبی، خونریزی جدی، مشکل در بهبود زخم، ایجاد سوراخ در دیواره معده یا روده، زوائد شدید و مشکلات قرمزی، درد یا حتی تاول کف دست و کف پا (به نام سندرم دست و پا یا hand-foot syndrome) باشد.
ریپرتینیب (Qinlock)

ریپرتینیب معمولاً برای درمان GISTهای پیشرفته استفاده میشود اگر سایر TKIها مانند ایماتینیب، سونیتینیب و رگورافنیب دیگر مفید نباشند یا اگر فرد به دلایلی نتواند این داروها را مصرف کند. این دارو بسیاری از پروتئینهای کیناز از جمله KIT و PDGFRA را هدف قرار میدهد.
ریپرتینیب میتواند رشد تومور را کاهش دهد و حتی برخی از تومورها را کوچک کند، اگرچه هنوز مشخص نیست که آیا میتواند به افراد کمک کند تا عمر طولانیتری داشته باشند یا خیر.
عوارض جانبی رایج ریپرتینیب میتواند شامل ریزش مو، حالت تهوع و استفراغ، از دست دادن اشتها، اسهال یا یبوست، احساس خستگی و درد عضلانی یا شکم باشد. عوارض جانبی کمتر شایع اما جدیتر میتواند شامل فشار خون بالا، افزایش خطر ابتلا به سرطانهای جدید پوست، مشکلات قلبی، مشکل در بهبود زخم و مشکلات قرمزی، درد یا حتی تاول زدن کف دستها و کف پا باشد. (به نام سندرم دست و پا)
آواپریتینیب (Ayvakit)
این TKI دیگری است که PDGFRA و KIT و همچنین چندین پروتئین دیگر را هدف قرار میدهد.
Avapritinib عمدتا برای درمان GISTهای پیشرفته استفاده میشود که سلولهای آنها دارای تغییر در ژن PDGFRA هستند که به عنوان جهش اگزون 18 شناخته میشود. این سرطانها معمولاً به درمان با TKIهای بالا پاسخ خوبی نمیدهند.
عوارض جانبی رایج آوپریتینیب میتواند شامل تورم یا احتباس مایعات، خستگی، تهوع و استفراغ، از دست دادن اشتها، اسهال یا یبوست، افزایش اشک در چشمها، تغییر رنگ مو، درد شکم، زوائد پوستی و سرگیجه باشد.
عوارض جانبی جدی تر میتواند شامل خونریزی در مغز و همچنین اثرات سیستم عصبی مرکزی (central nervous system یا CNS) باشد، مانند:
- فراموشی
- گیجی
- مشکل در فکر کردن
- خواب آلودگی
- مشکل خواب
- توهمات
- تغییر در خلق و خو یا رفتار
سایر مهار کنندههای تیروزین کیناز
چندین TKI دیگر در حال حاضر برای استفاده علیه GIST نیز در حال مطالعه هستند. در حالی که شواهد محدودی در مورد میزان مفید بودن آنها وجود دارد، برخی از TKIهایی که در صورت عدم کارایی موارد ذکر شده در بالا ممکن است گزینه مناسبی باشند، عبارتند از:
- سورافنیب (Nexavar)
- نیلوتینیب (Tasigna)
- داساتینیب (Sprycel)
- پازوپانیب (Votrient)
از آن جایی که دقیقاً مشخص نیست که این و سایر TKIها تا چه حد در برابر GIST کار میکنند، شرکت در یک کارآزمایی بالینی که مطالعه آنها را انجام میدهد ممکن است گزینه خوبی باشد.
فرسایش و آمبولیزاسیون برای درمان تومورهای استرومال دستگاه گوارش
اگر یک تومور استرومال گوارشی (GIST) به کبد گسترش یافته باشد، ممکن است از درمانهایی مانند فرسایش و آمبولیزاسیون استفاده شود، به ویژه اگر جراحی برای برداشتن تومورها انجام نشود.
فرسایش (Ablation)
فرسایش تخریب تومورها با استفاده از گرما یا سرمای شدید یا با استفاده از مواد شیمیایی است. گاهی اوقات میتوان از آن برای از بین بردن GISTهایی که به صورت چند تومور کوچک در کبد گسترش یافته اند استفاده کرد. از آن جایی که فرسایش اغلب، برخی از بافتهای طبیعی اطراف تومور را از بین میبرد، ممکن است برای درمان تومورها در نزدیکی ساختارهای مهم مانند رگهای خونی اصلی، دیافراگم (عضله تنفسی نازک بالای کبد) یا مجاری اصلی در کبد انتخاب خوبی نباشد.
چندین نوع فرسایش وجود دارد:
- فرسایش با فرکانس رادیویی (RFA یا Radiofrequency ablation) که از امواج رادیویی با انرژی بالا برای گرم کردن تومور و از بین بردن سلولهای سرطانی استفاده میکند.
- فرسایش اتانول (الکل) که در آن الکل غلیظ به طور مستقیم به تومور تزریق میشود تا سلولهای سرطانی را بکشد.
- حرارت درمانی با مایکروویو (Microwave thermotherapy) که در آن امواج مایکروویو منتقل شده از طریق یک پروب قرار داده شده در تومور برای گرم کردن و تخریب سلولهای سرطانی استفاده میشود.
- کرایوسرجری (کرایوتراپی یا cryotherapy) که تومور را با انجماد با استفاده از یک پروب فلزی نازک از بین میبرد. این روش گاهی نیاز به بیهوشی عمومی دارد (شما در خواب عمیق هستید و نمیتوانید درد را احساس کنید).
چیزهایی که باید انتظارشان را داشته باشید:
معمولاً برای این نوع درمان نیازی نیست یک شب در بیمارستان بمانید. فرسایش اغلب میتواند بدون جراحی با وارد کردن یک سوزن یا پروب به داخل تومور از طریق پوست انجام شود. سوزن یا پروب با سونوگرافی یا سی تی اسکن به جای خود هدایت میشود. این کار ممکن است با بیهوشی عمومی (شما در خواب عمیق هستید) یا با آرام بخش (بیدار هستید اما خواب آلود هستید و نباید دردی احساس کنید) انجام شود. اما گاهی اوقات، برای اطمینان از اینکه درمان در مکان مناسب انجام میشود، این کار در حین جراحی انجام میشود.
عوارض جانبی احتمالی فرسایش
عوارض جانبی احتمالی پس از درمان فرسایش شامل درد شکم (abdominal)، عفونت در کبد و خونریزی در حفره قفسه سینه یا شکم است. عوارض جدی غیر معمول هستند اما ممکن است رخ دهند.
آمبولیزاسیون (Embolization)
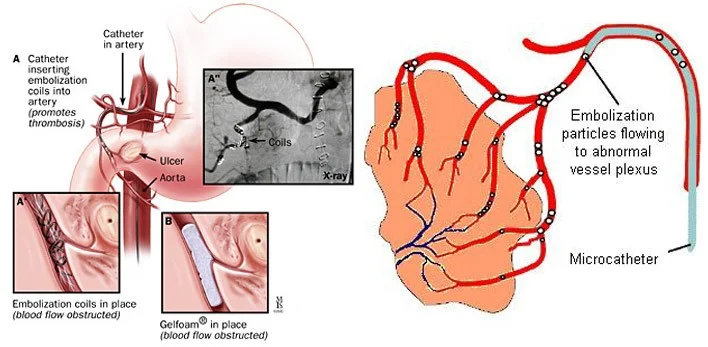
آمبولیزاسیون روشی است که در آن پزشک موادی را برای مسدود کردن یا کاهش جریان خون به سلولهای سرطانی در کبد تزریق میکند.
کبد از این جهت غیر عادی است که 2 منبع خون دارد. بیشتر سلولهای طبیعی کبد از شاخههای ورید باب (portal vein) تغذیه میشوند، در حالی که سلولهای سرطانی در کبد معمولاً از شاخههای شریان کبدی (hepatic artery) تغذیه میشوند. مسدود کردن شاخه شریان کبدی تغذیه کننده تومور به از بین بردن سلولهای سرطانی کمک میکند اما بیشتر سلولهای سالم کبد را بدون آسیب میگذارد زیرا خون خود را از ورید باب دریافت میکنند.
آمبولیزاسیون مقداری از خون رسانی به بافت طبیعی کبد را کاهش میدهد، بنابراین ممکن است برای برخی از بیمارانی که کبدشان قبلاً توسط بیماریهایی مانند هپاتیت (hepatitis) یا سیروز (cirrhosis) آسیب دیده است، گزینه خوبی نباشد.
چیزهایی که باید انتظارشان را داشته باشید:
نوع اصلی آمبولیزاسیون مورد استفاده برای درمان GISTهایی که به کبد گسترش یافته اند، آمبولیزاسیون شریانی یا arterial embolization است (همچنین به عنوان آمبولیزاسیون ترانس شریانی یا TAE شناخته میشود).
در این روش، یک کاتتر (catheter، یک لوله نازک و انعطاف پذیر) از طریق یک برش کوچک در قسمت داخلی ران وارد یک سرخرگ میشود و به داخل شریان کبدی در کبد میرود. معمولاً در این زمان رنگی به جریان خون تزریق میشود تا به پزشک کمک کند مسیر کاتتر را از طریق آنژیوگرافی (angiography) که نوع خاصی از اشعه ایکس است، ببیند. هنگامی که کاتتر در جای خود قرار گرفت، ذرات کوچک به شریان تزریق میشود تا آن را مسدود کند.
آمبولیزاسیون همچنین میتواند با تزریق کرههای رادیو اکتیو کوچک به شریان کبدی (رادیوامبولیزاسیون یا radioembolization) یا با دادن شیمی درمانی مستقیم به شریان درست قبل از وصل کردن آن (شیمی آمبولیزاسیون یا chemoembolization) انجام شود. اما مشخص نیست که هر یک از این تکنیکها بهتر از TAE باشد.
این روش ممکن است با بیهوشی عمومی (حالتی که در خواب عمیق هستید) یا با آرام بخشی آگاهانه (حالتی که بیدار اما خواب آلود هستید و نباید دردی احساس کنید) انجام شود. به طور معمول، برای انجام عمل آمبولیزاسیون لازم نیست یک شب در بیمارستان بمانید.
عوارض جانبی احتمالی آمبولیزاسیون
عوارض احتمالی پس از آمبولیزاسیون شامل درد شکم (belly)، تب، تهوع، عفونت در کبد، التهاب کیسه صفرا و لخته شدن خون در رگهای خونی اصلی کبد است. از آن جایی که بافت سالم کبد میتواند تحت تأثیر قرار گیرد، این خطر وجود دارد که عملکرد کبد پس از روند درمان بدتر شود. اگر شاخه بزرگی از شریان کبدی آمبولیزه شود، این خطر بیشتر است. عوارض جدی شایع نیستند اما ممکن است رخ دهند.
شیمی درمانی (Chemotherapy) برای تومورهای استرومال دستگاه گوارش
شیمی درمانی (chemo) استفاده از داروها برای درمان سرطان است. اغلب، این داروها به داخل ورید (IV) تزریق میشوند یا به صورت خوراکی تجویز میشوند. آنها وارد جریان خون میشوند و به سراسر بدن میرسند و این روش درمانی به طور بالقوه برای سرطانهایی که فراتر از اندامی که در آن شروع شده اند، مفید است.
هر دارویی که برای درمان سرطان استفاده میشود را میتوان شیمی درمانی در نظر گرفت، حتی داروهای درمانی هدفمند مانند ایماتینیب (Gleevec) که امروزه معمولاً برای درمان تومورهای استرومال دستگاه گوارش (GISTs) استفاده میشوند. اما اصطلاح شیمی درمانی به طور کلی برای توصیف داروهای خاصی استفاده میشود که با حمله به سلولهای در حال رشد سریع در هر نقطه از بدن، از جمله سلولهای سرطانی، کار میکنند.
قبل از اینکه مشخص شود داروهای درمانی هدفمند در درمان GIST مفید هستند، داروهای شیمی درمانی سنتی اغلب آزمایش میشدند. اما GISTها به ندرت در پاسخ به این داروها کوچک میشوند، بنابراین شیمی درمانی سنتی امروزه به ندرت استفاده میشود. افرادی که به شیمی درمانی فکر میکنند ممکن است بخواهند در مورد شرکت در یک کار آزمایی بالینی فکر کنند.
عوارض جانبی احتمالی
داروهای شیمی درمانی میتوانند عوارض جانبی ایجاد کنند. اینها به داروهای خاص مورد استفاده، دوز آنها و مدت زمان مصرف آنها بستگی دارد. عوارض جانبی رایج شیمی درمانی عبارتند از:
- تهوع و استفراغ
- از دست دادن اشتها
- زخمهای دهانی
- اسهال
- ریزش مو
- افزایش احتمال عفونت (به دلیل کمبود گلبولهای سفید)
- مشکلات خونریزی یا کبودی (به دلیل کمبود پلاکت خون)
- خستگی یا تنگی نفس (در اثر کمبود گلبولهای قرمز)
در کنار خطرات فوق، برخی از داروهای شیمی درمانی میتوانند عوارض جانبی دیگری نیز ایجاد کنند.
از تیم مراقبتهای بهداشتی و پزشکی خود بپرسید که بر اساس داروهای خاصی که دریافت میکنید چه عوارض جانبی میتوانید داشته باشید. در صورت داشتن عوارض جانبی حتماً به پزشک یا پرستار خود اطلاع دهید زیرا اغلب راههایی برای کمک به آنها وجود دارد. به عنوان مثال، میتوان داروهایی برای کمک به پیشگیری یا کاهش تهوع و استفراغ تجویز کرد.
پرتو درمانی (Radiation therapy) برای تومورهای استرومال دستگاه گوارش
پرتو درمانی استفاده از اشعه ایکس (یا ذرات) با انرژی بالا برای از بین بردن سلولهای سرطانی است. پرتو درمانی برای درمان تومورهای استرومال دستگاه گوارش (GIST) چندان مفید نیست، بنابراین اغلب از آن استفاده نمیشود. اما گاهی اوقات میتوان از آن برای تسکین علائمی مانند درد استخوان استفاده کرد.
قبل از شروع دوره درمان، تیم پرتو اندازی اندازه گیریهای دقیقی را برای یافتن زوایای صحیح برای نشانه گیری پرتوها و دوز مناسب تابش انجام میدهد. این جلسه برنامه ریزی که شبیه سازی (simulation) نامیده میشود، معمولا شامل انجام تستهای تصویر برداری مانند اسکن سی تی یا ام آر آی است.
پرتو درمانی بسیار شبیه عکس برداری با اشعه ایکس است اما پرتو درمانی بسیار قوی تر است. خود روند درمان بدون درد است. این کار فقط چند دقیقه طول میکشد، اگرچه زمان تنظیم – قرار دادن شما در وضعیت مناسب برای روند درمان – معمولاً بیشتر طول میکشد. ممکن است چندین روز متوالی تحت پرتو درمانی قرار بگیرید.
عوارض جانبی احتمالی پرتو درمانی
بسته به اینکه پرتو در کجا هدف قرار میگیرد، عوارض جانبی ممکن است شامل موارد زیر باشد:
- تغییرات پوستی در نواحی تحت تابش، از قرمزی تا تاول و پوسته پوسته شدن
- تهوع و استفراغ
- اسهال
- خستگی
- شمارش خون پایین
اکثر عوارض جانبی مدت کوتاهی پس از پایان روند درمان از بین میروند، اگرچه خستگی و تغییرات پوستی ممکن است مدت بیشتری طول بکشد. با پزشک خود در مورد عوارض جانبی احتمالی و راههای کاهش یا تسکین آنها صحبت کنید.
گزینههای درمانی معمول برای تومورهای استرومال دستگاه گوارش
درمان تومورهای استرومال دستگاه گوارش (GISTs) عمدتاً به عواملی مانند موارد زیر وابسته است:
اگر بتوان تومور را با جراحی برداشت (حذف کرد) که بر اساس اندازه تومور، محل قرارگیری و میزان گسترش آن است.
سرعت رشد تومور (سرعت میتوزی آن)
اگر سلولهای تومور دارای جهشهای ژنی خاصی باشند
خطر بازگشت تومور پس از دوره درمان
عوامل دیگری مانند سن و سلامت کلی فرد نیز میتواند مهم باشد.
تومورهای موضعی کوچک تر (قابل برداشت یا resectable)
بیشتر GISTهای کوچک نیاز به درمان دارند. اما برخی از تومورهای بسیار کوچک (با عرض کمتر از 2 سانتی متر) که هیچ علامتی ایجاد نمیکنند، ممکن است هرگز آن قدر رشد نکنند که مشکلی ایجاد کنند. یک گزینه برای چنین توموری ممکن است این باشد که آن را با دقت مشاهده کرده و با آندوسکوپی در فواصل زمانی منظم، مثلا یک یا دو بار در سال بررسی کنید. تا زمانی که تومور رشد نمیکند، ممکن است نیازی به دوره درمانی بیشتری نداشته باشید.
جراحی روش درمانی اصلی برای اکثر تومورهای کوچک دیگر است. نیاز به درمان بیشتر پس از جراحی به خطر بازگشت GIST بستگی دارد.
تومورهایی که کوچک هستند و به سرعت رشد نمیکنند، معمولاً خطر بازگشت کمی دارند، بنابراین اغلب نیازی به درمان بیشتر نیست.
خطر بازگشت GIST پس از جراحی بیشتر است اگر:
- تومور بزرگتر است
- از معده شروع نشده است
- سلولهای سرطانی به سرعت در حال تقسیم شدن هستند (میزان میتوزی بالایی دارند)
اگر پزشک بر اساس این عوامل فکر میکند که سرطان دارای خطر متوسط یا زیاد بازگشت است، درمان کمکی با داروی هدفمند ایماتینیب (Gleevec) معمولاً حداقل برای یک سال پس از جراحی توصیه میشود. اکنون بسیاری از پزشکان برای تومورهایی که احتمال بازگشت آنها زیاد است، حداقل 3 سال ایماتینیب را توصیه میکنند.
پزشک احتمالاً قبل از تجویز ایماتینیب، سلولهای تومور را برای یافتن تغییرات خاصی در ژنهای KIT و PDGFRA آزمایش میکند. این به این دلیل است که ایماتینیب احتمالاً برای تومورهایی که یکی از این تغییرات ژنی را ندارند، مفید نیست.
تومورهای موضعی بزرگ تر (در حاشیه قابل برداشت یا marginally resectable)
تومورهایی که بزرگ تر هستند یا در مکانهایی قرار دارند که برداشتن (رزکت) آنها را سخت تر میکند ممکن است به جراحی گسترده تری نیاز داشته باشند که میتواند در کوتاه مدت و بعداً مشکلات سلامتی ایجاد کند. به همین دلیل، جراحی معمولا اولین روش درمانی نیست.
درمان با داروی هدفمند ایماتینیب (Gleevec) معمولاً ابتدا برای کوچک کردن تومور انجام میشود. اما قبل از شروع روند درمان، مهم است که مطمئن شوید که تومور در واقع یک GIST است، بنابراین بیوپسی مورد نیاز است. به عنوان بخشی از آزمایش نمونه بیوپسی، سلولهای تومور معمولاً برای تغییرات خاصی در ژنهای KIT و PDGFRA بررسی میشوند. این به این دلیل است که ایماتینیب احتمالاً برای تومورهایی که یکی از این تغییرات ژنی را ندارند، مفید نیست. اگر ایماتینیب داده میشود، حداقل تا زمانی که کوچک شدن تومور متوقف شود، ادامه مییابد.
اگر تومور به اندازه کافی کوچک شود، در صورتی که پزشک فکر میکند که میتوان آن را با خیال راحت برداشت، ممکن است جراحی انجام شود. ایماتینیب احتمالاً پس از جراحی ادامه خواهد یافت تا به کاهش احتمال بازگشت سرطان کمک کند.
اگر تومور به اندازه کافی کوچک نشود که عمل جراحی را ممکن کند، ایماتینیب اغلب تا زمانی که به نظر میرسد کمک کننده است، ادامه مییابد. اگر این دارو دیگر عمل نمیکند، گاهی اوقات افزایش دوز میتواند مفید باشد. در غیر این صورت یا اگر عوارض جانبی خیلی شدید باشد، ممکن است به جای آن داروی هدفمند دیگری مانند سونیتینیب (Sutent) استفاده شود. اگر سونیتینیب نیز دیگر کار نمیکند، regorafenib (Stivarga) ممکن است به برخی افراد کمک کند. اگر این دارو نیز دیگر کار نمیکند، ریپرتینیب (Qinlock) ممکن است مفید باشد.
تومورهایی که قابل جابجایی نیستند یا به نقاط دور گسترش یافته اند (تومورهای غیر قابل برداشت یا unresectable tumors)
گزینههای درمانی برای GISTهای غیر قابل برداشت بستگی به این دارد که چرا قابل برداشت نیستند و اگر گسترش یافته اند، میزان گسترش آنها چقدر است.
جراحی معمولاً اولین روش درمانی برای این تومورها نیست، بنابراین قبل از شروع درمان، تأیید اینکه تومور در واقع یک GIST است با بیوپسی، مهم است.
داروی هدفمند ایماتینیب (Gleevec) معمولاً اولین روش درمانی ارجح برای اکثر GISTهای پیشرفته است. (در صورتی که سلولهای سرطانی تغییرات خاصی در ژن PDGFRA داشته باشند، ممکن است داروی هدفمند آواپریتینیب (Ayvakit) به جای آن استفاده شود.) به عنوان بخشی از آزمایش نمونه بیوپسی، سلولهای تومور ممکن است برای تغییرات خاصی در ژنهای KIT و PDGFRA بررسی شوند. این کار میتواند ایده ای در مورد اینکه چقدر احتمال دارد که ایماتینیب (یا آواپریتینیب) مفید باشد، ارائه دهد.
اگر ایماتینیب استفاده شود، تا زمانی که تومور رشد نکند (و عوارض جانبی قابل تحمل باشد) ادامه مییابد. اگر تومور دوباره شروع به رشد کند، ممکن است به افزایش دوز ایماتینیب پاسخ دهد. در غیر این صورت یا اگر عوارض جانبی ایماتینیب خیلی شدید باشد، تغییر به سونیتینیب (Sutent) ممکن است مفید باشد. اگر سونیتینیب دیگر کار نمیکند، regorafenib (Stivarga) ممکن است به برخی افراد کمک کند. اگر regorafenib نیز دیگر مفید نیست، ریپرتینیب (Qinlock) ممکن است یک گزینه باشد.
اگر تومور با درمان هدفمند به اندازه کافی کوچک شود، جراحی ممکن است برای برخی افراد یک گزینه باشد. اگر هنوز مؤثر باشد، ممکن است درمان هدفمندتری دنبال شود.
اگر سرطان تنها به 1 یا 2 محل در شکم (مانند کبد) گسترش یافته باشد، پزشک ممکن است تومور اصلی را برداشته و سعی کند این تومورهای دیگر را نیز خارج کند. در این صورت، حتماً با پزشک خود در مورد اهداف درمان (خواه تلاش برای درمان سرطان، کمک به طول عمر بیشتر یا پیشگیری یا کاهش علائم) و همچنین مزایا و خطرات احتمالی آن صحبت کنید.
گزینههای دیگر برای درمان سرطانهایی که به کبد گسترش یافته اند عبارتند از: فرسایش و آمبولیزاسیون برای از بین بردن این تومورها.
درمان سرطانهایی که دیگر به داروهای هدفمند مورد بحث در بالا پاسخ نمیدهند، میتواند سخت باشد. برخی از پزشکان ممکن است استفاده از داروهای هدفمند دیگر مانند سورافنیب (Nexavar)، داساتینیب (Sprycel)، نیلوتینیب (Tasigna) یا پازوپانیب (Votrient) را توصیه کنند، اگرچه هنوز مشخص نیست که این داروها چقدر مفید هستند.
داروهای شیمی درمانی استاندارد معمولاً چندان مؤثر نیستند. شرکت در کار آزمایی بالینی یک روش درمانی جدیدتر ممکن است گزینه خوبی برای برخی افراد باشد.
تومورهای عود کننده (Recurrent tumors)
هنگامی که سرطان پس از روند درمان عود میکند، عود (recurrence) نامیده میشود. اگر سرطان در محلی که در آن شروع شده یا نزدیک آن عود کند (بازگردد)، به آن عود موضعی (local recurrence) میگویند. اگر در نقاط دیگر (مانند ریهها یا کبد) عود کند، عود دور (distant recurrence) نامیده میشود. گزینههای درمانی برای GISTهای مکرره (عود کننده) به محل و میزان عود بستگی دارد.
برای اکثر موارد عود، درمان با داروی هدفمند ایماتینیب (Gleevec) اغلب اولین گزینه برای کوچک کردن تومورها است، تا زمانی که هنوز موثر باشد و بیمار بتواند مصرف آن را تحمل کند. اگر دوز اولیه ایماتینیب مؤثر نبود، میتوان دوز را افزایش داد. گزینه دیگر این است که سایر داروهای هدفمند مانند سونیتینیب (Sutent)، رگورافنیب (Stivarga) یا ریپرتینیب (Qinlock) را امتحان کنید.
اگر سرطان به صورت یک یا چند تومور کاملاً مشخص بازگشت کند، برداشتن یا از بین بردن تومور ممکن است یک گزینه باشد. پزشکان هنوز مطمئن نیستند که آیا حذف GIST که پس از درمان عود میکنند به افراد کمک میکند تا عمر طولانیتری داشته باشند، بنابراین مهم است که در مورد خطرات و مزایای این روش درمانی با پزشک و خانواده خود صحبت کنید.
پرتو درمانی همچنین ممکن است گزینه ای برای کمک به درمان علائمی مانند درد، به ویژه در تومورهای استخوانی باشد.
اگر داروهای هدفمند ذکر شده در بالا دیگر مفید نباشند، برخی از پزشکان ممکن است استفاده از داروهای هدفمند دیگر مانند سورافنیب (Nexavar)، داساتینیب (Sprycel)، nilotinib (Tasigna) یا pazopanib (Votrient) را توصیه کنند، اگرچه هنوز مشخص نیست که این داروها چقدر مفید هستند.
از آن جایی که درمان این سرطانها اغلب سخت است، ممکن است بخواهید در آزمایشات بالینی روشهای درمانی جدیدتر نیز شرکت کنید.
همچنین بخوانید:
- مزوتلیومای بدخیم چیست؟ تعریف، علائم، پیشگیری و درمان
- تومورهای کارسینوئید ریه چیست؟ انواع، علائم و درمان
- تومور ویلمز چیست؟ انواع، علائم، درمان
- سارکوم رحم (Uterine Sarcoma) چیست؟
- تومور کارسینوئید دستگاه گوارش چیست؟ علائم، پیشگیری و درمان
مترجم: فاطمه فریادرس




در مورد گزارش و نتیجه بیوپسی کبد سوال داشتم
به پزشک مراجعه کنید
آیا ممکن است این نوع تومور متاستاز کند و اینکه چقدر طول میکشد تا علائم آن بروز کند؟
تومورهای GIST میتوانند متاستاز دهند و علائم آنها ممکن است بسته به اندازه، محل و نرخ رشد تومور متفاوت باشد. بروز علائم ممکن است از چند ماه تا چند سال طول بکشد. تشخیص زودهنگام و مدیریت مناسب این تومورها میتواند به بهبود پیشآگهی کمک کند. در صورت شک به GIST یا علائم مرتبط با آن، مراجعه به متخصص گوارش یا انکولوژیست توصیه میشود.
سلام.من یک توده شکمی دارم. تو سیتی اسکن آیا مشخص میشه gist هست. یعنی بدخیم بودن تو سیتی اسکن مسخص میشه یا حتما برای بدخیم بودن باید به پاتولوژی برده بشه… ممنونم
به پزشک مراجعه کنید