تکثیر ایزوترمال با واسطه حلقه یا تکنیک LAMP چیست؟
تکثیر ایزوترمال با واسطه حلقه (LAMP) بهعنوان روشی برجسته برای تکثیر DNA ظهور پیدا کرده است و جایگزینی قوی برای تکنیکهای سنتی PCR به شمار میرود. LAMP که در سال ۲۰۰۰ توسط گروهی به سرپرستی نوتومی و همکارانش توسعه یافت، به دلیل سادگی و کارآمدی، انقلابی در زمینه تشخیص مولکولی ایجاد کرده است. این بررسی جامع، با کاوش در توسعه تاریخی، اصول اساسی، کاربردهای گسترده و ویژگیهای فنی LAMP، به پیچیدگیهای این روش میپردازد و عواملی را که باعث میشود LAMP به روشی ترجیحی در زمینههای علمی مختلف تبدیل شود، بررسی میکند.
پیشینه و توسعه تاریخی
ریشهها و تکامل
- شروع به کار: روش LAMP توسط T. Notomi و تیمش پیشگامان شد و اولین بار در مقاله برجسته آنها در سال ۲۰۰۰ در مجله «تحقیقات اسیدهای نوکلئیک» مستندسازی شد. انگیزه اصلی این توسعه، نیاز به روشی سادهتر و مقرونبهصرفهتر برای تکثیر DNA بود که بتواند در خارج از آزمایشگاههای مجهز قابل دسترس باشد.
- پیشرفتهای تکنولوژیکی: LAMP در طول سالها برای طیف وسیعی از کاربردها اصلاح و تطبیق داده شده است. نوآوریهایی مانند پایش لحظهای فرآیند تکثیر و ادغام دستگاههای قابل حمل، قابلیت استفاده و دسترسی آن را گسترش داده است.
اصول بنیادی تکنیک LAMP
مکانیسم عمل
- فرآیند ایزوترمال: LAMP، تکثیر DNA را در دمای ثابت (معمولاً بین ۶۰ تا ۶۵ درجه سانتیگراد) با استفاده از مجموعهای از چهار تا شش پرایمر که به مناطق متمایز DNA هدف متصل میشوند، تسهیل میکند و باعث اختصاصیت و سرعت بالا میشود.
- جایگزینی رشته: برخلاف PCR، LAMP از پلیمرازی با فعالیت جایگزینی رشته بالا استفاده میکند تا نیاز به چرخه حرارتی را برطرف کند. این پلیمراز امکان سنتز سریع رشتههای DNA را فراهم میکند و به طور مداوم DNA تازه سنتز شده را جابجا میکند تا امکان پرایمینگ و تکثیر بیشتر را فراهم کند.
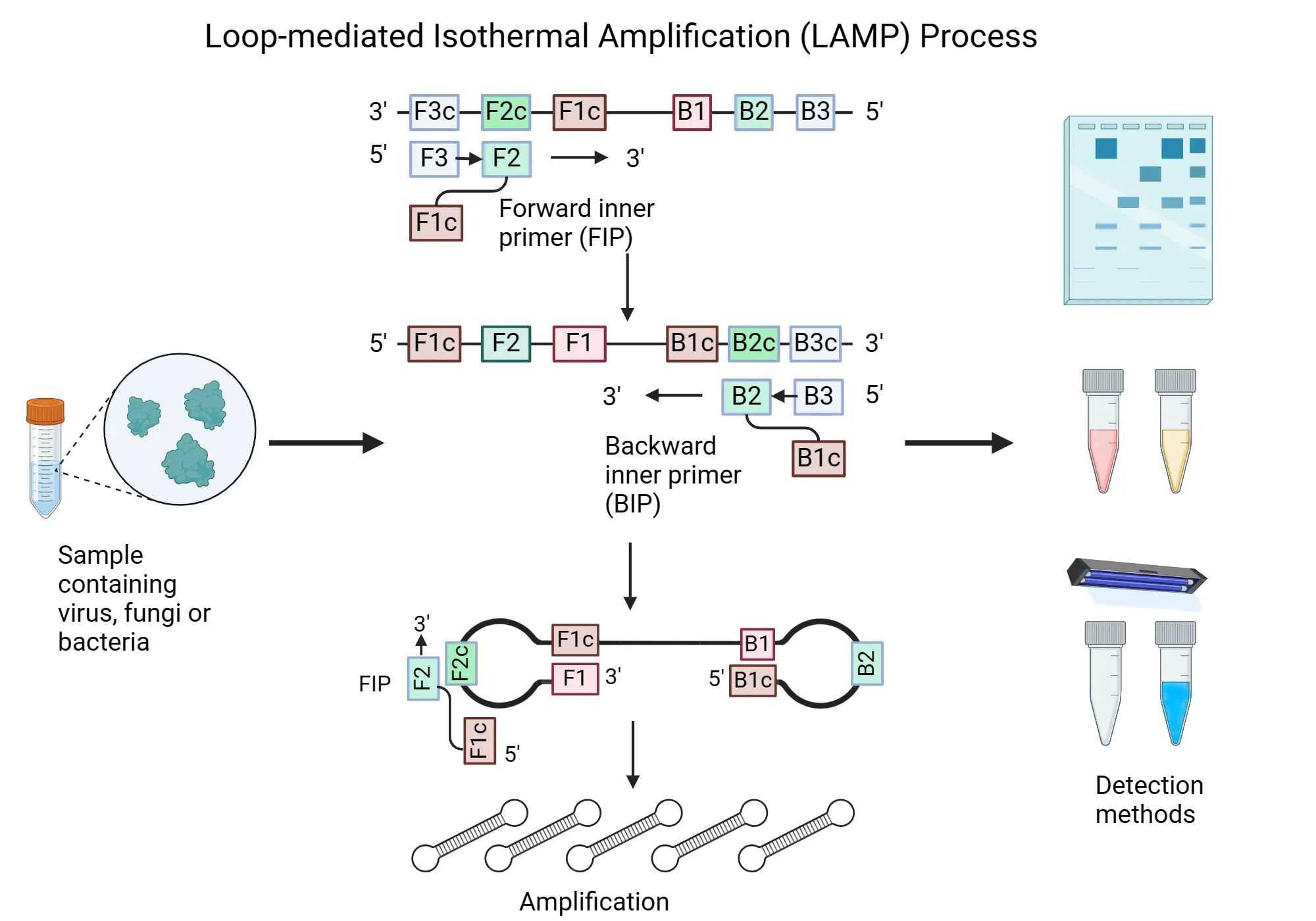
طراحی پرایمر پیچیده
- مجموعههای پرایمر منحصربهفرد: طراحی پرایمر LAMP پیچیده است و شامل دو پرایمر داخلی (FIP و BIP) و دو پرایمر خارجی است که واکنش را آغاز میکنند. پرایمرهای حلقه اختیاری میتوانند با اتصال به ساختارهای حلقهای که در حین تکثیر تشکیل میشوند، واکنش را تسریع کنند.
کاربردهای جامع
تشخیص پزشکی و بالینی
- تشخیص سریع بیماری: LAMP به طور خاص در تشخیص سریع بیماریهای عفونی که نتایج به موقع آن میتواند تأثیر قابل توجهی بر نتایج درمان داشته باشد، مفید واقع شده است.
- بهداشت عمومی: در طول همهگیری کووید-۱۹، آزمایشهای مبتنی بر LAMP برای تشخیص SARS-CoV-2 توسعه یافتهاند که نتایج سریعتری را با دقت قابل مقایسه با آزمایشهای مبتنی بر PCR ارائه میدهند.
کاربردهای کشاورزی و محیط زیستی
- آفتشناسی گیاهی: LAMP برای تشخیص عوامل بیماریزای گیاهی به طور مستقیم در مزرعه به کار گرفته میشود و اتخاذ تصمیمات فوری و آگاهانه در مورد مدیریت محصول را تسهیل میکند.
- حفاظت از حیات وحش: از این روش برای شناسایی گونهها در مطالعات تنوع زیستی و همچنین برای تشخیص عوامل بیماریزا در جمعیتهای حیات وحش استفاده میشود.
جنبههای فنی و نوآوریها
ابزار و تجهیزات
- نیازمندیهای تکنولوژی پایین: نیاز اولیه برای واکنش LAMP یک منبع حرارتی پایدار است که انجام آن را حتی در محیطهای با منابع کم امکانپذیر میکند.
- دستگاههای قابل حمل و زمان واقعی: پیشرفتهای فناوری منجر به توسعه دستگاههای قابل حمل مبتنی بر LAMP شده است که امکان آزمایش میدانی را به همراه قابلیت تجزیه و تحلیل دادههای لحظهای فراهم میکند.
مزایا نسبت به PCR سنتی
- کارآمدی و سرعت: LAMP میتواند در کمتر از یک ساعت نتایج را ارائه دهد که به طور قابل توجهی سریعتر از PCR است.
- بسیار اختصاصی و حساس: تعدد پرایمرهای استفادهشده در LAMP باعث افزایش اختصاصیت و حساسیت آن میشود و احتمال نتایج منفی کاذب را کاهش میدهد.
- مقاومت: LAMP در برابر مهارگرهایی که به طور معمول بر PCR تأثیر میگذارند، مقاومت بیشتری نشان میدهد و آن را برای نمونههای پیچیده مانند خون یا خاک مناسب میسازد.
چالشها و محدودیتها
- خطرات آلودگی: کارایی بالای تکثیر، خطر آلودگی با آئروسل را افزایش میدهد که به کار بستن شیوههای آزمایشگاهی دقیق را ضروری میکند.
- تحلیل کمی: در حالی که نتایج کیفی ساده هستند، کمیتسنجی مقدار DNA هدف در نمونهها همچنان چالشبرانگیز است و در مقایسه با PCR کمی، از دقت کمتری برخوردار است.
چشماندازهای آتی و مسیرهای تحقیقاتی
- ادغام با فناوریهای CRISPR: مطالعات اخیر در حال بررسی ترکیب LAMP با تشخیص مبتنی بر CRISPR برای افزایش اختصاصیت و حساسیت هستند.
- اتوماسیون و ادغام هوش مصنوعی: تلاشها برای خودکارسازی فرآیندهای LAMP و ادغام هوش مصنوعی برای تفسیر نتایج در حال انجام است که به طور بالقوه منجر به انقلابی در تشخیص در محل مراقبت از بیمار میشود.
جدول مقایسه LAMP و PCR
جدولی وجود دارد که LAMP و PCR را از نظر روششناسی، کاربرد، مزایا و محدودیتهای کلیدی آنها مقایسه میکند. لطفاً توجه داشته باشید که این جدول در متن انگلیسی گنجانده شده است. برای حفظ اصالت متن، ترجمه این جدول ضروری نیست.
| ویژگی | LAMP | PCR سنتی |
| اصل اساسی | با استفاده از مجموعه ای از چهار تا شش پرایمر که به طور اختصاصی به DNA هدف متصل می شوند، DNA را با راندمان بالا تکثیر می کند. در شرایط دمای ثابت (ایزوترمال) عمل می کند. | DNA را با چرخه حرارتی از طریق مراحل دناتوراسیون، اتصال و گسترش تکثیر می کند. از دو پرایمر استفاده می کند که به رشته های مقابل DNA هدف متصل می شوند. |
| نیازهای دما | به صورت ایزوترمال عمل می کند، به طور معمول بین 60-65 درجه سانتیگراد. | نیاز به چرخه حرارتی دارد، با دماهایی از 94-98 درجه سانتیگراد برای دناتوراسیون، 50-65 درجه سانتیگراد برای اتصال و 72 درجه سانتیگراد برای گسترش. |
| بازده زمانی | تکثیر سریع، نتایج را می توان در کمتر از یک ساعت به دست آورد. | به طور کلی کندتر است و بسته به پیچیدگی هدف و تنظیم واکنش، تقریباً 2-3 ساعت طول می کشد. |
| پیچیدگی عملکرد | عملکرد ساده با حداقل تجهیزات. مناسب برای استفاده در محیط و آزمایش در محل مراقبت. | نیاز به چرخه حرارتی دارد و آن را برای محیط های آزمایشگاهی مناسب تر می کند. |
| هزینه | به دلیل تجهیزات ساده تر و نیاز به معرفگرهای کمتر، هزینه عملیاتی پایین تری دارد. | به دلیل نیاز به چرخه حرارتی و معرفگرهای مرتبط، بالاتر است. |
| حساسیت و اختصاصیت | به دلیل استفاده از چندین پرایمر که چندین ناحیه از DNA هدف را هدف قرار می دهند، بسیار حساس و اختصاصی است. | بسیار حساس و اختصاصی، اما وابسته به طراحی پرایمر و شرایط واکنش است. |
| خطر آلودگی | به دلیل راندمان بالای تکثیر و فرآیندهای لوله باز، خطر آلودگی بالاتر است. | با فرآیندهای لوله بسته و ویژگی چرخه حرارتی، خطر آلودگی کمتر است. |
| کمیت سنجی | عمدتا کیفی؛ آنالیز کمی چالش برانگیز و کمتر دقیق است. | PCR کمی (qPCR) به کمیت سنجی دقیق و صحیح DNA هدف امکان می دهد. |
| کاربردها | برای تشخیص بیماری های عفونی، پایش محیط زیست و غربالگری سریع در محل مناسب است. | کاربردهای گسترده در تشخیص پزشکی، تحقیقات ژنتیکی، پزشکی قانونی و تحقیقات زیست شناسی مولکولی. |
| ابزار | بلوک حرارتی یا حمام آب اولیه کافی است. دستگاه های LAMP زمان واقعی برای نیازهای پیچیده تر در دسترس هستند. | نیاز به یک چرخه حرارتی تخصصی، با گزینه هایی برای تشخیص زمان واقعی (qPCR). |
| انعطاف پذیری | به دلیل نیاز به چندین پرایمر و ساختارهای ثانویه احتمالی، انعطاف پذیری کمتری در طراحی پرایمر دارد. | انعطاف پذیری بیشتر در طراحی پرایمر، امکان تکثیر طیف وسیعی از اهداف را فراهم می کند. |
نتیجهگیری
LAMP به عنوان شاهدی بر نوآوری در تشخیص مولکولی، روشی polyvalent ( پُلیوالان: polyvalent یعنی چند ظرفیتی، چند منظوره، چند کاربردی)، کارآمد و قابل دسترس برای تکثیر DNA ارائه میکند. با ادامه تکامل LAMP، ادغام آن در زمینههای مختلف علمی و پزشکی نویدبخش تأثیرگذاری بیشتر آن است و تشخیصهای پیشرفته را در سطح جهانی در دسترستر میکند. توسعه و تطبیق مداوم فناوری LAMP بدون شک همچنان راهحلهای جدیدی را برای چالشهای دیرینهی تشخیص و فراتر از آن ارائه خواهد کرد.
همچنین بخوانید:
مترجم: محمد صادق محمودی لرد