بیماری ها
سرطان سینه در مردان (Breast Cancer in Men) چیست؟
سرطان سینه (Breast cancer) عمدتاً در زنان رخ میدهد اما مردان نیز ممکن است به آن مبتلا شوند. بسیاری از مردم نمیدانند که مردان نیز بافت سینه دارند و ممکن است به سرطان سینه مبتلا شوند. سلولهای تقریباً هر قسمت از بدن میتوانند به سرطان تبدیل شوند و به نواحی دیگر گسترش یابند.
سرطان سینه زمانی شروع میشود که سلولهای سینه شروع به رشد خارج از کنترل میکنند. این سلولها معمولاً توموری را تشکیل میدهند که اغلب در عکس برداری با اشعه ایکس دیده شده یا به صورت یک توده در سینه احساس میشود. تومور، بدخیم (سرطانی) است اگر سلولها بتوانند به بافتهای اطراف رشد کنند (در آنها نفوذ کرده و به آن نواحی حمله کنند) یا به نواحی دور دست بدن گسترش یابند (متاستاز).
بافت سینه مردانه
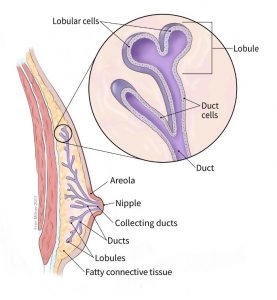
تا زمان بلوغ (به طور متوسط در حدود سن 9 یا 10 سالگی)، پسران و دختران جوان دارای مقدار کمی بافت سینه هستند که شامل چند مجرای در زیر نوک پستان و آرئول (areola، ناحیه اطراف نوک پستان) است. در دوران بلوغ، تخمدانهای دختران، هورمونهای زنانه میسازند و باعث رشد مجرای سینه و تشکیل لوبولها (lobules) در انتهای مجاری میشوند. حتی پس از بلوغ، پسران و مردان به طور معمول سطوح پایینی از هورمونهای زنانه دارند اما بافت سینه رشد چندانی ندارد. بافت سینه مردان مجرای نیز دارد اما فقط تعداد کمی لوبول را دارا است.
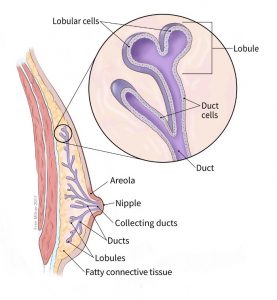
سرطان سینه از کجا شروع میشود؟
سرطان سینه میتواند از قسمتهای مختلف سینه شروع شود. بیشتر سرطانهای سینه در مجاری که شیر را به نوک پستان میرسانند (سرطانهای مجاری یا ductal cancers) شروع میشود.
برخی از آنها از غدد سازنده شیر مادر شروع میشوند (سرطانهای لوبولار یا lobular cancers). مردان نیز این مجراها و غدد را دارند، حتی اگر این نواحی به طور معمول عملکردی نداشته باشند. انواع سرطان سینه نیز وجود دارد که در انواع دیگر سلولهای سینه شروع میشوند اما این موارد کمتر رایج هستند.
تعداد کمی از سرطانها در سایر بافتهای سینه شروع میشوند. این سرطانها سارکوم (sarcomas) و لنفوم (lymphomas) نامیده میشوند و در واقع به عنوان سرطان سینه در نظر گرفته نمیشوند.
اگرچه بسیاری از انواع سرطان سینه میتوانند باعث ایجاد توده در سینه شوند اما همه آنها این گونه نیستند. علائم دیگری از سرطان سینه وجود دارد که باید مراقب آنها باشید و آنها را به یک پزشک گزارش دهید.
همچنین درک این نکته مهم است که اکثر تودههای سینه خوش خیم بوده و سرطانی (بدخیم) نیستند. تومورهای خوش خیم پستان، تودههایی غیر طبیعی هستند اما در خارج از سینه منتشر نمیشوند و تهدیدی برای زندگی نمیباشند. هر توده یا تغییر پستان باید توسط یک پزشک بررسی شود تا مشخص شود که آیا خوش خیم یا بدخیم (سرطانی) است و آیا ممکن است بر خطر ابتلا به سرطان شما در آینده تأثیر بگذارد.
نحوه انتشار سرطان سینه
سرطان سینه زمانی گسترش مییابد که سلولهای سرطانی وارد خون یا سیستم لنفاوی شده و به سایر قسمتهای بدن منتقل شوند.
سیستم لنفاوی (lymph system) شبکه ای از عروق لنفاوی (یا lymphatic) است که در سراسر بدن یافت میشود. رگهای لنفاوی مایع لنف (lymph fluid) را حمل کرده و گرههای لنفاوی را به هم متصل میکنند.
غدد لنفاوی (Lymph nodes) مجموعههای کوچک لوبیایی شکل از سلولهای سیستم ایمنی هستند. رگهای لنفاوی (Lymph vessels) مانند رگهای کوچک هستند، با این تفاوت که مایع شفافی به نام لنف (به جای خون) را از سینه دور میکنند. لنف حاوی مایع بافتی و مواد زائد و همچنین سلولهای سیستم ایمنی است. سلولهای سرطانی سینه میتوانند وارد عروق لنفاوی شده و در غدد لنفاوی شروع به رشد کنند. بیشتر عروق لنفاوی پستان به مناطق زیر تخلیه میشوند:
- گرههای لنفاوی زیر بازو (گرههای زیر بغل)
- غدد لنفاوی اطراف استخوان ترقوه (غدد لنفاوی فوق ترقوه [بالای استخوان ترقوه] و زیر ترقوه [زیر استخوان ترقوه])
- غدد لنفاوی داخل قفسه سینه نزدیک استخوان سینه (غدد لنفاوی پستانی داخلی)
اگر سلولهای سرطانی به گرههای لنفاوی شما گسترش یافته باشند، احتمال بیشتری وجود دارد که سلولها از طریق سیستم لنفاوی انتقال پیدا کرده و به سایر قسمتهای بدن گسترش یافته باشند (متاستاز).
هر چه تعداد غدد لنفاوی دارای سلولهای سرطانی سینه بیشتر باشد، احتمال اینکه سرطان در سایر اندامها نیز وجود داشته باشد، بیشتر میشود. به همین دلیل، یافتن سرطان در یک یا چند مورد از غدد لنفاوی اغلب بر برنامه درمانی شما تأثیر میگذارد. معمولاً جراحی برای برداشتن یک یا چند غدد لنفاوی برای اطلاع از گسترش سرطان مورد نیاز است.
با این حال، همه مردانی که سلولهای سرطانی در غدد لنفاوی خود دارند، متاستاز به نواحی دیگر را ایجاد نمیکنند و حتی ممکن است برخی از مردان سلولهای سرطانی در غدد لنفاوی خود نداشته باشند و بعداً متاستاز ایجاد کنند.
حالات خوش خیم در سینه
مردان همچنین ممکن است برخی از اختلالات خوش خیم (نه سرطانی) در سینه را داشته باشند.
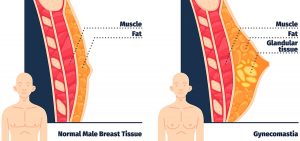
ژنیکوماستی (Gynecomastia)
ژنیکوماستی شایع ترین اختلال سینه در مردان است. این عارضه یک تومور نیست، بلکه افزایش مقدار بافت سینه مردان است. معمولاً مردان بافت سینه کمی دارند که قابل احساس یا توجه نیست. ژنیکوماستی میتواند به صورت یک رشد دکمه مانند یا دیسک در زیر نوک پستان و آرئول (دایره تیره اطراف نوک پستان) ظاهر شود که میتواند احساس و حتی گاهی دیده شود.
برخی از مردان ژنیکوماستی شدیدتری دارند و ممکن است به نظر برسد که سینههای کوچکی را دارا هستند. اگرچه ژنیکوماستی در مردان بسیار شایعتر از سرطان سینه است اما هر دو این عارضهها میتوانند به عنوان رشد زیر نوک پستان احساس شوند، به همین دلیل ضروری است که چنین تودههایی توسط پزشک بررسی شوند.
ژنیکوماستی در بین پسران نوجوان شایع است زیرا تعادل هورمونها در بدن در دوران نوجوانی تغییر میکند. همچنین در مردان مسن به دلیل تغییر در تعادل هورمونی آنها نیز شایع میباشد.
در موارد نادر، ژنیکوماستی به این دلیل رخ میدهد که تومورها یا بیماریهای غدد درون ریز خاص (تولید کننده هورمون) باعث میشوند بدن مرد استروژن بیشتری (هورمون اصلی زنانه) بسازد. غدد مردان به طور معمول مقداری استروژن تولید میکنند اما این مقدار از هورمون به اندازه ای نیست که باعث رشد سینه شود.
بیماریهای مربوط به کبد – که ارگان مهمی در متابولیسم هورمونهای مردانه و زنانه است – میتواند تعادل هورمونی مردان را تغییر داده و منجر به ژنیکوماستی شود. چاقی (اضافه وزن) همچنین میتواند باعث افزایش سطح استروژن در مردان شود.
برخی از داروها میتوانند باعث ژنیکوماستی شوند. این داروها شامل برخی از داروهای مورد استفاده برای درمان زخم و سوزش معده، فشار خون بالا، نارسایی قلبی و شرایط روانپزشکی است. مردان مبتلا به ژنیکوماستی باید از پزشک خود بپرسند که آیا داروهایی که مصرف میکنند ممکن است باعث این بیماری شود یا خیر.
سندرم کلاین فلتر (Klinefelter syndrome) – یک بیماری ژنتیکی نادر – میتواند منجر به ژنیکوماستی و همچنین افزایش خطر ابتلا به سرطان سینه در مردان شود. این وضعیت بیشتر در مبحث عوامل خطرزا برای سرطان پستان در مردان مورد بحث قرار گرفته است.
تومورهای خوش خیم سینه
انواع زیادی از تومورهای خوش خیم سینه (تودههای غیر طبیعی یا تودههای بافتی) مانند پاپیلوما (papillomas) و فیبروآدنوم (fibroadenomas) وجود دارد. تومورهای خوش خیم خارج از پستان پخش نمیشوند و تهدیدی برای زندگی نیستند. تومورهای خوش خیم سینه در زنان شایع هستند اما در مردان بسیار نادر اند.
انواع سرطان سینه در مردان
شایع ترین انواع سرطان سینه عبارتند از: کارسینوم مجرای در محل (ductal carcinoma in situ)، کارسینوم مجرای مهاجم (invasive ductal carcinoma) و کارسینوم لوبولار مهاجم (invasive lobular carcinoma).
بیشتر سرطانهای سینه کارسینوم هستند. در واقع، سرطانهای سینه اغلب نوعی سرطان به نام آدنوکارسینوم هستند که در سلولهایی که غدد را میسازند (بافت غدهای) شروع میشود. آدنوکارسینوم پستان از مجاری (مجاری شیر) یا لوبولها (غدد تولید کننده شیر) نیز شروع میشود.
انواع دیگری از سرطان سینه نیز وجود دارد که کمتر رایج هستند، مانند سارکوم (sarcomas)، فیلود (phyllodes)، بیماری پاژه (Paget’s disease) و آنژیوسارکوم (angiosarcomas) که در سلولهای عضله، چربی یا بافت همبند شروع میشود.
گاهی اوقات یک تومور سینه میتواند ترکیبی از انواع مختلف باشد و در برخی از انواع بسیار نادر سرطان سینه، سلولهای سرطانی ممکن است اصلاً توده یا تومور تشکیل ندهند.
هنگامی که بیوپسی برای کشف نوع خاص سرطان سینه انجام میشود، آسیب شناس همچنین میگوید که آیا سرطان به بافتهای اطراف گسترش یافته است یا خیر. نام و نوع سرطان سینه بسته به وسعت سرطان تغییر میکند.
- سرطان سینه در محل گسترش نیافته است.
- سرطانهای مهاجم یا نفوذی به بافت سینه اطراف گسترش یافته (تهاجم انجام داده اند).
این انواع کلی سرطان سینه را میتوان با عباراتی که در بالا ذکر شد بیشتر توضیح داد.
کارسینوم مجرای در محل (Ductal carcinoma in situ)
کارسینوم مجرای درجا (DCIS)؛ همچنین به عنوان کارسینوم داخل مجاری – intraductal carcinoma – نیز شناخته میشود) سرطان پستان غیر تهاجمی یا پیش تهاجمی در نظر گرفته میشود. در DCIS، سلولهایی که مجاری را پوشانده اند، شبیه سلولهای سرطانی به نظر میرسند. تفاوت بین DCIS و سرطان مهاجم در این است که سلولها از طریق دیواره مجاری به بافت اطراف پستان (یا به خارج از سینه پخش نشده اند) گسترش یافته اند.
DCIS به عنوان یک حالت پیش سرطانی در نظر گرفته میشود زیرا در برخی از موارد میتوانند به سرطانهای مهاجم تبدیل شوند. با این حال، در حال حاضر، هیچ راه خوبی وجود ندارد که به طور قطع بدانیم کدام موارد تبدیل به سرطانهای مهاجم میشوند و کدام یک نمیشوند. DCIS حدود 1 مورد از هر 10 مورد سرطان سینه در مردان را تشکیل میدهد. این نوع تقریباً همیشه با جراحی قابل درمان است.
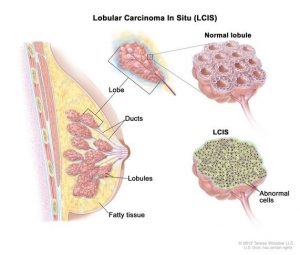
کارسینوم لوبولار در محل (Lobular carcinoma in situ)
کارسینوم لوبولار درجا (LCIS) ممکن است نئوپلازی لوبولار (lobular neoplasia) نیز نامیده شود. در LCIS، سلولهایی که شبیه سلولهای سرطانی هستند در لوبولهای غدد تولید کننده شیر پستان رشد میکنند اما از طریق دیواره لوبولها رشد نکردهاند. LCIS یک سرطان پیش تهاجمی واقعی نیست زیرا در صورت عدم درمان به سرطان مهاجم تبدیل نمیشود اما با افزایش خطر ابتلا به سرطان مهاجم در هر دو پستان مرتبط است. LCIS به ندرت در مردان دیده میشود.
کارسینوم مجرای نفوذی یا مهاجم (Infiltrating or invasive ductal carcinoma)
این نوع شایع ترین نوع سرطان سینه است. کارسینوم مجرای مهاجم (یا نفوذی) (IDC) از مجرای شیر پستان شروع میشود، از دیواره مجرا عبور کرده و به بافت چربی پستان رشد میکند. هنگامی که از دیواره مجرا عبور میکند، پتانسیل انتشار به سایر قسمتهای بدن را دارد. در این مرحله، ممکن است بتواند از طریق سیستم لنفاوی و جریان خون به سایر نقاط بدن گسترش یابد (متاستاز).
حداقل 8 مورد از هر 10 سرطان پستان مردان IDC (به تنهایی یا مخلوط با سایر انواع سرطان سینه مهاجم یا در محل) هستند. از آن جایی که سینه مردان بسیار کوچکتر از سینه زنان است، همه سرطانهای سینه مردان نسبتاً نزدیک به نوک پستان شروع میشوند، بنابراین احتمال انتشار آنها به نوک پستان بیشتر است. این موضوع با بیماری پاژه که در زیر توضیح داده شده است متفاوت است.
کارسینوم لوبولار نفوذی یا مهاجم (Infiltrating or invasive lobular carcinoma)
کارسینوم لوبولار مهاجم (ILC) در غدد تولید کننده شیر (لوبولها) شروع میشود.
این نوع مانند IDC، میتواند به سایر قسمتهای سینه و بدن گسترش یابد. ILC در مردان بسیار نادر است و تنها حدود 2 درصد از سرطانهای سینه مردانه را تشکیل میدهد. این امر به این دلیل است که مردان معمولاً بافت سینه لوبولار (غده ای) زیادی ندارند.
بیماری پاژه نوک پستان (Paget disease of the nipple)
این نوع سرطان سینه از مجاری پستان شروع میشود و به نوک پستان سرایت میکند. همچنین ممکن است به آرئول (دایره تیره اطراف نوک پستان) نیز گسترش یابد. پوست نوک پستان معمولاً پوسته پوسته، ملتهب و قرمز با نواحی دارای خارش، تراوش، سوزش یا خونریزی به نظر میرسد. همچنین ممکن است یک توده داخلی در سینه وجود داشته باشد.
بیماری پاژه ممکن است با DCIS یا با کارسینوم مجرای نفوذی همراه باشد. این همراهی نادر است و حدود 1 تا 3 درصد از سرطانهای سینه زنانه و درصد بیشتری (5 درصد) از سرطانهای سینه مردانه را تشکیل میدهد.
سرطان سینه التهابی (Inflammatory breast cancer)
سرطان سینه التهابی یک نوع سرطان سینه تهاجمی اما نادر است. این سرطان به جای ایجاد توده، سینه را متورم، قرمز، گرم و حساس میکند. این بیماری ممکن است با عفونت سینه اشتباه گرفته شود. این عارضه در مردان بسیار نادر است.
انواع خاص سرطان سینه مهاجم
انواع خاصی از سرطان سینه وجود دارد که زیر گروه سرطان مهاجم هستند. آنها بسیار کمتر از سرطانهای پستان ذکر شده در بالا شایع هستند.
برخی از این سرطانها ممکن است چشم انداز بهتر یا بدتری نسبت به کارسینوم مجرای نفوذی استاندارد داشته باشند.
- کارسینوم کیستیک آدنوئید یا آدنوسیستیک (Adenoid cystic or adenocystic carcinoma)
- کارسینوم آدنوسکواموس درجه پایین (Low-grade adenosquamous carcinoma، این یک نوع کارسینوم متاپلاستیک – metaplastic carcinoma – است)
- کارسینوم مدولاری (Medullary carcinoma)
- کارسینوم موسینوز یا کلوئید (Mucinous or colloid carcinoma)
- کارسینوم پاپیلاری (Papillary carcinoma)
- کارسینوم توبولار (Tubular carcinoma)
- کارسینوم متاپلاستیک (Metaplastic carcinoma، شامل سلول دوکی و سنگفرشی، به جز کارسینوم آدنوسکواموس درجه پایین)
- کارسینوم میکروپاپیلاری (Micropapillary carcinoma)
- کارسینوم مختلط (Mixed carcinoma ، دارای ویژگیهای مجرای مهاجم و لوبولار)
به طور کلی، این انواع فرعی هنوز مانند کارسینوم نفوذی استاندارد درمان میشوند.
آمار کلیدی برای سرطان سینه در مردان
تخمینهای انجمن سرطان آمریکا برای سرطان سینه در مردان در ایالات متحده برای سال 2022 عبارتند از:
- حدود 2710 مورد جدید سرطان تهاجمی پستان تشخیص داده خواهد شد.
- حدود 530 مرد بر اثر سرطان سینه خواهند مرد.
سرطان سینه در میان مردان سفید پوست حدود 100 برابر کمتر از زنان سفید پوست شایع است. این بیماری در بین مردان سیاه پوست حدود 70 برابر کمتر از زنان سیاه پوست است. مانند زنان سیاه پوست، مردان سیاه پوست مبتلا به سرطان سینه معمولاً پیش آگهی بدتری دارند. برای مردان، خطر ابتلا به سرطان سینه در طول زندگی حدود 1 در 833 است.
علائم و نشانههای سرطان سینه در مردان
علائم احتمالی سرطان سینه که باید مراقب آنها بود عبارتند از:
- وجود یک توده یا تورم که اغلب (اما نه همیشه) بدون درد است.
- فرو رفتگی یا چروک شدن پوست
- جمع شدن نوک پستان (چرخش به داخل)
- قرمزی یا پوسته پوسته شدن نوک پستان یا پوست سینه
- ایجاد ترشح از نوک پستان
گاهی اوقات سرطان سینه میتواند به غدد لنفاوی زیر بازو یا اطراف استخوان یقه (ترقوه) گسترش یابد و حتی قبل از اینکه تومور اصلی در سینه به اندازه کافی بزرگ شود تا توسط فرد احساس شود، توده یا تورم ایجاد کند.
این تغییرات همیشه ناشی از سرطان نیستند اما در صورت مشاهده هرگونه تغییر در پستان، باید در اسرع وقت به یک متخصص مراقبتهای پزشکی مراجعه کنید.
چه چیزی باعث سرطان سینه در مردان میشود؟
اگرچه برخی عوامل خطرزا ممکن است شانس ابتلای مردان به سرطان سینه را افزایش دهند اما علت بیشتر سرطانهای سینه در مردان ناشناخته است.
سطوح هورمونی
سلولهای پستان به طور معمول در پاسخ به هورمونهای زنانه مانند استروژن رشد و تقسیم میشوند. هر چه سلولها بیشتر تقسیم شوند، احتمال اشتباه در هنگام کپی کردن DNAشان بیشتر میشود. این تغییرات DNA در نهایت میتواند منجر به سرطان شود.
عواملی که سطح هورمونهای زنانه و مردانه را در بدن نامتعادل میکنند، میتوانند بر خطر سرطان سینه تأثیر بگذارند. بسیاری از این موارد در مبحث عوامل خطرزا برای سرطان پستان در مردان شرح داده شده است.
تغییرات ژنی (جهش)
محققان در درک اینکه چگونه تغییرات خاصی در DNA میتواند باعث سرطانی شدن سلولهای طبیعی شود، پیشرفت زیادی کرده اند. DNA ماده شیمیایی موجود در سلولهای ما است که ژنهای ما – دستور العملهایی برای نحوه عملکرد سلولهای ما – را میسازد. ما معمولا شبیه والدین خود هستیم زیرا آنها منبع DNA ما هستند. با این حال، DNA بر چیزی بیشتر از ظاهر ما تأثیر میگذارد.
برخی از ژنها حاوی دستور العملهایی برای کنترل زمان رشد، تقسیم و مرگ سلولهای ما هستند. ژنهای خاصی که تقسیم سلولی را سرعت میبخشند، انکوژن (oncogenes) نامیده میشوند. سایر مواردی که تقسیم سلولی را کند میکنند یا باعث میشوند سلولها در زمان مناسب بمیرند، ژنهای سرکوبگر تومور (tumor suppressor genes) نامیده میشوند. سرطانها میتوانند ناشی از جهشهای DNA (نقایص) باشند که انکوژنها را فعال میکنند یا ژنهای سرکوبگر تومور را خاموش میکنند.
جهشهای ژنی اکتسابی
بیشتر جهشهای DNA مربوط به سرطان سینه مردان در طول زندگی اتفاق میافتند نه اینکه قبل از تولد از والدین به ارث رسیده باشند. مشخص نیست چه چیزی باعث بیشتر بروز این جهشها میشود. تابش به ناحیه پستان در تعداد کمی از موارد عاملی برای ابتلا به سرطان است.
برخی از جهشهای اکتسابی انکوژنها و یا ژنهای سرکوبکننده تومور ممکن است نتیجه مواد شیمیایی سرطانزا در محیط یا رژیم غذایی ما باشند اما مطالعات تاکنون هیچ ماده شیمیایی را که مسئول این جهشها در سرطان سینه مردانه باشد، شناسایی نکردهاند.
جهشهای ژنی ارثی
برخی از تغییرات ارثی DNA میتواند باعث بروز خطر بالای ابتلا به برخی سرطانها شود و مسئول سرطانهایی هستند که در برخی خانوادهها وجود دارد.
برخی از سرطانهای سینه با جهشهای ارثی ژنهای سرکوبکننده تومور BRCA1 یا BRCA2 مرتبط هستند. به طور معمول، این ژنها پروتئینهایی را میسازند که به سلولها کمک میکنند تا آسیب DNA را شناسایی و یا ترمیم کرده و از رشد غیر عادی آنها جلوگیری کنند. اما اگر فردی یک ژن جهش یافته را از یکی از والدین به ارث برده باشد، احتمال ابتلا به سرطان سینه بیشتر است.
مردانی که دارای جهش ارثی در ژنهای BRCA1 و BRCA2 هستند، خطر ابتلا به سرطان سینه و احتمالاً برخی سرطانهای دیگر مانند سرطان پروستات و لوزالمعده را در طول زندگی دارند. سندرمهای سرطان ارثی دیگری نیز وجود دارد که میتوانند با سرطان سینه مردان مرتبط باشند.
همه مردانی که سرطان سینه در آنها تشخیص داده شده است باید آزمایش ژنتیک را در نظر بگیرند زیرا ممکن است در معرض خطر ابتلا به سرطانهای دیگری مانند سرطان پروستات و پانکراس باشند. داشتن یکی از این تغییرات ژنی ارثی ممکن است بر شانس ابتلای اعضای خانواده آنها به سرطانهای خاص تأثیر بگذارد.
عوامل خطرزا سرطان سینه در مردان
عامل خطرزا هر چیزی است که بر شانس ابتلا به بیماری مانند سرطان سینه تأثیر میگذارد.
اما داشتن یک عامل خطرزا یا حتی تعداد زیادی از آنها به این معنی نیست که مطمئناً به این بیماری مبتلا خواهید شد. برخی از مردان با یک یا چند عامل خطرزا سرطان سینه هرگز به این بیماری مبتلا نمیشوند، در حالی که اکثر مردان مبتلا به سرطان سینه هیچ عامل خطرزا آشکاری ندارند.
ما هنوز به طور کامل دلایل سرطان سینه در مردان را درک نکرده ایم اما محققان چندین عامل را یافته اند که ممکن است خطر ابتلا به آن را افزایش دهد. مانند سرطان سینه زنانه، بسیاری از این عوامل با سطح هورمون جنسی بدن شما مرتبط هستند.
سال خوردگی
افزایش سن یک عامل خطرزا مهم برای ایجاد سرطان سینه در مردان است. خطر ابتلا به سرطان سینه با افزایش سن در مردان افزایش مییابد. به طور متوسط، مردان مبتلا به سرطان سینه زمانی که با این بیماری تشخیص داده میشوند، حدود 72 سال سن دارند.
سابقه خانوادگی سرطان سینه
اگر سایر اعضای خانواده (بستگان خونی) سرطان سینه داشته باشند، خطر ابتلا به سرطان سینه در افراد دیگر افزایش مییابد. از هر 5 مرد مبتلا به سرطان سینه، 1 مورد دارای یکی از بستگان نزدیک – زن یا مرد – مبتلا به این بیماری است.
جهشهای ژنی ارثی
مردانی که دارای جهش (نقص) در ژن BRCA2 هستند، خطر ابتلا به سرطان سینه را افزایش میدهند و خطر ابتلا به سرطان سینه در طول زندگی آنها حدود 6 در 100 است. جهشهای BRCA1 همچنین میتوانند باعث سرطان سینه در مردان شوند اما این خطر کمتر است، حدود 1 در 100.
اگرچه جهش در این ژنها اغلب در اعضای خانوادههایی با موارد زیادی از سرطان سینه و یا تخمدان دیده میشوند اما در مردان مبتلا به سرطان سینه که سابقه خانوادگی قوی نداشته اند نیز دیده شده اند.
جهش در ژنهای CHEK2، PTEN و PALB2 نیز ممکن است مسئول برخی سرطانهای سینه در مردان باشد.
سندرم کلاین فلتر (Klinefelter syndrome)
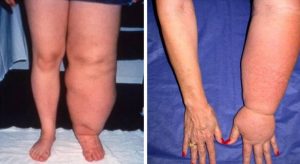
سندرم کلاین فلتر یک بیماری مادرزادی (موجود در زمان تولد) است که از هر 1000 مرد 1 نفر را مبتلا میکند. به طور معمول سلولهای بدن مردان دارای یک کروموزوم X منفرد به همراه یک کروموزوم Y هستند، در حالی که سلولهای زنان دارای دو کروموزوم X هستند. مردان مبتلا به سندرم کلاین فلتر دارای سلولهایی با کروموزوم Y به علاوه حداقل دو کروموزوم X (اما گاهی اوقات بیشتر) هستند.
مردان مبتلا به سندرم کلاین فلتر نیز بیضههای کوچکی دارند و اغلب نابارور هستند زیرا قادر به تولید سلولهای اسپرم کارآمد نمیباشند. در مقایسه با مردان دیگر، سطح آندروژن (androgens، هورمونهای مردانه) کمتر و استروژن (estrogens، هورمونهای زنانه) بیشتر است. به همین دلیل، آنها اغلب دچار ژنیکوماستی (رشد خوش خیم سینه مردان) میشوند.
احتمال ابتلا به سرطان سینه در مردان مبتلا به سندرم کلاین فلتر بیشتر از مردان دیگر است. ابتلا به این بیماری میتواند خطر ابتلا را بین 20 تا 60 برابر بیشتر از مردان در جمعیت عمومی افزایش دهد.
قرار گیری در معرض تشعشع
مردی که ناحیه قفسه سینهاش با پرتو درمانی (مانند درمان سرطان موجود قفسه سینه، مانند لنفوم) تحت درمان قرار گرفته است، خطر ابتلا به سرطان سینه را افزایش میدهد.
الکل
مصرف الکل زیاد (نوشیدنیهای الکلی) خطر ابتلا به سرطان سینه را در مردان افزایش میدهد. این امر ممکن است به دلیل اثرات الکل بر روی کبد باشد.
بیماریهای کبدی
کبد (Liver) نقش مهمی در متعادل کردن سطح هورمونهای جنسی دارد. در موارد بیماریهای شدید کبدی مانند سیروز (cirrhosis)، کبد به خوبی کار نمیکند و سطح هورمونها ناهموار است و در واقع همین امر باعث کاهش سطح آندروژن و افزایش سطح استروژن میشود. مردان مبتلا به بیماری کبدی نیز میتوانند شانس بیشتری برای ایجاد رشد خوش خیم سینه مردان (ژنیکوماستی) داشته باشند و همچنین خطر ابتلا به سرطان سینه را افزایش میدهند.
استروژن درمانی (Estrogen treatment)
داروهای مرتبط با استروژن زمانی در هورمون درمانی برای مردان مبتلا به سرطان پروستات استفاده میشد. این نوع روند درمانی ممکن است به میزان کمی خطر سرطان سینه را افزایش دهد.
این نگرانی وجود دارد که افراد تراجنسیتی یا ترنسکشوالی که دوزهای بالایی از استروژن را به عنوان بخشی از روند تغییر جنسیت خود مصرف میکنند نیز ممکن است در معرض خطر ابتلا به سرطان سینه باشند. با این حال، هیچ مطالعه ای در مورد خطر ابتلا به سرطان سینه در افراد تراجنسیتی انجام نشده است، بنابراین مشخص نیست که خطر ابتلا به سرطان سینه در آنها چقدر است.
چاقی
مطالعات نشان داده اند که خطر ابتلا به سرطان سینه در زنان با چاقی (اضافه وزن) پس از یائسگی افزایش مییابد. چاقی همچنین یک عامل خطرزا برای سرطان سینه در مردان است. دلیل آن این است که سلولهای چربی در بدن هورمونهای مردانه (آندروژنها) را به هورمونهای زنانه (استروژن) تبدیل میکنند. این بدان معناست که مردان چاق سطوح بالاتری از استروژن را در بدن خود دارند.
عارضههای بیضوی
برخی شرایط، مانند داشتن یک بیضه افتاده، داشتن اوریون (mumps) در بزرگسالی یا برداشتن یک یا هر دو بیضه با جراحی (ارکیکتومی یا orchiectomy) ممکن است خطر ابتلا به سرطان سینه در مردان را افزایش دهد.
آیا میتوان از سرطان سینه در مردان پیشگیری کرد؟
از آن جایی که علت اکثر سرطانهای سینه مشخص نیست، هیچ راه شناخته شده ای برای پیشگیری از آنها وجود ندارد. اما کارهایی وجود دارد که یک مرد میتواند برای کاهش خطر ابتلا به سرطان سینه انجام دهد.
به وزن سالم خود برسید و آن را حفظ کنید: هم افزایش وزن بدن و هم چاقی در بزرگسالی با خطر بالاتر سرطان سینه در زنان مرتبط است. از آن جایی که اضافه وزن یا چاقی با افزایش خطر ابتلا به چندین سرطان مرتبط است، انجمن سرطان آمریکا به شما توصیه میکند در طول زندگی وزن سالمی داشته باشید و با متعادل کردن میزان مصرف غذا و فعالیت بدنی از اضافه وزن خودداری کنید.
اجتناب از مصرف الکل یا محدود کردن آن: مصرف الکل خطر ابتلا به سرطان سینه را در زنان افزایش میدهد. حتی سطوح پایین مصرف الکل با افزایش خطر ابتلا به این بیماری مرتبط است. مصرف الکل با ابتلا به چندین سرطان مرتبط است و سومین عامل خطرزا مهم قابل پیشگیری برای سرطان میباشد. بهتر است الکل مصرف نکنید. برای مردانی که مشروب الکلی مینوشند، نباید این مقدار بیش از 2 نوشیدنی الکلی در روز شود.
از نظر بدنی فعال باشید: بسیاری از مطالعات نشان داده اند که فعالیت بدنی متوسط تا شدید با کاهش خطر ابتلا به سرطان سینه در زنان و همچنین بسیاری از انواع دیگر سرطان مرتبط است. انجمن سرطان آمریکا توصیه میکند که بزرگسالان حداقل 150 تا 300 دقیقه فعالیت با شدت متوسط یا 75 تا 150 دقیقه فعالیت شدید در هفته (یا ترکیبی از اینها) را ترجیحاً در طول هفته انجام دهند. رسیدن به میزان بالای 300 دقیقه یا فراتر از آن ایده آل است.
در حال حاضر بهترین راهکار برای کاهش مرگ و میر ناشی از این بیماری، تشخیص زود هنگام و درمان سریع است. تشخیص زود هنگام برای مردان مشکل ساز بوده است، زیرا ممکن است متوجه وجود تودهها در سینه نشوند یا فقط زمانی که تودهها بزرگ شده اند به پزشک مراجعه کنند. به طور کلی، سرطان سینه در مردان در مراحل پیشرفته تری نسبت به زنان تشخیص داده میشود.
آیا سرطان سینه در مردان را میتوان زود تشخیص داد؟
یافتن زود هنگام سرطان سینه شانس درمان موفقیت آمیز سرطان سینه مردانه را افزایش میدهد. با این حال، از آن جایی که سرطان سینه در مردان بسیار غیر معمول است، بعید است که غربالگری مردان در جمعیت عمومی از نظر سرطان سینه با ماموگرافی (mammograms) یا سایر آزمایشها فایدهای داشته باشد.
تفاوت در تشخیص زود هنگام سرطان سینه در مردان و زنان
شباهتهای زیادی بین سرطان سینه در مردان و زنان وجود دارد اما تفاوتهای مهمی وجود دارد که بر تشخیص زود هنگام آن تأثیر میگذارد.
اندازه پستان
واضح ترین تفاوت بین سینه مردانه و زنانه اندازه پستان است. از آن جایی که مردان بافت پستان بسیار کمی دارند، برای مردان و متخصصان مراقبتهای پزشکی آنها راحت تر است که تودههای کوچک (تومور) را احساس کنند. از سوی دیگر، از آن جایی که مردان بافت سینه کمی دارند، سرطانها برای رسیدن به نوک پستان، پوستی که سینه را پوشانده است یا ماهیچههای زیر سینه نیازی به رشد زیادی ندارند. بنابراین، اگرچه سرطان سینه در مردان در ابتدا کمی کوچکتر از زنان است اما اغلب به بافتها یا غدد لنفاوی مجاور گسترش یافته است. میزان انتشار یکی از مهم ترین عوامل در چشم انداز (وضعیت آتی بیمار) سرطان سینه است.
نداشتن آگاهی
تفاوت دیگر این است که سرطان سینه در بین زنان شایع و در بین مردان نادر است. خانمها تمایل دارند از این بیماری و علائم هشدار دهنده احتمالی آن آگاه باشند اما بسیاری از مردان فکر نمیکنند که اصلا ممکن است به آن مبتلا شوند.
برخی از مردان تودههای سینه را نادیده میگیرند یا فکر میکنند که ناشی از عفونت یا علل دیگری است و تا زمانی که توده فرصتی برای رشد نداشته باشد تحت درمان پزشکی قرار نمیگیرند. برخی از مردان وقتی تودهای در سینه خود پیدا میکنند خجالت میکشند و نگران هستند که ممکن است کسی مردانگی آنها را زیر سوال ببرد. این مسائل نیز میتواند تشخیص را به تاخیر بیندازد و شانس مرد را برای درمان موفقیت آمیز کاهش دهد.
برای مردانی که در معرض خطر هستند یا ممکن است باشند
معاینه دقیق پستان ممکن است برای غربالگری مردان با سابقه خانوادگی قوی سرطان سینه و یا با جهشهای BRCA که با آزمایش ژنتیکی کشف شدهاند، مفید باشد. غربالگری سرطان سینه برای مردان مورد مطالعه قرار نگرفته است تا بدانیم که آیا این روش تشخیص سرطان مفید است یا خیر و ماموگرافی (تاباندن اشعه ایکس به پستان) و سونوگرافی معمولاً تنها در صورت یافتن توده انجام میشود. مردانی که در معرض خطر بالای ابتلا به سرطان سینه هستند، باید با پزشک خود در مورد نحوه مدیریت میزان خطر ابتلای خود صحبت کنند.
مشاوره و آزمایش ژنتیک
اگر سابقه خانوادگی قوی سرطان سینه (در مردان یا زنان)، سرطان تخمدان، سرطان لوزالمعده و یا سرطان پروستات دارید که ممکن است ناشی از جهش BRCA باشد، و یا اگر فرد دیگری در خانواده شما شناخته شده باشد یک جهش BRCA را داشته باشد، ممکن است بخواهید آزمایش ژنتیکی را برای تعیین اینکه آیا یک ژن جهش یافته BRCA را به ارث برده اید یا خیر در نظر بگیرید.
اگر آزمایش یک ژن جهش یافته BRCA را تشخیص دهد، شما و تیم مراقبتهای پزشکیتان میتوانید به دقت مراقب علائم اولیه سرطان باشید. سرطانهای دیگر از جمله سرطان پروستات، سرطان پانکراس و سرطان بیضه نیز با جهشهای BRCA مرتبط هستند.
از آن جایی که سرطان سینه در مردان میتواند ناشی از جهشهای BRCA باشد، مردان مبتلا به سرطان سینه باید آزمایش ژنتیک را نیز در نظر بگیرند.
اگر به انجام آزمایش ژنتیک فکر میکنید، اکیداً توصیه میشود که ابتدا با یک متخصص واجد شرایط برای توضیح و تفسیر این آزمایشها صحبت کنید، مانند یک مشاور ژنتیک یا یک پرستار یا پزشک با آموزشهای ویژه. بسیار مهم است که بدانید آزمایش ژنتیک چه چیزی را میتواند به شما بگوید و چه چیزی را نمیتواند به شما بگوید و قبل از انجام آزمایش، مزایا و خطرات آن را به دقت بسنجید.
نتایج آزمایش همیشه واضح نیست و حتی اگر هم باشد، همیشه مشخص نیست که در رابطه آنها چه باید کرد. ممکن است نگرانیهای دیگری نیز وجود داشته باشد، از جمله اینکه نتایج ممکن است برای سایر اعضای خانواده چه معنایی داشته باشند.
آزمایشات سرطان سینه در مردان
تاریخچه پزشکی و معاینه فیزیکی
اگر احتمال ابتلا به سرطان سینه وجود دارد، پزشک شما میخواهد یک تاریخچه کامل پزشکی شخصی و خانوادگی را دریافت کند. این کار ممکن است سرنخهایی را در مورد علت علائمی که دارید و اینکه آیا ممکن است در معرض خطر ابتلا به سرطان سینه باشید، ارائه دهد.
یک معاینه کامل پستان برای یافتن هر گونه توده یا نواحی مشکوک و وجود بافت، اندازه و ارتباط آنها با پوست و ماهیچه انجام میشود. پزشک همچنین ممکن است بقیه بدن شما را برای یافتن شواهدی مبنی بر گسترش احتمالی، مانند بزرگ شدن غدد لنفاوی (به خصوص زیر بازو) بررسی کند.
آزمایشات تصویر برداری سرطان سینه در مردان
اگر علائم یا علائمی دارید که میتواند به معنای سرطان سینه یا بیماری دیگر پستانی باشد، پزشک ممکن است یک یا چند یا چند آزمایش تصویر برداری زیر را توصیه کند.
ماموگرافی تشخیصی (Diagnostic mammogram)
ماموگرافی یک معاینه اشعه ایکس با دوز کم از پستان است که به پزشکانی به نام رادیولوژیست اجازه میدهد تا تغییرات در بافت پستان را بررسی کنند. به دلیل وجود عارضهها در زمان انجام این تست به آن ماموگرافی تشخیصی میگویند.
ماموگرافی از دستگاهی استفاده میکند که فقط بافت سینه را مورد بررسی قرار میدهد. سینه بین 2 صفحه فشار داده میشود تا بافت صاف و پخش شود. فشرده سازی فقط چند ثانیه طول میکشد و ممکن است برای مدت کوتاهی ناراحت کننده باشد اما برای گرفتن تصویر بهتر ضروری است. در برخی موارد، تصاویر خاصی به نام نماهای مخروطی یا نقطهای (cone or spot views) با بزرگنمایی گرفته میشود تا ارزیابی ناحیه کوچکی از بافت غیر طبیعی سینه آسانتر شود.
نتایج این آزمایش ممکن است نشان دهد که برای تشخیص سرطانی بودن ناحیه غیر طبیعی به بیوپسی نیاز است. ماموگرافی اغلب در مردان دقیقتر از زنان است زیرا مردان سینههای متراکم یا سایر تغییرات رایج سینهای ندارند که ممکن است در آزمایش اختلال ایجاد کنند.
سونوگرافی سینه (Breast ultrasound)
سونوگرافی پستان اغلب برای بررسی وجود برخی از انواع تغییرات پستانی استفاده میشود.
سونوگرافی سینه از امواج صوتی برای ایجاد تصویر کامپیوتری از داخل سینه استفاده میکند. یک ژل روی پوست سینه مالیده میشود و ابزاری گرز مانند به نام مبدل (transducer) روی پوست حرکت میکند.
مبدل امواج صوتی را میفرستد و پژواکها را هنگامی که از بافتهای بدن منعکس میشوند، دریافت میکند. پژواکها به یک تصویر روی صفحه کامپیوتر تبدیل میشوند. ممکن است زمانی که مبدل در سینه حرکت میکند فشاری را احساس کنید اما نباید دردناک باشد. این آزمایش شما را در معرض تشعشع قرار نمیدهد.
سونوگرافی پستان اغلب برای بررسی تغییرات پستان که در طول ماموگرافی یا معاینه فیزیکی پیدا میشوند، استفاده میشود. این روش مفید است زیرا اغلب میتواند تفاوت بین کیستهای پر از مایع (که بعید به نظر میرسد سرطان باشند) و تودههای جامد (که ممکن است برای اطمینان از سرطانی نبودن آنها به آزمایش بیشتری نیاز داشته باشند) را تشخیص دهد.
در فردی که تومور سینه دارد، از سونوگرافی نیز میتوان برای بررسی بزرگ شدن غدد لنفاوی زیر بازو استفاده کرد. در صورت وجود، میتوان از سونوگرافی برای هدایت سوزن برای گرفتن نمونه (بیوپسی) برای جستجوی سلولهای سرطانی در آن جا و در بافت پستان استفاده کرد.
بیوپسی پستان (Breast Biopsy)
هنگامی که آزمایشات دیگر نشان میدهد که شما ممکن است سرطان سینه داشته باشید، احتمالاً نیاز به بیوپسی (نمونه برداری) خواهید داشت. نیاز به بیوپسی سینه لزوماً به معنای ابتلا به سرطان نیست.
اکثر نتایج بیوپسی سرطان نیستند اما بیوپسی تنها راه برای پیدا کردن سرطان است. در طول بیوپسی، پزشک سلولها را از ناحیه مشکوک خارج میکند تا بتوان آنها را در آزمایشگاه بررسی کرد تا ببیند آیا سلولهای سرطانی وجود دارند یا خیر. معمولاً حداقل چند روز طول میکشد تا شما از نتایج آگاه شوید.
اگر پزشک فکر میکند که نیازی به بیوپسی ندارید اما همچنان احساس میکنید مشکلی در سینهتان وجود دارد، حس درونی خود را دنبال کنید. از صحبت با پزشک خود در این مورد نترسید یا برای گرفتن نظر دومی نزد پزشک دیگری بروید. بیوپسی تنها راه مطمئن برای تشخیص سرطان سینه است.
انواع مختلفی از بیوپسی سینه وجود دارد. نوع بیوپسی در نظر گرفته شده برای شما بستگی به شرایط شما دارد.
بیوپسی آسپیراسیون با سوزن ظریف (Fine needle aspiration biopsy یا FNA): این نوع بیوپسی اغلب برای بررسی گسترش سرطان در غدد لنفاوی مجاور استفاده میشود. پزشک از یک سوزن بسیار نازک و تو خالی متصل به سرنگ استفاده میکند تا مقدار کمی از بافت یا مایع را از یک ناحیه مشکوک خارج کند.
یک بی حس کننده موضعی (داروی بی حس کننده) ممکن است استفاده شود یا روند بیوپسی بدون بی حسی انجام شود. سپس نمونه بیوپسی بررسی میشود تا بررسی کنند که آیا سلولهای سرطانی در آن وجود دارد یا خیر.
اگر ناحیه قرار گرفته تحت بیوپسی قابل لمس باشد، سوزن را میتوان در زمانی که پزشک آن را احساس میکند به داخل آن هدایت کرد. اگر توده را نتوان به راحتی حس کرد، پزشک ممکن است سوزن را روی صفحه اولتراسوند در حین حرکت آن به ناحیه تماشا کند. این روش بیوپسی با هدایت اولتراسوند (ultrasound-guided biopsy) نامیده میشود.
بیوپسی FNA ساده ترین نوع بیوپسی است اما گاهی اوقات اگر سوزن به داخل سلولهای سرطانی نرود، سرطان تشخیص داده نمیشود.
اگر نتایج بیوپسی FNA تشخیص واضحی را ارائه نکند یا پزشک شما همچنان نگرانی داشته باشد، ممکن است نیاز به انجام بیوپسی دوم یا نوع دیگری از بیوپسی داشته باشید.
بیوپسی با سوزن مرکزی (Core needle biopsy یا CNB): این روش رایج ترین نوع بیوپسی است که برای تشخیص سرطان سینه استفاده میشود. پزشک از یک سوزن پهن و تو خالی برای بیرون آوردن تکههای بافت سینه از ناحیه مشکوک استفاده میکند.
سوزن مورد استفاده در این روش بزرگتر از سوزن مورد استفاده برای FNA است و به پزشک اجازه میدهد تا سیلندرهای (هسته) بزرگتری از بافت را خارج کند. چندین سیلندر اغلب حذف میشوند. بیوپسی با داروهای بی حس کننده موضعی انجام میشود و پزشک یا ناحیه غیر طبیعی را احساس میکند یا از آزمایش تصویر برداری (مانند سونوگرافی یا MRI) برای یافتن نقطه مورد استفاده برای بیوپسی استفاده میکند.
علاوه بر CNB استاندارد، دو نوع دیگر از CNB وجود دارد:
- بیوپسی سوزنی هسته استریوتاکتیک (Stereotactic core needle biopsy)
- بیوپسی هسته با کمک خلاء (Vacuum-assisted core biopsy)
اگر نتایج CNB تشخیص واضحی را ارائه نکرد یا پزشک شما همچنان نگرانیهایی را داشت، ممکن است نیاز به بیوپسی دوم یا نوع دیگری از بیوپسی داشته باشید.
بیوپسی جراحی (باز یا Surgical biopsy): بیشتر موارد سرطان سینه را میتوان با بیوپسی سوزنی تشخیص داد. به ندرت، جراحی برای برداشتن تمام یا بخشی از توده برای آزمایش لازم است. بیشتر اوقات، جراح کل توده یا ناحیه غیر طبیعی و همچنین حاشیه اطراف بافت طبیعی سینه را بر میدارد.
2 نوع بیوپسی جراحی وجود دارد:
- بیوپسی برشی (incisional biopsy) تنها بخشی از ناحیه مشکوک را بر میدارد که برای تشخیص کافی است.
- بیوپسی اکسیزیونال (excisional biopsy) کل تومور یا ناحیه غیر طبیعی را همراه با تلاش برای بیرون آوردن لبه بافت طبیعی پستان یا بدون آن (بسته به دلیل انجام بیوپسی) بر میدارد.
بیوپسی غدد لنفاوی: پزشک همچنین ممکن است نیاز به بیوپسی غدد لنفاوی زیر بازو داشته باشد تا آنها را از نظر گسترش سرطان بررسی کند. این کار ممکن است همزمان با بیوپسی تومور سینه یا در حین جراحی برای برداشتن تومور سینه انجام شود. این کار با بیوپسی سوزنی یا با بیوپسی غدد لنفاوی نگهبان و یا تشریح غدد لنفاوی زیر بغل انجام میشود.
سرطان سینه در مردان چگونه طبقه بندی میشود؟
سرطان سینه بر اساس نتایج آزمایشات آزمایشگاهی پس از بیوپسی یا جراحی به روشهای مختلفی طبقه بندی میشود. به سرطان سینه بر اساس نوع سلولی که از آن شروع شده، درجه آن بر اساس ظاهر سلولها و سرعت رشد آنها و طبقه بندیهای دیگر بر اساس نتایج آزمایشات برای گیرندههای هورمونی یا ژنهای مختلف در سلولهای سرطانی، نوعی داده میشود.
نوع سرطان سینه
بافت برداشته شده در طی بیوپسی (یا در حین جراحی) ابتدا در آزمایشگاه بررسی میشود تا مشخص شود آیا سرطان وجود دارد یا خیر و همچنین آیا کارسینوما یا نوع دیگری از سرطان است (مانند سارکوم). اگر بافت کافی وجود داشته باشد، پاتولوژیست ممکن است بتواند تشخیص دهد که سرطان در محل (نه تهاجمی) است یا مهاجم. بیوپسی همچنین برای تعیین نوع سرطان مانند کارسینوم مجرای مهاجم یا کارسینوم لوبولار مهاجم استفاده میشود.
درجه سرطان سینه
به سلولهای سرطانی زمانی که از پستان خارج شده و در آزمایشگاه بررسی میشوند، درجه داده میشود. درجه بر اساس این است که سلولهای سرطانی چقدر شبیه سلولهای طبیعی پستان هستند.
برای سرطانهای مهاجم، عدد درجه پایینتر (1) معمولاً به این معنی است که سرطان کندتر رشد میکند و احتمال انتشار آن کمتر است. عدد بالاتر (3) به معنای سرطان با رشد سریعتر است که احتمال انتشار آن بیشتر است. درجه برای کمک به پیش بینی وضعیت شما (چشم انداز) و کمک به تشخیص اینکه چه درمانهایی ممکن است بهترین کارایی را داشته باشند، استفاده میشود. گاهی اوقات به جای اعداد، از کلماتی مانند “خوب متمایز شده”، “تمایز متوسط” و “تمایز ضعیف” برای توصیف درجه استفاده میشود:
- درجه 1 یا به خوبی تمایز یافته (well differentiated): سلولها کندتر رشد میکنند و بیشتر شبیه بافت طبیعی پستان هستند.
- درجه 2 یا با تمایز متوسط (moderately differentiated): سلولها با سرعت رشد میکنند و شبیه سلولها در مرحله ای بین درجه 1 و 3 هستند.
- درجه 3 یا با تمایز ضعیف (poorly differentiated): سلولهای سرطانی بسیار متفاوت از سلولهای طبیعی به نظر میرسند و احتمالاً سریعتر رشد و گسترش مییابند.
اطلاعات ما در مورد گزارشهای پاتولوژی میتواند به شما در درک جزئیات سرطان سینه کمک کند.
کارسینوم مجرای در محل نیز درجه بندی میشود اما درجه فقط بر اساس غیر طبیعی بودن سلولهای سرطانی است.
مناطق نکروز (necrosis، سلولهای سرطانی مرده یا در حال مرگ) نیز ذکر شده است. اگر نکروز وجود داشته باشد، به این معنی است که تومور به سرعت در حال رشد است.
آزمایشاتی برای طبقه بندی سرطان سینه
گیرنده استروژن (Estrogen receptor یا ER) و گیرنده پروژسترون (progesterone receptor یا PR)
گیرندهها پروتئینهایی در داخل یا روی سلولها هستند که میتوانند به مواد خاصی در خون بچسبند. سلولهای طبیعی سینه و برخی از سلولهای سرطانی سینه گیرندههایی دارند که به هورمونهای استروژن و پروژسترون متصل میشوند و برای رشد به این هورمونها وابسته هستند. سرطانها را بر اساس داشتن یا نداشتن این گیرندهها (پروتئینها) گیرنده هورمونی مثبت (hormone receptor-positive) یا گیرنده هورمونی منفی (hormone receptor- negative) مینامند.
دانستن وضعیت گیرنده هورمونی در تصمیم گیری برای انتخاب گزینههای درمانی مهم است. جلوگیری از اتصال این گیرندهها به هورمونها میتواند به جلوگیری از رشد و گسترش سرطان کمک کند. داروهایی وجود دارند که میتوان از آنها برای این کار استفاده کرد.
سلولهای سرطان سینه ممکن است یکی، هر دو یا هیچ یک از این گیرندهها را نداشته باشند:
- سرطان سینه ER مثبت (+ER) دارای گیرندههای استروژن هستند.
- سرطانهای پستان PR مثبت (+PR) دارای گیرندههای پروژسترون هستند.
وضعیت HER2/neu
در تعداد کمی از سرطانهای سینه در مردان، سلولها دارای مقدار زیادی پروتئین محرک رشد به نام HER2/neu هستند (اغلب به HER2 کوتاه میشود). به تومورهایی که سطح HER2/neu در آنها افزایش یافته است، HER2 مثبت میگویند. سلولها با داشتن کپیهای بیش از حد از ژن HER2/neu (معروف به تقویت ژن) به سرطان سینه HER2 مثبت تبدیل میشوند. سلولهای سرطانی با مقادیر بیش از حد نرمال پروتئین HER2/neu نسبت به سایر سرطانهای سینه به شدت رشد و گسترش مییابند.
همه سرطانهای پستان تازه تشخیص داده شده باید از نظر داشتن HER2/neu آزمایش شوند زیرا اگر داروهایی که پروتئین HER2/neu را هدف قرار میدهند، مانند تراستوزوماب (Herceptin) و lapatinib (Tykerb) به عنوان بخشی از درمان استفاده شوند، چشم انداز سرطانهای HER2 مثبت بهبود مییابد. برای دریافت اطلاعات بیشتر در مورد داروهایی که این پروتئین را هدف قرار میدهند، به مبحث درمان هدفمند (Targeted Therapy) برای سرطان سینه در مردان مراجعه کنید.
نمونه بیوپسی یا جراحی معمولاً به یکی از دو روش زیر آزمایش میشود:
- ایمونوهیستوشیمی (Immunohistochemistry یا IHC): در این آزمایش آنتی بادیهای ویژه ای که پروتئین HER2/neu را شناسایی میکنند روی نمونه اعمال میشوند که در صورت وجود سطوح غیر طبیعی بالا تغییر رنگ ایجاد کنند. نتایج آزمایش به صورت 0، 1+، 2+ یا 3+ گزارش میشود.
- هیبریداسیون در محل فلورسنت (Fluorescent in situ hybridization یا FISH): این آزمایش از قطعات فلورسنت DNA استفاده میکند که به طور خاص به نسخههایی از ژن HER2/neu در سلولها میچسبند و سپس میتوان آنها را زیر میکروسکوپ ویژه ای شمارش کرد.
بسیاری از متخصصان سرطان سینه فکر میکنند که آزمایش FISH نتایج دقیقتری نسبت به IHC به ما میدهد اما این آزمایش گرانتر است و دریافت نتایج در آن بیشتر طول میکشد. اغلب در ابتدا آزمایش IHC استفاده میشود.
- اگر نتایج 1+ (یا 0) باشند، سرطان HER2 منفی در نظر گرفته میشود. افراد مبتلا به تومورهای HER2 منفی با داروهایی که HER2 را هدف قرار میدهند، درمان نمیشوند.
- اگر آزمایش 3+ باشد، سرطان HER2 مثبت است. افراد مبتلا به تومورهای HER2 مثبت ممکن است با داروهایی که HER2 را هدف قرار میدهند، درمان شوند.
- هنگامی که نتیجه 2+ باشد، وضعیت HER2 تومور مشخص نیست و سپس تومور با FISH آزمایش میشود. برخی از موسسات همچنین از FISH برای تایید وضعیت HER2 که توسط IHC 3+ است، استفاده میکنند و برخی فقط FISH را انجام میدهند.
نوع جدیدتری از آزمایش که به عنوان هیبریداسیون در محل کروموژنیک (CISH یا chromogenic in situ hybridization) شناخته میشود، با استفاده از پروبهای کوچک DNA برای شمارش تعداد ژنهای HER2 در سلولهای سرطان سینه، مشابه FISH عمل میکند. اما این آزمایش به میکروسکوپ خاصی نیاز ندارد و به دنبال تغییرات رنگی (نه فلورسانس) است که ممکن است هزینه آن را کاهش دهد. در حال حاضر، از این روش به اندازه IHC یا FISH استفاده نمیشود.
طبقه بندی سرطان سینه بر اساس گیرندههای هورمونی و وضعیت HER2
پزشکان اغلب سرطانهای مهاجم سینه را بر اساس وجود گیرندههای هورمونی (ER و PR) و اینکه آیا سرطان جهش HER2 را به میزان بیش از حدی دارد یا نه، به گروههایی تقسیم میکنند.
گیرنده هورمونی مثبت (Hormone receptor-positive): اگر سلولهای سرطان سینه حاوی گیرندههای استروژن یا پروژسترون باشند، میتوان آنها را گیرنده هورمونی مثبت (یا فقط هورمون مثبت) نامید. سرطان سینه در مردانی که گیرنده هورمونی مثبت دارند را میتوان با داروهای هورمون درمانی که سطح استروژن را کاهش میدهند، گیرندههای استروژن را مسدود میکنند یا بر سطح آندروژن (هورمون مردانه) تأثیر میگذارند، درمان میشود (به مبحث هورمون درمانی برای سرطان سینه در مردان مراجعه کنید).
این روش شامل سرطانهایی میشود که ER منفی اما PR مثبت هستند. سرطانهای گیرنده هورمونی مثبت نسبت به سرطانهایی که گیرنده هورمونی منفی هستند (و گیرندههای استروژن یا پروژسترون ندارند) کندتر رشد میکنند. بیماران مبتلا به این سرطانها در کوتاه مدت چشم انداز بهتری دارند اما سرطانهایی که گیرنده هورمونی مثبت هستند، گاهی ممکن است سالها پس از درمان عود کنند. حدود 9 مورد از هر 10 سرطان سینه مردانه گیرنده هورمونی مثبت هستند.
گیرنده هورمونی منفی (Hormone receptor-negative): اگر سلولهای سرطانی پستان گیرندههای استروژن یا پروژسترون نداشته باشند، گفته میشود که گیرنده هورمونی منفی هستند (یا فقط هورمون منفی). درمان با داروهای هورمون درمانی برای این سرطانها مفید نیست. این سرطانها نسبت به سرطانهای گیرنده هورمونی مثبت سریع تر رشد میکنند. اگر این نوع سرطانها بعد از درمان دوباره عود کنند، این اتفاق بیشتر در چند سال اول رخ میدهد.
HER2 مثبت: سرطانهایی که پروتئین یا ژن HER2 را به میزان بیش از حدی دارند HER2 مثبت نامیده میشوند. این سرطانها را میتوان با داروهایی که HER2 را هدف قرار میدهند، درمان کرد.
HER2 منفی: سرطانهایی که ژن HER2 را به میزان اضافی ندارند، HER2 منفی نامیده میشوند. این سرطانها به درمان با داروهایی که HER2 را هدف قرار میدهند، پاسخ نمیدهند.
سه گانه منفی (Triple-negative): اگر سلولهای سرطانی پستان گیرندههای استروژن یا پروژسترون و HER2 بیش از حد نداشته باشند، سه گانه منفی نامیده میشوند (HER2 منفی، ER منفی و PR منفی).
سرطان سینه سه گانه منفی نسبت به سایر انواع سرطان پستان سریع تر رشد و گسترش مییابد. از آن جایی که سلولهای تومور گیرندههای هورمونی ندارند، هورمون درمانی برای درمان این سرطانها مفید نیست. همچنین از آن جایی که آنها HER2 زیادی نیز ندارند، داروهایی که HER2 را هدف قرار میدهند، نیز مفید نیستند. شیمی درمانی هنوز هم برای این سرطانها میتواند مفید باشد.
سه گانه مثبت (Triple-positive): این اصطلاح برای توصیف سرطانهایی استفاده میشود که ER مثبت، PR مثبت و دارای HER2 بیش از حد هستند. این سرطانها را میتوان با داروهای هورمونی و همچنین داروهایی که HER2 را هدف قرار میدهند، درمان کرد.
سایر آزمایشات آزمایشگاهی
آزمایشات پلوئیدی (Tests of ploidy) و سرعت تکثیر سلولی
یافتن اطلاعات بیشتر در مورد DNA در سلولهای سرطان سینه میتواند به پیش بینی سرعت تقسیم و رشد سلولهای سرطانی کمک کند.
پلوئیدی سلولهای سرطانی به مقدار DNA آنها اشاره دارد.
- اگر مقدار طبیعی DNA در سلولها وجود داشته باشد، گفته میشود که آنها دیپلوئید (diploid) هستند. این سرطانها تمایل به رشد و انتشار کندتری دارند.
- اگر مقدار DNA غیر طبیعی باشد، سلولها به عنوان آنیوپلوئید (aneuploid) توصیف میشوند. این سرطانها تهاجمیتر هستند و سریعتر نیز رشد و گسترش مییابند.
آزمایشات پلوئیدی ممکن است به تعیین چشم انداز (نتیجه) کمک کند اما به ندرت درمان را تغییر میدهند و بنابراین اختیاری در نظر گرفته میشوند. آنها معمولاً به عنوان بخشی از یک روند درمانی معمول سرطان سینه توصیه نمیشوند.
تکثیر سلولی سرعتی است که یک سلول سرطانی در طی آن DNA خود را کپی میکند و به 2 سلول تقسیم میشود. اگر سلولهای سرطانی با سرعت بیشتری تقسیم شوند، به این معنی است که سرطان سریع تر رشد میکند یا تهاجمی تر است.
DNA زمانی کپی میشود که سلول در حال آماده شدن برای تقسیم به 2 سلول جدید است. کسر فاز S درصدی از سلولها در یک نمونه است که DNA خود را کپی میکنند. میزان تقسیم سلولی سرطانی را میتوان با آزمایش Ki-67 نیز تخمین زد. اگر کسر فاز S یا تست Ki-67 بالا باشد، به این معنی است که سلولهای سرطانی با سرعت بیشتری تقسیم میشوند که میتواند نشان دهنده سرطان تهاجمی تر باشد.
تستهای بیان ژن
آزمایشهایی که الگوهای برخی از ژنها (که گاهی به عنوان پروفایل بیان ژن – gene expression profiling – نیز نامیده میشوند) را بررسی میکنند، میتوانند به پیش بینی اینکه آیا احتمال بازگشت سرطان پستان موجود در مراحل اولیه (مرحله 1 یا 2) پس از درمان اولیه وجود دارد یا خیر، کمک کند. پزشکان میتوانند از این اطلاعات استفاده کنند تا بدانند چه کسانی به احتمال زیاد از شیمی درمانی پس از جراحی سینه سود میبرند.
Oncotype DX و MammaPrint نمونههایی از آزمایشهایی هستند که مجموعههای مختلف ژنهای سرطان سینه را بررسی میکنند. تستهای بیشتری در حال توسعه وجود دارد. آزمایشهایی مانند این بخشی از روندی است که “پزشکی شخصی یا personalized medicine” نامیده میشود – یادگیری بیشتر در مورد سرطان خود برای تنظیم کردن خاص روند درمانی شما.
اطلاعات بیشتری برای تصمیم گیری در مورد مفید بودن این آزمایش برای سرطان سینه در مردان مورد نیاز است اما دادههای کافی وجود دارد که نشان میدهند این آزمایش میتواند به مردان مبتلا به سرطان سینه در مراحل اولیه کمک کند تا در مورد انتخاب شیمی درمانی پس از جراحی تصمیم بگیرند. از پزشک خود بپرسید که آیا این آزمایشات ممکن است برای شما مناسب باشند یا خیر.
آزمایشاتی برای بررسی شیوع سرطان سینه در مردان
اگر سرطان سینه برای شما تشخیص داده شده است و پزشک فکر میکند سرطان ممکن است با توجه به علائم، نتایج معاینه فیزیکی یا اندازه تومور گسترش یافته باشد، ممکن است به آزمایشهای بیشتری نیاز داشته باشید. پزشک با شما در مورد هر کدام از این آزمایشات (در صورت وجود) که به آنها نیاز دارید صحبت خواهد کرد.
اشعه ایکس قفسه سینه
این آزمایش ممکن است برای بررسی اینکه آیا سرطان سینه به ریهها سرایت کرده است یا خیر، انجام شود.
اسکن توموگرافی کامپیوتری (CT یا Computed tomography)
سی تی اسکن از اشعه ایکس گرفته شده از زوایای مختلف استفاده میکند که توسط کامپیوتر برای ایجاد تصاویر دقیق از اندامها ترکیب میشوند. این آزمایش اغلب برای بررسی قفسه سینه و یا شکم (abdomen) استفاده میشود تا متوجه شوند که آیا سرطان سینه به سایر اندامها گسترش یافته است یا خیر. همچنین میتوان از آن برای هدایت سوزن بیوپسی به ناحیه مورد نظر استفاده کرد.
اسکن تصویر برداری رزونانس مغناطیسی (Magnetic resonance imaging یا MRI)
اسکن MRI با استفاده از امواج رادیویی و آهنرباهای قوی به جای اشعه ایکس، تصاویر دقیقی ایجاد میکند. این آزمایش میتواند برای بررسی مغز و نخاع شما مفید باشد. ام آر آی میتواند ناراحت کننده تر از سی تی اسکن باشد زیرا مدت زمان بیشتری طول میکشد و اغلب لازم است در حین انجام آزمایش در یک دستگاه لوله مانند و باریک دراز بکشید.
سونوگرافی (Ultrasound)
برای سونوگرافی، یک دستگاه که امواج صوتی را منتشر میکند روی پوست حرکت میکند تا از داخل بدن عکس بگیرد. اغلب ابتدا یک ژل روی پوست شما مالیده میشود. از این آزمایش میتوان برای تشخیص سرطان سینه استفاده کرد اما همچنین میتواند برای بررسی سرطانی که به سایر قسمتهای بدن گسترش یافته است نیز استفاده شود.
از سونوگرافی شکم میتوان برای یافتن تومورها در کبد یا سایر اندامهای شکمی استفاده کرد.
اسکن استخوان (Bone scan)
اسکن استخوان میتواند به نشان دادن متاستاز (گسترش) سرطان به استخوانها کمک کند. این روش میتواند تمام استخوانهای بدن را به طور همزمان نشان دهد و میتواند مناطق کوچکی از سرطان را پیدا کند که در اشعه ایکس ساده دیده نمیشوند.
تغییرات استخوانی به صورت ” hot spots” روی اسکلت شما ظاهر میشود. آنها رادیو اکتیویته را جذب میکنند. این نواحی ممکن است نشان دهنده سرطان متاستاتیک (metastatic cancer) باشند اما آرتریت (arthritis) یا سایر بیماریهای استخوانی نیز میتوانند همین الگو را ایجاد کنند. برای تمایز بین این عارضهها، تیم مراقبت از سرطان شما ممکن است از آزمایشهای تصویر برداری دیگری مانند اشعه ایکس ساده یا سی تی اسکن، ام آر آی یا اسکن PET برای مشاهده بهتر نواحی غیر طبیعی استفاده کنند یا حتی ممکن است نمونههای بیوپسی از استخوان بگیرند.
اسکن توموگرافی گسیل پوزیترون (PET یا Positron emission tomography)
برای این آزمایش، نوعی قند رادیو اکتیو وارد رگ میشود و در سراسر بدن حرکت میکند. سلولهای سرطانی مقادیر بالایی از این قند را جذب میکنند. سپس یک دوربین ویژه عکسهایی را میگیرد که نواحی تجمع قند در بدن را نشان میدهد.
اسکن PET زمانی مفید است که پزشک فکر میکند سرطان ممکن است گسترش یافته باشد اما نمیداند که دقیقا به کجا گسترش یافته است. تصویر به اندازه یک سی تی اسکن یا ام آر آی جزئیات دقیقی ندارد اما میتواند اطلاعات مفیدی در مورد کل بدن شما ارائه دهد. برخی از دستگاهها میتوانند هر دو اسکن PET و CT را به طور همزمان انجام دهند (PET/CT scan). رادیولوژیست میتواند نواحی با رادیو اکتیویته بالاتر در PET را با ظاهر آن ناحیه در CT مقایسه کند.
این آزمایش میتواند در جستجوی سرطانی که به اندامهای دور گسترش یافته است، مفید باشد اما در جستجوی تودههای کوچک سلولهای سرطانی در غدد لنفاوی زیر بازو (غدد لنفاوی زیر بغل) مفید نیست.
مراحل سرطان سینه در مردان
پس از تشخیص سرطان سینه در فردی، پزشکان سعی میکنند بفهمند که آیا این سرطان گسترش یافته است یا خیر و اگر چنین است، این گسترش تا چه حد است. این فرآیند مرحله بندی (staging) نامیده میشود. مرحله سرطان، میزان سرطان در بدن را توصیف میکند. این کار به تعیین اینکه سرطان چقدر جدی است و بهترین روش درمان آن کمک میکند. پزشکان همچنین هنگام صحبت در مورد آمار بقا و زنده مانی از مرحله سرطان استفاده میکنند.
سیستم مرحله بندی مورد استفاده برای سرطان سینه در مردان همان سیستمی است که برای سرطان سینه در زنان استفاده میشود.
مراحل اولیه سرطان سینه مرحله 0 (سرطان در محل) است. سپس این مراحل از مرحله I (1) تا IV (4) متغیر هستند. به عنوان یک قاعده، هرچه این عدد کمتر باشد، سرطان کمتر گسترش یافته است. عدد بالاتر، مانند مرحله IV، به معنای گسترش بیشتر سرطان است. در یک مرحله، حرف قبلی به معنای مرحله پایین تر است.
مرحله چگونه تعیین میشود؟
سیستم مرحله بندی که اغلب برای سرطان پستان استفاده میشود، سیستم TNM کمیته مشترک آمریکایی سرطان (AJCC) است که بر اساس 7 اطلاعات کلیدی عمل میکند:
- وسعت (اندازه) تومور (T): اندازه سرطان چقدر است؟ آیا در مناطق مجاور رشد کرده است؟
- گسترش به غدد لنفاوی مجاور (N): آیا سرطان به غدد لنفاوی مجاور سرایت کرده است؟ اگر چنین است، این گسترش تا چه حد است؟
- گسترش (متاستاز) به نقاط دور دست (M): آیا سرطان به اندامهای دور مانند ریهها یا کبد گسترش یافته است؟
- وضعیت گیرنده استروژن (ER): آیا سرطان پروتئینی به نام گیرنده استروژن را دارد؟
- وضعیت گیرنده پروژسترون (PR): آیا سرطان پروتئینی به نام گیرنده پروژسترون را دارد؟
- وضعیت HER2/neu (HER2): آیا سرطان به میزان بیش از حدی پروتئینی به نام HER2 را میسازد؟
- درجه سرطان (G): سلولهای سرطانی چقدر شبیه سلولهای طبیعی هستند؟
نتایج درجه عود Oncotype Dx (Oncotype Dx Recurrence Score) نیز ممکن است در شرایط خاص در تعیین مرحله در نظر گرفته شوند.
جدید ترین سیستم AJCC که در ژانویه 2018 اجرا شد، هم دارای سیستمهای مرحله بندی بالینی (clinical) و هم پاتولوژیک (pathologic) برای سرطان سینه است. مرحله پاتولوژیک (که مرحله جراحی – surgical stage – نیز نامیده میشود) با بررسی بافت برداشته شده در طول عمل جراحی تعیین میشود.
گاهی اوقات، اگر بررسی بافت بلافاصله در حین جراحی یا اصلا امکان پذیر نباشد، به جای آن به سرطان یک مرحله بالینی داده میشود. این مرحله بر اساس نتایج یک معاینه فیزیکی، بیوپسی و آزمایشات تصویر برداری است. مرحله بالینی برای کمک به برنامه ریزی روند درمانی استفاده میشود. با این حال، گاهی اوقات سرطان فراتر از تخمینهای مرحله بالینی گسترش یافته است و ممکن است چشم انداز بیمار را به دقت یک مرحله پاتولوژیک پیش بینی نکند.
اعداد یا حروف بعد از T، N و M جزئیات بیشتری در مورد هر یک از این عوامل ارائه میدهند. اعداد بالاتر به معنای پیشرفته تر بودن سرطان است. هنگامی که دسته بندی T، N، و M فرد و همچنین وضعیت ER، PR، HER2 و درجه سرطان مشخص شد، این اطلاعات در فرآیندی به نام گروه بندی مرحله ای (stage grouping) ترکیب میشوند تا یک مرحله کلی را تعیین کنند. توضیحات تفصیلی دسته بندیهای TNM در زیر مشاهده میشود. افزودن اطلاعات مربوط به وضعیت ER، PR و HER2 به همراه درجه، گروه بندی مرحله ای را پیچیده کرده است، بنابراین بهتر است از پزشک خود در مورد مرحله خاص خود و معنای آن سؤال کنید.
جزئیات سیستم مرحله بندی TNM
دسته بندی T برای سرطان سینه
T و به دنبال آن عددی از 0 تا 4 اندازه تومور اصلی (اولیه) و اینکه آیا به پوست یا دیواره قفسه سینه زیر سینه گسترش یافته است یا خیر را توصیف میکند. اعداد T بالاتر به معنای تومور بزرگتر و یا گسترش وسیع تر به بافتهای نزدیک سینه است.
TX: تومور اولیه قابل ارزیابی نیست.
T0: شواهدی از تومور اولیه وجود ندارد.
Tis: کارسینوم در محل (DCIS یا بیماری پاژه نوک پستان بدون توده توموری مرتبط)
T1 (شامل T1a، T1b و T1c): عرض تومور 2 سانتی متر (3/4 اینچ) یا کمتر است.
T2: تومور بیش از 2 سانتی متر است اما عرض آن از 5 سانتی متر (2 اینچ) بیشتر نیست.
T3: عرض تومور بیش از 5 سانتی متر است.
T4 (شامل T4a، T4b، T4c و T4d): تومور با هر اندازه ای در دیواره قفسه سینه یا پوست رشد میکند. این نوع شامل سرطان سینه التهابی است.
دسته N برای سرطان سینه
N به دنبال عددی از 0 تا 3 نشان میدهد که آیا سرطان به غدد لنفاوی نزدیک پستان گسترش یافته است یا خیر و اگر چنین است، با چند مورد از غدد لنفاوی درگیر شده است.
مرحله بندی غدد لنفاوی برای سرطان سینه بر اساس نحوه شکل گرهها در زیر میکروسکوپ بوده و با پیشرفت تکنولوژی تغییر کرده است. روشهای جدیدتر امکان یافتن مجموعههای کوچکتر و کوچکتری از سلولهای سرطانی را فراهم کردهاند اما کارشناسان مطمئن نیستند که این رسوبات کوچک سلولهای سرطانی چقدر بر تعیین چشم انداز تأثیر میگذارند.
هنوز مشخص نیست که چه مقدار سرطان در غدد لنفاوی برای مشاهده تغییر در دیدگاه یا روند درمان مورد نیاز است. این موضوع هنوز در حال مطالعه است اما در حال حاضر، یک رسوب از سلولهای سرطانی باید حداقل شامل 200 سلول یا حداقل 0.2 میلی متر (کمتر از 1/100 اینچ) باشد تا بتواند مرحله N را تغییر دهد. ناحیه گسترش سرطان که کوچکتر از 0.2 میلی متر (یا کمتر از 200 سلول) است، مرحله را تغییر نمیدهد اما با اختصارات (+i یا +mol) ثبت میشود که نشان دهنده نوع آزمایش ویژه مورد استفاده برای یافتن میزان گسترش است.
اگر ناحیه گسترش سرطان حداقل 0.2 میلی متر (یا 200 سلول) باشد اما باز هم بزرگتر از 2 میلی متر نباشد، به آن میکرومتاستاز (micrometastasis) میگویند (یک میلی متر به اندازه عرض یک دانه برنج است).
میکرومتاستازها تنها در صورتی شمارش میشوند که مناطق وسیع تری از گسترش سرطان وجود نداشته باشد. مناطقی از سرطان گسترش یافته که بزرگتر از 2 میلی متر هستند، بر چشم انداز تأثیر میگذارند و مرحله N را تغییر میدهند. این مناطق بزرگتر گاهی اوقات ماکروماتاستاز (macrometastases) نامیده میشوند اما اغلب فقط با نام متاستاز شناخته میشوند.
NX: غدد لنفاوی مجاور را نمیتوان ارزیابی کرد (مثلاً اگر قبلاً برداشته شده باشند).
N0: سرطان به غدد لنفاوی مجاور سرایت نکرده است.
N0(i+): ناحیه گسترش سرطان شامل کمتر از 200 سلول و کوچکتر از 0.2 میلی متر است. مخفف “+i” به این معنی است که تعداد کمی از سلولهای سرطانی (به نام سلولهای توموری ایزوله یا isolated tumor cells) در تودههای رنگی معمولی یا زمانی که نوع خاصی از تکنیک رنگ آمیزی به نام ایمونوهیستوشیمی () استفاده میشود، دیده میشوند.
N0(mol+): سلولهای سرطانی را نمیتوان در غدد لنفاوی زیر بغل دید (حتی با استفاده از رنگهای خاص) اما ردپای سلولهای سرطانی با استفاده از تکنیکی به نام RT-PCR شناسایی شده است. RT-PCR یک آزمایش مولکولی است که میتواند تعداد بسیار کمی از سلولهای سرطانی را پیدا کند. (این آزمایش اغلب برای یافتن سلولهای سرطان سینه در غدد لنفاوی استفاده نمیشود زیرا نتایج بر تصمیم گیریهای درمانی تأثیری ندارد.)
N1: سرطان به 1 تا 3 غدد لنفاوی زیر بغل گسترش یافته است و یا مقادیر کمی سرطان در غدد لنفاوی پستانی داخلی (آنهایی که نزدیک استخوان سینه هستند) در بیوپسی غدد لنفاوی نگهبان یافت میشود.
N1mi: میکرومتاستازها (نواحی کوچک گسترش سرطان) در غدد لنفاوی زیر بازو دیده می شوند. نواحی گسترش سرطان در غدد لنفاوی حداقل 0.2 میلی متر عرض دارند اما بزرگتر از 2 میلی متر نیستند.
N1a: سرطان به 1 تا 3 غدد لنفاوی زیر بازو با حداقل یک ناحیه سرطانی با اندازه بیش از 2 میلی متر گسترش یافته است.
N1b: سرطان به غدد لنفاوی پستانی داخلی در همان سمت سرطان گسترش یافته است اما این گسترش فقط در بیوپسی غدد لنفاوی نگهبان یافت میشود (این امر باعث بزرگ شدن غدد لنفاوی نمیشود).
N1c: هر دو شرایط N1a و N1b اعمال میشوند.
N2: سرطان به 4 تا 9 مورد از غدد لنفاوی زیر بازو گسترش یافته است یا سرطان، غدد لنفاوی پستانی داخلی را بزرگ کرده است.
N2a: سرطان به 4 تا 9 مورد از غدد لنفاوی زیر بازو گسترش یافته است که حداقل یک ناحیه سرطانی بزرگتر از 2 میلی متر گسترش یافته است.
N2b: سرطان به یک یا چند مورد از غدد لنفاوی پستانی داخلی گسترش یافته و باعث بزرگ شدن آنها شده است.
N3: هر یک از موارد زیر میتواند صدق کند:
N3a:
سرطان به 10 مورد یا تعداد بیشتری از غدد لنفاوی زیر بغل گسترش یافته که حداقل در یک ناحیه سرطانی بیش از 2 میلی متر گسترش یافته است.
یا
سرطان به غدد لنفاوی زیر استخوان ترقوه (گرههای زیر ترقوه) گسترش یافته و حداقل در یک ناحیه سرطانی بیش از 2 میلی متر گسترش یافته است.
N3b:
سرطان حداقل در یکی از غدد لنفاوی زیر بغل (با حداقل یک ناحیه سرطانی بیشتر از 2 میلی متر) یافت میشود و غدد لنفاوی پستانی داخلی را بزرگ کرده است.
یا
سرطان به 4 مورد یا تعداد بیشتری از غدد لنفاوی زیر بغل گسترش یافته است (با حداقل یک ناحیه سرطانی که بیش از 2 میلی متر گسترش یافته) و مقادیر کمی سرطان در غدد لنفاوی پستانی داخلی در بیوپسی غدد لنفاوی نگهبان یافت میشود.
N3c: سرطان به غدد لنفاوی بالای استخوان ترقوه (گرههای فوق ترقوه) با حداقل یک ناحیه سرطانی با اندازه بیش از 2 میلی متر گسترش یافته است.
دستههای M برای سرطان سینه
M به دنبال اعداد 0 یا 1 نشان میدهد که آیا سرطان به اندامهای دور گسترش یافته است – به عنوان مثال، ریهها، کبد یا استخوانها.
M0: در اشعه ایکس (یا سایر آزمایشهای تصویر برداری) یا معاینه فیزیکی، هیچ گسترش دوری یافت نمیشود.
cM0(i+): تعداد کمی از سلولهای سرطانی در خون یا مغز استخوان (فقط با آزمایشهای ویژه تشخیص داده میشوند) و یا مناطق کوچک گسترش سرطان (حداکثر 0/2 میلیمتر) در غدد لنفاوی دور از زیر بغل، استخوان ترقوه، یا نواحی داخلی پستان، یافت میشوند.
M1: سرطان به اندامهای دور (اغلب به استخوانها، ریهها، مغز یا کبد) گسترش یافته است.
نمونههایی با استفاده از سیستم مرحله بندی جدید
مثال شماره 1
اگر اندازه سرطان بین 2 تا 5 سانتیمتر باشد (T2) اما به غدد لنفاوی مجاور (N0) یا اندامهای دور دست (M0) گسترش نیافته باشد:
- درجه 3
- HER2 منفی
- ER مثبت
- PR مثبت
مرحله سرطان IB است.
مثال شماره 2
اگر سرطان بزرگتر از 5 سانتی متر (T3) باشد و به 4 تا 9 غدد لنفاوی زیر بازو یا به هر غدد لنفاوی پستانی داخلی (N2) گسترش یافته باشد اما به اندامهای دور دست (M0) گسترش نیافته باشد:
- درجه 2
- HER2 مثبت
- ER مثبت
- PR مثبت
مرحله سرطان IB است.
مثال شماره 3
اگر سرطان بزرگتر از 5 سانتی متر (T3) باشد و به 4 تا 9 غدد لنفاوی زیر بازو یا به هر غدد لنفاوی پستانی داخلی (N2) گسترش یافته باشد اما به اندامهای دور دست (M0) گسترش نیافته باشد:
- درجه 2
- HER2 منفی
- ER منفی
- PR منفی
مرحله سرطان IIIB است.
میزان بقای (زنده مانی) سرطان سینه در مردان
میزان بقا میتواند به شما ایده دهد که چند درصد از افراد مبتلا به همان نوع و مرحله سرطان در مدت زمان معینی (معمولاً 5 سال) پس از تشخیص هنوز زنده هستند. این آمار نمیتوانند به شما بگویند که چقدر زنده خواهید ماند اما ممکن است به شما کمک کنند تا درک بهتری از میزان احتمال موفقیت روند درمانیتان داشته باشید.
به خاطر داشته باشید که میزان بقا تخمینی است و اغلب بر اساس نتایج قبلی تعداد زیادی از افرادی است که سرطان خاصی داشته اند اما این اعداد نمیتوانند پیش بینی کنند که در مورد فرد خاصی چه اتفاقی خواهد افتاد. این آمار میتواند گیج کننده باشد و ممکن است شما را به پرسیدن سوالات بیشتری سوق دهد. با پزشک خود در مورد چگونگی اعمال این اعداد برای خود صحبت کنید زیرا او با وضعیت شما آشنا است.
نرخ بقای نسبی 5 ساله چیست؟
نرخ بقای نسبی، افراد مبتلا به همان نوع و مرحله سرطان را با افراد موجود در کل جمعیت مقایسه میکند. به عنوان مثال، اگر میزان بقای نسبی 5 ساله برای مرحله خاصی از سرطان سینه در مردان 80 درصد باشد، به این معنی است که احتمال ابتلا به آن سرطان در مردانی که به آن سرطان مبتلا هستند، به طور متوسط 80 درصد نسبت به مردانی هستند که به آن سرطان مبتلا نیستند.
این نرخ زنده مانی برای یک سرطان تا حداقل 5 سال پس از تشخیص ابتلا است. در واقع معنای اصلی این عدد این است که احتمال زنده ماندن فرد مبتلا به سرطان تا 5 سال آینده پس از تشخیص 80 درصد میباشد.
این اعداد از کجا میآیند؟
انجمن سرطان آمریکا به اطلاعات پایگاه داده SEER که توسط موسسه ملی سرطان (NCI) نگهداری میشود، برای ارائه آمار بقای انواع مختلف سرطان متکی است.
پایگاه داده SEER نرخ بقای نسبی 5 ساله سرطان سینه را در مردان در ایالات متحده بر اساس میزان گسترش سرطان بررسی میکند. با این حال، پایگاه داده SEER سرطانها را بر اساس مراحل AJCC TNM (مرحله 1، مرحله 2، مرحله 3، و غیره) گروه بندی نمیکند. در عوض، سرطانها را به مراحل موضعی، منطقه ای و دور دسته بندی میکند:
- موضعی (Localized): هیچ نشانه ای از گسترش سرطان به خارج از سینه وجود ندارد.
- منطقه ای (Regional): سرطان در خارج از پستان به ساختارها یا غدد لنفاوی مجاور گسترش یافته است.
- دور (Distant): سرطان به نقاط دورتر بدن مانند ریهها یا مغز گسترش یافته است.
نرخ بقای نسبی 5 ساله برای سرطان سینه در مردان
این اعداد بر اساس اطلاعات مردانی است که بین سالهای 2011 تا 2017 به سرطان سینه مبتلا شدهاند.
درک اعداد
- این اعداد فقط برای مرحله سرطان در هنگام اولین تشخیص صدق میکنند. اگر سرطان رشد کند، گسترش یابد یا پس از درمان عود کند، دیگر اعمال نمیشوند.
- این اعداد همه چیز را در نظر نمیگیرند. میزان بقا بر اساس میزان گسترش سرطان گروه بندی میشود. اما عوامل دیگری مانند سن و سلامت کلی شما، اینکه آیا سلولهای سرطانی تغییرات ژنی یا پروتئینی خاصی دارند و اینکه سرطان چگونه به درمان پاسخ میدهد نیز میتواند بر دیدگاه شما تأثیر بگذارد.
- مردانی که اکنون مبتلا به سرطان سینه تشخیص داده میشوند، ممکن است چشم انداز بهتری نسبت به این اعداد داشته باشند. درمانها با گذشت زمان بهبود مییابند و این اعداد بر اساس اطلاعات مردانی هستند که حداقل 5 سال زودتر مبتلا به این بیماری تشخیص داده شده و درمان شده اند.
درمان سرطان سینه در مردان
درمانهای محلی (Local treatments)
برخی از درمانها درمانهای موضعی نامیده میشوند، به این معنی که تومور را بدون تأثیر بر بقیه بدن درمان میکنند. این درمانها بیشتر برای سرطانهای مرحله اولیه (کمتر پیشرفته) مفید هستند، اگرچه ممکن است در برخی موقعیتهای دیگر نیز استفاده شوند. انواع درمان موضعی مورد استفاده برای سرطان سینه عبارتند از:
جراحی (Surgery) سرطان سینه در مردان
اکثر مردان مبتلا به سرطان سینه نوعی جراحی را به عنوان بخشی از درمان خود انجام میدهند. جراحی سینه انواع مختلفی دارد و بسته به شرایط ممکن است به دلایل مختلفی نیز انجام شود. به عنوان مثال، ممکن است جراحی برای موارد زیر انجام شود:
- تا حد امکان سرطان را حذف کرده و بردارند (جراحی حفظ پستان یا ماستکتومی یا mastectomy)
- بررسی کنند که آیا سرطان به غدد لنفاوی زیر بازو گسترش یافته است (بیوپسی غدد لنفاوی نگهبان یا تشریح غدد لنفاوی زیر بغل)
- علائم سرطان پیشرفته را از بین ببرند
پزشک ممکن است بر اساس ویژگیهای سرطان سینه و سابقه پزشکی شما، عمل خاصی را توصیه کند یا ممکن است انتخابی در مورد نوع انجام آن داشته باشید. مهم است که گزینههای خود را بدانید تا بتوانید در مورد آنها با پزشکتان صحبت کنید و انتخاب مناسب خود را انجام دهید.
جراحی برای برداشتن سرطان سینه
دو نوع جراحی اصلی برای برداشتن سرطان سینه وجود دارد:
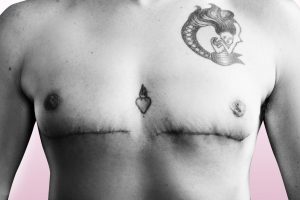
ماستکتومی (Mastectomy) – جراحی که در آن کل پستان، از جمله تمام بافت سینه و گاهی دیگر بافتهای مجاور برداشته میشود. اکثر مردان مبتلا به سرطان سینه تحت ماستکتومی قرار میگیرند زیرا مردان دارای مقدار کمی بافت پستان هستند.
انواع مختلفی از ماستکتومی وجود دارد:
- در ماستکتومی ساده یا کامل، جراح کل سینه از جمله نوک سینه را برمی دارد، اما غدد لنفاوی زیر بغل یا بافت ماهیچه ای زیر سینه را بر نمیدارد.
- در ماستکتومی رادیکالی اصلاح شده (modified radical mastectomy)، جراح برش ایجاد را گسترش میدهد تا کل سینه و غدد لنفاوی زیر بازو را نیز بردارد.
- اگر تومور بزرگ است و در عضلات قفسه سینه رشد میکند، جراح باید یک ماستکتومی رادیکال انجام دهد، یک عمل گسترده تر که کل سینه، غدد لنفاوی زیر بغل و عضلات دیواره قفسه سینه زیر سینه را خارج میکند. این جراحی تنها در صورتی لازم است که سرطان به عضلات سینه ای زیر گسترش یافته باشد.
جراحی حفظ پستان (BCS یا Breast-conserving surgery) (همچنین لامپکتومی (lumpectomy)، کوادرانکتومی (quadrantectomy)، ماستکتومی جزئی (partial mastectomy) یا ماستکتومی سگمنتال (segmental mastectomy) نیز نامیده میشود) جراحی است که در آن فقط بخشی از پستان که حاوی سرطان است برداشته میشود. هدف از بین بردن سرطان و همچنین برخی از بافتهای طبیعی اطراف آن است. اینکه چه مقدار از سینه برداشته شود به اندازه و محل تومور و سایر عوامل بستگی دارد.
BCS معمولاً برای درمان زنان مبتلا به سرطان سینه استفاده میشود. این روش در مردان کمتر مورد استفاده قرار میگیرد زیرا اکثر سرطانهای سینه مردانه در پشت نوک پستان قرار دارند و بارها به نوک پستان نفوذ یافته اند که نیاز به جراحی گسترده تری مانند ماستکتومی دارد. اگر BCS انجام شود، معمولاً با پرتو درمانی دنبال میشود.
عوارض احتمالی جراحی سینه
به غیر از درد پس از جراحی، تورم موقت و تغییر در ظاهر پستان، عوارض احتمالی جراحی شامل خونریزی و عفونت در محل جراحی، هماتوم (hematoma، جمع شدن خون در زخم) و سروما (seroma، تجمع مایع شفافی در زخم) است.
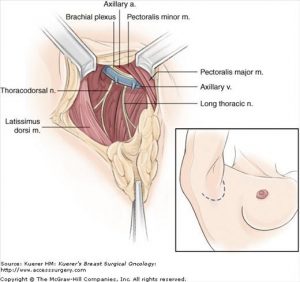
جراحی برای برداشتن غدد لنفاوی مجاور
برای فهمیدن اینکه آیا سرطان سینه به غدد لنفاوی زیر بغل گسترش یافته است، ممکن است یک یا چند مورد از این غدد لنفاوی برداشته شده و در آزمایشگاه بررسی شوند. این مرحله بخش مهمی از تشخیص مرحله (وسعت) سرطان است.
غدد لنفاوی ممکن است به عنوان بخشی از جراحی برای برداشتن سرطان سینه یا به عنوان یک عمل جداگانه برداشته شوند.
دو نوع اصلی جراحی برای برداشتن غدد لنفاوی عبارتند از:
- بیوپسی غدد لنفاوی نگهبان (Sentinel lymph node biopsy یا SLNB) – روشی که در آن جراح فقط گره(های) لنفاوی زیر بازو را که احتمالاً سرطان به آنها گسترش مییابد، بر میدارد. برداشتن تنها یک یا چند مورد از غدد لنفاوی خطر عوارض جانبی ناشی از جراحی را کاهش میدهد.
- تشریح غدد لنفاوی زیر بغل (ALND یا Axillary lymph node dissection) – روشی که در آن جراح بسیاری از (معمولاً کمتر از 20) غدد لنفاوی را از زیر بازو خارج میکند. ALND به میزانی که در گذشته انجام میشد، انجام نمیشود اما همچنان ممکن است بهترین راه برای بررسی غدد لنفاوی در برخی شرایط باشد.
معمولاً هر یک از این روشها میتوانند همزمان با ماستکتومی یا لامپکتومی انجام شوند اما ممکن است در یک عمل دومی نیز انجام شوند.
برای بیوپسی غدد لنفاوی نگهبان (نوعی از بیوپسی که اغلب انجام میشود)، جراح گره (یا گرههای) نگهبان را پیدا کرده و بر میدارد – اولین گره (گرههای) لنفاوی که تومور به داخل آن نفود کرده و گره یا گرههایی که به احتمال زیاد حاوی آن هستند درحالتی که سلولهای سرطانی شروع به گسترش کرده باشند.
برای انجام این کار، جراح یک ماده رادیو اکتیو و یا یک رنگ آبی را به ناحیه اطراف تومور، به پوست روی تومور یا به بافتهای قرار گرفته درست زیر آرئول (ناحیه رنگی اطراف نوک پستان) تزریق میکند. عروق لنفاوی این مواد را طی چند ساعت آینده به گره(های) نگهبان میبرند.
پزشک میتواند از یک دستگاه مخصوص برای تشخیص رادیو اکتیویته در گرهها استفاده کرده یا میتواند غدد لنفاوی آبی شده را پیدا کند. (اینها راههای جداگانهای برای یافتن گرههای نگهبان هستند اما اغلب با هم و به عنوان یک بررسی مضاعف انجام میشوند.) سپس پزشک یک برش (incision) در پوست ناحیه زیر بغل ایجاد میکند و گرهها را خارج میکند. سپس این گرهها (اغلب 2 یا 3 عدد) در آزمایشگاه بررسی میشوند.
گاهی اوقات میتوان غده لنفاوی را از نظر سرطانی بودن در طی جراحی بررسی کرد. اگر سرطان در غدد لنفاوی نگهبان (sentinel lymph node) یافت شود، جراح ممکن است یک ALND کامل را انجام دهد. اگر در زمان جراحی هیچ سلول سرطانی در غده لنفاوی دیده نشد یا اگر غدد نگهبان در حین جراحی بررسی نشدند، غدد لنفاوی در چند روز آینده با دقت بیشتری مورد بررسی قرار خواهند گرفت. اگر سرطان در غدد لنفاوی یافت شود، جراح ممکن است ALND کامل را در زمان روند بعدی توصیه کند.
اگر هیچ سلول سرطانی در گره(های نگهبان) وجود نداشته باشد، بعید است که سرطان به سایر غدد لنفاوی سرایت کرده باشد، بنابراین نیازی به جراحی بیشتر غدد لنفاوی نیست. این امر به شما امکان میدهد تا از برخی از عوارض جانبی بالقوه ALND به شکل کامل جلوگیری کنید.
بیوپسی غدد لنفاوی نگهبان همیشه مناسب نیست. اگر غده لنفاوی زیر بغل با لمس یا آزمایشی مانند سونوگرافی بزرگ یا غیر طبیعی به نظر برسد، ممکن است با آسپیراسیون با سوزن ظریف بررسی شوند. در صورت یافتن سرطان، ALND کامل توصیه میشود و نیازی به بیوپسی گره نگهبان نیست.
بیوپسی غدد لنفاوی نگهبان یک تکنیک پیچیده است که به مهارت زیادی نیاز دارد. این روش فقط باید توسط یک تیم جراحی با تجربه در این تکنیک انجام شود. اگر به انجام این نوع بیوپسی فکر میکنید، از تیم مراقبتهای پزشکی خود بپرسید که آیا این روشی است که آنها به طور منظم انجام میدهند یا خیر.
عوارض جانبی احتمالی جراحی غدد لنفاوی
مانند سایر عملها، درد، تورم، خونریزی و عفونت امکان پذیر است.
ادم لنف (Lymphedema): یک اثر طولانی مدت احتمالی برداشتن غدد لنفاوی زیر بغل، ادم (ورم) لنف بازو است. این پدیده به این دلیل است که هر مایع اضافی در بازوها معمولاً از طریق سیستم لنفاوی به جریان خون باز میگردد. برداشتن غدد لنفاوی گاهی اوقات باعث مسدود شدن راه بازو شده و باعث تجمع این مایع میشود.
این عارضه جانبی در مردان به خوبی مورد مطالعه قرار نگرفته است اما تصور میشود که خطر ابتلا به آن در محدوده 3-7 درصد در زنان دارای SLNB و حدود 20-30 درصد در زنان مبتلا به ALND باشد. به نظر میرسد که اگر پس از جراحی پرتو داده شود، ادم لنف شایع تر است.
گاهی اوقات این بیماری بلافاصله پس از جراحی شروع میشود اما همچنین ممکن است مدت زیادی طول بکشد تا رخ دهد. برای برخی افراد، تورم تنها چند هفته طول میکشد و سپس از بین میرود. در موارد دیگر، تورم مدت زیادی طول میکشد. اگر بازوی شما بعد از جراحی دارای غدد لنفاوی متورم، سفت یا دردناک است، حتماً فوراً به یکی از افراد تیم مراقبت سرطان خود اطلاع دهید.
محدودیت حرکت بازو و شانه: همچنین ممکن است پس از جراحی حرکت محدودی در بازو و شانه خود داشته باشید. این عارضه بعد از ALND بیشتر از SLNB رخ میدهد. پزشک ممکن است تمریناتی را به شما بدهد تا مطمئن شود که مشکل دائمی در حرکت شانه خود (شانه یخ زده) ندارید.
برخی از بیماران متوجه ساختار طناب مانندی میشوند که از زیر بازو شروع میشود و میتواند به سمت آرنج ادامه یابد. این عارضه گاهی اوقات سندرم شبکه ای زیر بغل () یا بند ناف لنفاوی (lymphatic cording) نامیده میشود. این عارضه بعد از ALND شایع تر از SLNB است. علائم ممکن است هفتهها یا حتی ماهها پس از جراحی ظاهر نشوند. این وضعیت میتواند باعث درد شود و حرکت بازو و شانه را محدود کند. اغلب بدون درمان از بین میرود، اگرچه به نظر میرسد برخی افراد فیزیوتراپی را برای رفع این مشکل مفید میدانند.
بی حسی: بی حسی پوست بالای بازو، یکی دیگر از عوارض جانبی رایج است زیرا عصبی که در اینجا حس را کنترل میکند از ناحیه غدد لنفاوی عبور میکند.
درد مزمن بعد از جراحی سینه
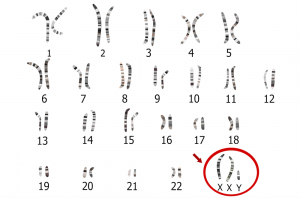
برخی از بیماران پس از جراحی مشکلاتی با درد عصبی (نوروپاتیک یا neuropathic) در دیواره قفسه سینه، زیر بغل و یا بازو دارند که با گذشت زمان از بین نمیرود. این عارضه، سندرم درد پس از ماستکتومی (post-mastectomy pain syndrome یا PMPS) نامیده میشود زیرا اولین بار در زنانی که ماستکتومی انجام داده بودند، توصیف شد اما پس از روند درمانی حفظ پستان نیز رخ میدهد.
تصور میشود که PMPS با آسیب وارد شده به اعصاب زیر بغل و قفسه سینه در طول جراحی مرتبط باشد اما علل قطعی آن مشخص نیست. بین 20 تا 30 درصد از زنان پس از جراحی دچار علائم PMPS میشوند. مشخص نیست که این امر در مردان پس از جراحی سرطان سینه چقدر رایج است. به نظر میرسد این بیماری در بیماران جوانتر، افرادی که ALND کامل داشتند (نه فقط SLNB) و کسانی که پس از جراحی تحت درمان با اشعه قرار گرفتند، شایعتر است. از آن جایی که ALND در حال حاضر کمتر انجام میشود، PMPS کمتر از گذشته رایج است.
علائم PMPS عبارتند از:
- درد و گزگز در دیواره قفسه سینه، زیر بغل و یا بازو
- درد در شانه یا اسکار (جای زخم) جراحی
- بی حسی
- درد ناشی از سوزش یا تیر کشیدن
- احساس “سوزن و سوزن” شدن
- خارش شدید
اکثر بیماران مبتلا به PMPS میگویند که علائم آنها شدید نیست اما PMPS میتواند باعث شود که از بازوی خود آن طور که باید استفاده نکنید و به مرور زمان توانایی استفاده از آن را به طور معمول از دست بدهید. اگر درد یا سایر علائم مربوط به PMPS را دارید به پزشک خود اطلاع دهید. درد عصبی نیاز به درمان متفاوتی نسبت به سایر انواع درد دارد.
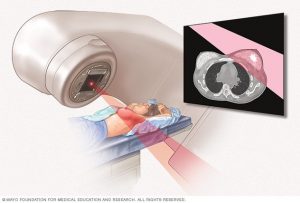
پرتو درمانی (Radiation Therapy) برای سرطان سینه در مردان
برخی از مردان مبتلا به سرطان سینه اغلب علاوه بر دورههای درمانی دیگر به پرتو درمانی نیز نیاز دارند. توصیههای پرتو درمانی در مردان مبتلا به سرطان سینه عمدتاً از توصیههای مربوط به سرطان سینه زنان گرفته شده است زیرا مطالعات کافی در مردان انجام نشده است.
نیاز به اشعه بستگی به نوع جراحی شما دارد یا اینکه ِآیا سرطان شما به غدد لنفاوی یا جای دیگری در بدن شما گسترش یافته است. تومورهایی که بزرگ هستند یا پوست را درگیر میکنند نیز ممکن است نیاز به اشعه داشته باشند. شما میتوانید فقط یک نوع تابش یا ترکیبی از انواع مختلف را دریافت کنید.
پرتو درمانی درمان با پرتوهای پر انرژی (مانند اشعه ایکس) یا ذراتی است که سلولهای سرطانی را از بین میبرند. رایج ترین نوع پرتو درمانی برای مردان مبتلا به سرطان سینه، پرتو درمانی خارجی (external beam radiation) نام دارد. یک دستگاه تابش را روی ناحیه تحت تاثیر سرطان متمرکز میکند.
چه زمانی میتوان از پرتو درمانی استفاده کرد؟
همه مردان مبتلا به سرطان سینه به پرتو درمانی نیاز ندارند اما این روش ممکن است در چندین موقعیت استفاده شود:
- پس از جراحی حفظ پستان (BCS یا breast-conserving surgery)، برای کمک به کاهش احتمال بازگشت سرطان در بافت باقی مانده پستان یا غدد لنفاوی مجاور. برای مردان مبتلا به سرطان سینه کمتر از زنان به پرتو درمانی نیاز است، عمدتاً به این دلیل که جراحی حفظ پستان (BCS) به اندازه کافی انجام نمیشود.
- پس از ماستکتومی، به خصوص اگر سرطان بزرگتر از 5 سانتی متر (حدود 2 اینچ) و به پوست چسبیده باشد یا اگر سرطان در غدد لنفاوی یافت شود.
- اگر سرطان به سایر قسمتهای بدن مانند استخوان یا مغز گسترش یافته باشد.
اینکه کدام نواحی به اشعه نیاز دارند بستگی به این دارد که آیا ماستکتومی یا جراحی حفظ پستان (BCS) انجام داده اید و اینکه آیا سرطان به غدد لنفاوی مجاور رسیده است یا خیر.
- اگر ماستکتومی انجام داده اید و هیچ غده لنفاوی سرطانی نداشته است، تابش روی دیواره قفسه سینه، اسکار ماستکتومی و هر جایی که پس از جراحی درین (drains) در آن گذاشته شده است، متمرکز میشود.
- اگر BCS داشتید، به احتمال زیاد به کل پستان تابش خواهید داشت (به نام تشعشع کل پستان یا whole breast radiation) و تشعشع اضافی به ناحیه ای در پستان که سرطان از آن جا برداشته شده است (به نام بستر تومور) برای کمک به پیشگیری از بازگشت آن به منطقه پس از پایان روند درمان و برای کل پستان انجام میشود. این دستگاه از همان مقادیر کمتر تشعشع استفاده میکند اما پرتوها به سمت بستر تومور نشانه میروند.
- اگر سرطان در غدد لنفاوی زیر بازو (غدد لنفاوی زیر بغل) یافت شد، ممکن است به این ناحیه نیز پرتو داده شود. در برخی موارد، ناحیه تحت درمان ممکن است شامل گرههای بالای استخوان ترقوه (غدد لنفاوی فوق ترقوه) و گرههای زیر استخوان سینه در مرکز قفسه سینه (گرههای لنفاوی پستانی داخلی) باشد.

چه زمانی رادیوتراپی کنیم؟
اگر بعد از جراحی نیاز به پرتو درمانی خارجی دارید، معمولاً تا زمانی که محل جراحی شما بهبود نیافته است – که اغلب یک ماه یا بیشتر طول میکشد – روند پرتو درمانی شروع نمیشود. اگر شیمی درمانی هم میکنید، پرتو درمانی معمولاً تا پایان شیمی درمانی به تعویق میافتد.
پرتو درمانی پستان اغلب 5 روز در هفته (دوشنبه تا جمعه) برای حدود 6 تا 7 هفته انجام میشود.
آماده شدن برای پرتو درمانی خارجی
قبل از شروع روند درمان، تیم تشعشع با دقت زوایای مناسب برای هدف گیری پرتوهای تابشی و دوز مناسب تابش را تعیین میکند. آنها چند علامت کوچک روی پوست شما ایجاد میکنند تا تابش را روی ناحیه مناسب متمرکز کنند. با تیم مراقبتهای پزشکی خود بررسی کنید که آیا علائمی که استفاده میکنند دائمی هستند یا خیر.
پرتو درمانی خارجی بسیار شبیه عکس برداری با اشعه ایکس است اما پرتو درمانی قوی تر میباشد. این روش به خودی خود بدون درد است. هر دوره درمانی فقط چند دقیقه طول میکشد اما زمان تنظیم – قرار دادن شما در موقعیت مناسب برای روند درمان – معمولاً بیشتر طول میکشد.
عوارض جانبی احتمالی پرتو درمانی
عوارض جانبی اصلی کوتاه مدت پرتو درمانی خارجی سینه عبارتند از:
- تورم در سینه یا دیواره قفسه سینه
- تغییرات پوستی در ناحیه تحت درمان مشابه آفتاب سوختگی (قرمزی، پوسته پوسته شدن و تیره شدن پوست)
- خستگی
تیم مراقبت پزشکی شما ممکن است به شما توصیه کند که از قرار دادن پوست قرار گرفته تحت درمان در معرض نور خورشید خودداری کنید زیرا ممکن است تغییرات پوستی را بدتر کند. اکثر تغییرات پوستی در عرض چند ماه بهتر میشوند. تغییرات در بافت سینه معمولاً در عرض 6 تا 12 ماه از بین میرود اما ممکن است این مدت بیشتر نیز طول بکشد.
پرتو درمانی خارجی میتواند عوارض جانبی را مدتی بعد ایجاد کند:
- تابش به سینه یا دیواره قفسه سینه گاهی اوقات میتواند به برخی از اعصاب بازو آسیب برساند. این پدیده پلکسوپاتی بازویی (brachial plexopathy) نامیده میشود و میتواند منجر به بی حسی، درد و ضعف در شانه، بازو و دست شود.
- تابش به غدد لنفاوی زیر بغل میتواند باعث ایجاد ادم لنف، نوعی درد و تورم در بازو یا قفسه سینه شود.
- در موارد نادر، پرتو درمانی ممکن است دندهها را ضعیف کند که همین امر میتواند منجر به شکستگی شود.
- در گذشته قسمتهایی از ریهها و قلب بیشتر در معرض اشعه قرار میگرفتند که میتوانست منجر به آسیب طولانی مدت این اندامها شود. تجهیزات پرتو درمانی مدرن به پزشکان اجازه میدهد تا پرتوهای تابشی را بهتر متمرکز کنند، بنابراین امروزه این مشکلات نادر هستند.
- یک عارضه بسیار نادر تابش به سینه یا دیواره قفسه سینه، ایجاد سرطان دیگری به نام آنژیوسارکوم (angiosarcoma) است.
درمانهای سیستمیک (Systemic treatments)
سرطان سینه را میتوان با استفاده از داروها نیز درمان کرد که میتوانند از طریق دهان و به صورت خوراکی مصرف شده یا مستقیماً وارد جریان خون شوند. این دورههای در مانی، درمانهای سیستمیک نامیده میشوند زیرا میتوانند تقریباً در هر نقطه از بدن به سلولهای سرطانی برسند. بسته به نوع سرطان سینه، انواع مختلفی از داروها ممکن است استفاده شود، از جمله:
شیمی درمانی (Chemotherapy) برای سرطان سینه در مردان
شیمی درمانی (chemo) درمان با داروهای کشنده سرطان است که ممکن است به صورت داخل وریدی (تزریق در رگ شما) یا از طریق دهان و به صورت خوراکی به فرد داده شوند. این داروها از طریق جریان خون حرکت میکنند تا به سلولهای سرطانی در بیشتر قسمتهای بدن برسند. گاهی اوقات، شیمی درمانی ممکن است مستقیماً در مایع نخاعی که مغز و نخاع را احاطه کرده است، داده شود.
چه زمانی از شیمی درمانی استفاده میشود؟
همه مردان مبتلا به سرطان سینه به شیمی درمانی نیاز ندارند اما چندین موقعیت وجود دارد که ممکن است در آنها شیمی درمانی توصیه شود:
- پس از عمل جراحی (شیمی درمانی کمکی یا adjuvant chemotherapy): زمانی که روش درمانی برای بیمارانی انجام میشود که هیچ شواهدی از عود سرطان پس از جراحی ندارند، به آن درمان کمکی میگویند. شیمی درمانی کمکی برای از بین بردن هر سلول سرطانی که ممکن است باقی مانده یا گسترش یافته باشد اما قابل مشاهده نباشد – حتی در آزمایشات تصویر برداری – استفاده میشود. اگر به این سلولها اجازه رشد داده شود، میتوانند تومورهای جدیدی را در سایر نقاط بدن تشکیل دهند. شیمی درمانی کمکی میتواند خطر عود سرطان سینه را کاهش دهد. از پرتو درمانی و هورمون درمانی نیز میتوان به عنوان درمان کمکی استفاده کرد.
- قبل از جراحی (شیمی درمانی نئوادجوانت یا neoadjuvant chemotherapy): درمان نئوادجوانت مانند درمان کمکی است با این تفاوت که شما دورههای درمانی را قبل از جراحی به جای بعد از آن انجام میدهید (یا حداقل آنها را شروع میکنید). از شیمی درمانی نئوادجوانت میتوان برای کوچک کردن تومور استفاده کرد تا بتوان آن را با جراحی کوچکتری برداشت.
به همین دلیل، شیمی درمانی نئوادجوانت اغلب برای درمان سرطانهایی استفاده میشود که آنقدر بزرگ هستند که در زمان تشخیص توسط جراحی برداشته شوند (به نام سرطانهای پیشرفته محلی یا locally advanced cancers). همچنین، با دادن شیمی درمانی قبل از برداشتن تومور، پزشکان میتوانند بهتر بررسی کنند که سرطان چگونه به آن واکنش نشان میدهد.
اگر اولین مجموعه از داروهای شیمی درمانی تومور را کوچک نکند، پزشک متوجه میشود که به داروهای دیگری نیز نیاز است. همچنین باید هر سلول سرطانی را که گسترش یافته اما دیده نمیشود، از بین ببرد. درست مانند شیمی درمانی کمکی، شیمی درمانی نئوادجوانت نیز میتواند خطر عود سرطان سینه را کاهش دهد. از نظر بقا و احتمال عود سرطان، تفاوتی بین انجام شیمی درمانی قبل یا بعد از جراحی وجود ندارد.
- برای سرطان پیشرفته پستان: شیمی درمانی همچنین میتواند به عنوان درمان اصلی برای مردانی استفاده شود که سرطان آنها پس از تشخیص به خارج از سینه و ناحیه زیر بغل گسترش یافته است یا اگر پس از درمانهای اولیه گسترش یابد. طول دوره درمانی بستگی به عملکرد شیمی درمانی و میزان تحمل فرد دارد.
گاهی اوقات مشخص نیست که آیا شیمی درمانی مفید خواهد بود یا خیر. آزمایشهایی مانند Oncotype DX و MammaPrint وجود دارد که میتواند به تعیین اینکه کدام مردان به احتمال زیاد از شیمی درمانی پس از جراحی سینه سود میبرند، کمک میکند.
کدام داروهای شیمی درمانی برای سرطان سینه استفاده میشوند؟
در بیشتر موارد (به ویژه به عنوان درمان کمکی یا نئوادجوانتی)، شیمی درمانی زمانی مؤثرتر است که ترکیبی از داروها استفاده شود. امروزه پزشکان از ترکیبهای مختلف استفاده میکنند و مشخص نیست که کدام یک از ترکیبها به وضوح بهترین است.
رایج ترین داروهای مورد استفاده برای شیمی درمانی کمکی و نئوادجوانت عبارتند از:
- آنتراسایکلینها (Anthracyclines)، مانند دوکسوروبیسین (doxorubicin یا Adriamycin) و اپی روبیسین (Ellence یا epirubicin)
- تاکسانها (Taxanes)، مانند پاکلیتاکسل (paclitaxel یا Taxol) و دوستاکسل (docetaxel یا Taxotere)
- 5-فلوئورواوراسیل (5-FU)
- سیکلوفسفامید (Cyclophosphamide یا Cytoxan)
- کربوپلاتین (Paraplatin یا Carboplatin)
اغلب، ترکیبی از 2 یا 3 مورد از این داروها استفاده میشود.
داروهای شیمی درمانی مفید در درمان سرطان پستان که گسترش یافته است، عبارتند از:
- تاکسانها، مانند پاکلیتاکسل (Taxol)، دوستاکسل (Taxotere) و پاکلیتاکسل متصل به آلبومین (Abraxane)
- آنتراسایکلینها (دوکسوروبیسین، دوکسوروبیسین لیپوزومی پگیله (pegylated liposomal doxorubicin) و اپی روبیسین)
- عوامل پلاتینه (سیس پلاتین یا cisplatin، کربوپلاتین یا carboplatin)
- Vinorelbine (Navelbine)
- کاپسیتابین (Capecitabine یا Xeloda)
- جمسیتابین (Gemcitabine یا Gemzar)
- ایکسابپیلون (Ixabepilone یا Ixempra) پاکلی تاکسل متصل به آلبومین (nab-paclitaxel یا Abraxane)
- Eribulin (Halaven)
اگرچه ترکیبات دارویی اغلب برای درمان سرطان پستان اولیه استفاده میشوند، سرطان پیشرفته پستان اغلب با داروهای شیمی درمانی منفرد درمان میشود. با این حال، برخی از ترکیبات، مانند پاکلیتاکسل به علاوه کربوپلاتین، معمولا برای درمان سرطان پستان پیشرفته نیز استفاده میشود.
برای سرطانهایی که HER2 مثبت هستند، یک یا چند دارو که HER2 را هدف قرار میدهند ممکن است همراه با شیمی درمانی استفاده شود. برای اطلاعات بیشتر در مورد این داروها به مبحث درمان هدفمند برای سرطان سینه در مردان مراجعه کنید.
شیمی درمانی چگونه انجام میشود؟
داروهای شیمی درمانی برای سرطان سینه معمولاً در ورید (IV) یا به صورت تزریق در چند دقیقه یا به صورت انفوزیون در مدت زمان طولانیتر به فرد داده میشوند. این کار را میتوان در مطب پزشک، کلینیک شیمی درمانی یا در بیمارستان انجام داد.
اغلب، یک IV کمی بزرگتر و محکم تر در سیستم ورید برای انجام شیمی درمانی مورد نیاز است. آنها به عنوان کاتترهای ورید مرکزی (central venous catheters یا CVCs)، دستگاههای دسترسی وریدی مرکزی (CVAD یا central venous access devices) یا خطوط مرکزی شناخته میشوند. آنها برای قرار دادن داروها، فرآوردههای خونی، مواد مغذی یا مایعات مستقیماً در خون شما استفاده میشوند. همچنین میتوان از آنها برای خارج کردن خون برای انجام آزمایش نیز استفاده کرد.
بسیاری از انواع مختلف CVC در دسترس هستند. 2 نوع متداول پورت و خط PICC هستند. برای بیماران مبتلا به سرطان سینه، خط مرکزی معمولاً در سمت مخالف سینهای قرار میگیرد که تحت عمل جراحی قرار گرفته است.
پزشکان دورههای شیمی درمانی را انجام میدهند و هر دوره درمانی پس از یک دوره استراحت از سر گرفته میشود. شیمی درمانی در روز اول هر سیکل شروع میشود اما برنامه تنظیمی بسته به داروهای مورد استفاده متفاوت است. به عنوان مثال، برای برخی داروها، شیمی درمانی فقط در روز اول چرخه انجام میشود. برای سایر داروها، برنامه دوره درمانی میتواند به شکل دریافت هر روزه به مدت 14 روز یا هر هفته به مدت 2 هفته دارو باشد. سپس، در پایان چرخه، برنامه شیمی درمانی برای شروع چرخه بعدی تکرار میشود.
چرخهها اغلب 2 یا 3 هفته هستند اما بسته به داروی خاص یا ترکیبی از داروها متفاوت اند. برخی از داروها مدت زمان بیشتری تجویز میشوند. شیمی درمانی ادجوانت و نئوادجوانت اغلب در مجموع 3 تا 6 ماه، بسته به اینکه چه دارویی استفاده میشود، تجویز میشود. روند درمانی برای سرطان پیشرفته پستان اغلب طولانیتر است و مدت آن بر این اساس است که این روش درمانی چقدر خوب کار میکند و چه عوارض جانبی را به همراه دارد.
شیمی درمانی متراکم دوز (Dose-dense chemotherapy): پزشکان دریافته اند که نزدیکتر کردن چرخههای برخی از داروهای شیمی درمانی میتواند احتمال بازگشت سرطان و بهبود بقا را در برخی از بیماران کاهش دهد. این موضوع معمولاً به معنای دادن همان شیمی درمانی است که به طور معمول تجویز میشود اما به جای هر 3 هفته، آن را هر 2 هفته یک بار تجویز میکنند.
یک دارو (عامل رشد) برای کمک به افزایش تعداد گلبولهای سفید بعد از شیمی درمانی به بیمار داده میشود تا اطمینان حاصل شود که تعداد گلبولهای سفید خون به موقع برای چرخه بعدی به حالت عادی باز میگردد. این روش را میتوان هم برای شیمی درمانی کمکی و هم برای نئوادجوانت استفاده کرد. این روش میتواند منجر به مشکلات بیشتر در رابطه با شمارش خون پایین شود، بنابراین برای همه افراد مناسب نیست.
عوارض جانبی احتمالی شیمی درمانی
داروهای شیمی درمانی به سلولهایی که به سرعت در حال تقسیم هستند حمله میکنند، به همین دلیل است که آنها علیه سلولهای سرطانی عمل میکنند. اما سلولهای دیگر بدن مانند سلولهای مغز استخوان، پوشش دهان و روده و فولیکولهای مو نیز به سرعت تقسیم میشوند. این سلولها احتمالاً تحت تأثیر شیمی درمانی نیز قرار میگیرند که میتواند منجر به عوارض جانبی شود. برخی از مردان عوارض جانبی زیادی دارند در حالی که برخی دیگر ممکن است عوارض جانبی کمی داشته باشند.
عوارض جانبی شیمی درمانی به نوع دارو، مقدار مصرف و طول درمان بستگی دارد. برخی از رایج ترین عوارض جانبی ممکن عبارتند از:
- ریزش مو
- زخمهای دهانی
- از دست دادن اشتها (یا افزایش اشتها)
- تهوع و استفراغ
- تعداد کم سلولهای خونی
شیمی درمانی میتواند سلولهای خون ساز مغز استخوان را تحت تاثیر قرار دهد که همین امر میتواند منجر به بروز موارد زیر شود:
- افزایش احتمال عفونت (به دلیل تعداد کم گلبولهای سفید خون)
- کبودی یا خونریزی آسان (به دلیل تعداد کم پلاکت خون)
- خستگی (به دلیل کاهش تعداد گلبولهای قرمز خون یا دلایل دیگر)
این عوارض معمولا کوتاه مدت هستند و پس از پایان دوره درمانب از بین میروند. اگر عوارض جانبی دارید به تیم مراقبت از سرطان خود اطلاع دهید زیرا اغلب راههایی برای کاهش آنها وجود دارد. به عنوان مثال، میتوان داروهایی را برای کمک به پیشگیری یا کاهش تهوع و استفراغ تجویز کرد.
چندین عارضه جانبی دیگر نیز ممکن است، رخ دهد. برخی از این موارد فقط با مصرف داروهای شیمی درمانی خاص دیده میشوند. از تیم مراقبت سرطان خود در مورد عوارض جانبی احتمالی داروهای خاصی که دریافت میکنید سوال بپرسید.
آسیب عصبی (نوروپاتی یا neuropathy): بسیاری از داروهایی که برای درمان سرطان سینه استفاده میشوند، از جمله تاکسانها (دوستاکسل و پاکلیتاکسل)، عوامل پلاتینه (کاربوپلاتین، سیس پلاتین)، وینورلبین، اروبولین و ایکسابپیلون میتوانند به اعصاب خارج از مغز و نخاع آسیب برسانند.
این عارضه گاهی اوقات ممکن است به بروز علائمی (عمدتاً در دستها و پاها) مانند بی حسی، درد، سوزش سوزن شدن، حساسیت به سرما یا گرما یا ضعف منجر شود. در بیشتر موارد، پس از قطع روند درمان، این مشکل از بین میرود اما ممکن است در برخی از مردان مدت طولانی ادامه داشته باشد.
آسیب قلبی: دوکسوروبیسین، اپی روبیسین و برخی داروهای دیگر ممکن است باعث آسیب دائمی قلب شوند (به نام کاردیومیوپاتی یا cardiomyopathy). اگر دارو برای مدت طولانی یا در دوزهای بالا استفاده شود، این خطر بالاتر است. اکثر پزشکان قبل از شروع یکی از این داروها، عملکرد قلب شما را با آزمایشی مانند MUGA یا اکوکاردیوگرام (echocardiogram، سونوگرافی قلب) بررسی میکنند.
آنها همچنین دوزها را به دقت کنترل کرده و علائم مشکلات قلبی را بررسی میکنند و ممکن است آزمایش قلب را برای نظارت بر عملکرد قلب در طول درمان تکرار کنند. اگر عملکرد قلب شروع به بدتر شدن کند، درمان با این داروها به طور موقت یا دائم متوقف میشود. با این حال، در برخی افراد، علائم نشان دهنده آسیب ممکن است تا ماهها یا سالها پس از توقف روند درمان ظاهر نشود. در صورت استفاده از داروهای دیگری که میتوانند باعث آسیب قلبی شوند (مانند داروهایی که HER2 را هدف قرار میدهند)، آسیب ناشی از این داروها بیشتر اتفاق میافتد، بنابراین پزشکان هنگام استفاده از این داروها با هم محتاط تر هستند.
سندرم دست و پا (Hand-foot syndrome): برخی از داروهای شیمی درمانی، مانند کپسیتابین و لیپوزومال دوکسوروبیسین، میتوانند کف دستها و کف پا را تحریک کنند. به این عارضه سندرم دست و پا (Hand-foot syndrome) میگویند. علائم اولیه شامل بی حسی، سوزن سوزن شدن و قرمزی است. اگر بیماری بدتر شود، دستها و پاها میتوانند متورم، ناراحت کننده یا حتی دردناک شوند.
ممکن است پوست تاول بزند و حتی کنده شود. هیچ درمان خاصی در این شرایط وجود ندارد، اگرچه برخی از کرمها یا استروئیدهایی که قبل از شیمی درمانی داده میشوند ممکن است کمک کننده باشند. این علائم با قطع دارو یا کاهش دوز به تدریج بهتر میشوند. بهترین راه برای پیشگیری از سندرم شدید دست-پا این است که در صورت بروز علائم اولیه به پزشک خود اطلاع دهید تا بتوان دوز دارو را تغییر داده یا داروهای دیگری را تجویز کرد.
شیمی درمانی مغز (Chemo brain): تحقیقات بسیار کمی در مورد شیمی درمانی مغز در مردان وجود دارد اما بسیاری از زنانی که برای سرطان سینه تحت درمان قرار میگیرند، کاهش جزئی در عملکرد ذهنی را گزارش میکنند. ممکن است برخی مشکلات طولانی مدت در تمرکز و حافظه وجود داشته باشد.
اگرچه بسیاری از زنان این علائم را به شیمی درمانی مرتبط میدانند اما این حالات در زنانی که به عنوان بخشی از درمان خود شیمی درمانی انجام نداده اند نیز دیده شده است. همچنین، اکثر زنان پس از شیمی درمانی عملکرد خوبی دارند. در مطالعات مربوط به شیمی درمانی مغز به عنوان یک عارضه جانبی روند درمان، علائم اغلب در عرض چند سال از بین میروند. اگرچه بیشتر تحقیقات در زنان انجام شده است اما دلیلی وجود ندارد که انتظار تفاوت در مردان تحت درمان سرطان سینه وجود داشته باشد.
افزایش خطر ابتلا به سرطان خون: به ندرت، برخی از داروهای شیمی درمانی میتوانند باعث بیماریهای مغز استخوان مانند سندرم میلودیسپلاستیک (myelodysplastic syndrome) یا حتی لوسمی میلوئید حاد (acute myeloid leukemia)، سرطان گلبولهای سفید خون شوند. هنگامی فرد به این بیماریها مبتلا میشود که معمولا 10 سال از روند درمان گذشته است. با این حال، برای اکثر مردان، مزایای شیمی درمانی برای جلوگیری از عود سرطان سینه یا افزایش طول عمر احتمالاً بسیار بیشتر از خطر این عارضه جدی اما نادر است.
احساس ناخوشی یا خستگی: بسیاری از افراد پس از شیمی درمانی مانند قبل احساس سلامتی نمیکنند. اغلب یک احساس باقی مانده از درد یا درد بدن و از دست دادن خفیف عملکرد فیزیکی وجود دارد. این حالات ممکن است تغییرات بسیار ظریفی باشند که به آرامی و در طول زمان اتفاق میافتند.
خستگی اغلب یکی دیگر از مشکلات رایج (اما اغلب نادیده گرفته شده) برای کسانی است که شیمی درمانی کرده اند. این حالت ممکن است تا چندین سال طول بکشد. اغلب میتوان به رفع این خستگی کمک کرد، بنابراین مهم است که پزشک یا پرستار خود را در مورد آن مطلع کنید. ممکن است ورزش، چرت زدن و صرفه جویی در انرژی توصیه شود. اگر مشکلاتی در خواب وجود دارد، میتوان آنها را درمان کرد. گاهی اوقات افسردگی وجود دارد که ممکن است با مشاوره و یا مصرف دارو رفع شود.
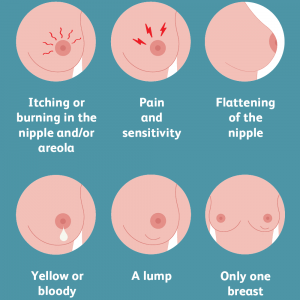
هورمون درمانی (Hormone Therapy) برای سرطان سینه در مردان
هورمون درمانی (گاهی اوقات درمان غدد درون ریز یا endocrine therapy نامیده میشود) راهی برای درمان سرطان با استفاده از هورمونها یا داروها یا سایر روشهای درمانی است که بر هورمونها تأثیر میگذارند. هورمون درمانی نوعی درمان سیستمیک مانند شیمی درمانی است. میتوان از آن بعد از جراحی (درمان کمکی) برای کمک به کاهش خطر عود سرطان یا قبل از جراحی (درمان نئوادجوانت) استفاده کرد. همچنین برای درمان سرطان گسترش یافته یا سرطانی که پس از گذراندن دوره درمانی عود کرده است (بازگشت) استفاده میشود.
برخی از سرطانهای سینه در پاسخ به هورمونهای استروژن یا پروژسترون رشد میکنند. استروژن و پروژسترون معمولاً به عنوان هورمونهای زنانه در نظر گرفته میشوند اما مردان نیز آنها را در بدن خود دارند، فقط در سطوح پایین تر.
حدود 9 مورد از 10 مورد سرطان سینه در مردان دارای گیرنده هورمونی مثبت هستند. این پدیده باعث میشود که آنها بیشتر به درمانهای هورمونی پاسخ دهند. سرطان سینه میتواند گیرنده استروژن (ER) مثبت، یا گیرنده پروژسترون (PR) مثبت یا دارای هر دو مورد باشد. هورمون درمانی به افرادی که تومورهایشان هم ER و هم PR منفی است، کمک نمیکند.
چه نوع داروهایی در هورمون درمانی استفاده میشود؟
چندین روش برای جلوگیری از اثرات استروژن یا کاهش سطح استروژن برای درمان سرطان سینه در زنان استفاده میشود. اگرچه بسیاری از این موارد ممکن است در مردان نیز موثر باشد اما اغلب به خوبی مورد مطالعه قرار نگرفته اند.
تاموکسیفن (Tamoxifen) و تورمیفن (Fareston یا toremifene)
این داروها گیرندههای استروژن روی سلولهای سرطان سینه را مسدود میکنند. این داروها با مسدود کردن این گیرندههای استروژن، از پیوستن استروژن به سلولهای سرطانی جلوگیری میکنند و رشد سلولها متوقف میشود. هر دو دارو روزانه به صورت قرص مصرف میشوند.
تاموکسیفن بهترین داروی هورمونی مورد مطالعه برای سرطان سینه در مردان است و اغلب در ابتدا استفاده میشود. اگر تاموکسیفن مؤثر نباشد (یا از کار بیفتد)، داروهای هورمونی دیگری ممکن است آزمایش شوند اما این امر تا حد زیادی بر اساس میزان عملکرد آنها در زنان مبتلا به سرطان سینه است. مطالعات بزرگ روی زنان مبتلا به سرطانهای گیرنده هورمونی مثبت که در آنها تومور به طور کامل با جراحی حذف شده است، نشان میدهد که مصرف تاموکسیفن بعد از عمل جراحی به مدت 5 سال، احتمال عود سرطان را به نصف کاهش میدهد.
مصرف آن به مدت 10 سال ممکن است کمک بیشتری کند. مطالعات بر روی مردان مبتلا به سرطان سینه کوچکتر بوده است اما نشان میدهد که مصرف تاموکسیفن پس از جراحی برای سرطان پستان در مراحل اولیه میتواند شانس عود سرطان را کاهش داده و بقا را بهبود بخشد. تاموکسیفن همچنین میتواند برای درمان سرطان سینه متاستاتیک نیز استفاده شود.
Toremifene مانند تاموکسیفن عمل میکند اما اغلب استفاده نمیشود و فقط برای بیماران مبتلا به سرطان سینه متاستاتیک تایید شده است. اگر تاموکسیفن قبلاً استفاده شده باشد و اثر آن متوقف شده باشد، احتمالاً این دارو نیز مؤثر نیست.
شایع ترین عوارض جانبی تاموکسیفن و تورمیفن عبارتند از:
- گر گرفتگی
- مشکلات جنسی
- خستگی
برخی از مردان مبتلا به سرطانی که به استخوانها گسترش مییابد، ممکن است دچار داغ شدن تومور همراه با درد و تورم در عضلات و استخوانها شوند. این عارضه معمولاً به سرعت کاهش مییابد اما در برخی موارد نادر ممکن است یک مرد سطح کلسیم بالایی در خون داشته باشد که کنترل آن دشوار است. اگر این اتفاق بیفتد، ممکن است لازم باشد روند درمان برای مدتی متوقف شود.
عوارض جانبی نادر اما جدی تر نیز ممکن است رخ دهند:
- لخته شدن خون یکی دیگر از عوارض جانبی غیر معمول اما جدی است. این لختهها معمولاً در پاها ایجاد میشوند (به نام ترومبوز ورید عمقی یا deep vein thrombosis یا DVT) اما گاهی اوقات ممکن است یک تکه لخته بشکند و در نهایت منجر به مسدود شدن یک شریان در ریهها شود (آمبولی ریوی یا PE). اگر دچار درد، قرمزی یا تورم در ساق پا، تنگی نفس یا درد قفسه سینه شدید، فوراً با پزشک یا پرستار خود تماس بگیرید زیرا اینها میتوانند علائم DVT یا PE باشند.
- به ندرت، تاموکسیفن با سکته مغزی در زنان یائسه همراه بوده است. خطر ایجاد این پدیده در مردان مشخص نیست. اگر دچار سردرد شدید ناگهانی، گیجی یا مشکل در صحبت کردن یا حرکت شدید، به پزشک خود اطلاع دهید.
تاموکسیفن همچنین ممکن است خطر حملات قلبی را در برخی بیماران افزایش دهد اما این ارتباط به درستی مشخص نیست.
مهارکنندههای آروماتاز (Aromatase inhibitors)
این گروه از داروها شامل آناستروزول (Arimidex یا anastrozole)، لتروزول (Femara یا letrozole) و exemestane (Aromasin) است. این داروها با مسدود کردن آنزیمی (آروماتاز) در بافت چربی که هورمونهای مردانه از غدد فوق کلیوی را به استروژن تبدیل میکند، تولید استروژن را متوقف میکنند. مهارکنندههای آروماتاز روزانه به صورت قرص مصرف میشوند.
آنها در درمان سرطان سینه در زنان بسیار مؤثر بوده اند اما در مردان به خوبی مطالعه نشده اند. با این حال، برخی از پزشکان از آنها برای درمان سرطان پستان پیشرفته در مردان استفاده میکنند که اغلب با یک آنالوگ هورمون آزاد کننده هورمون لوتئین کننده (luteinizing hormone-releasing hormone یا LHRH) ترکیب میشود تا تولید هورمون توسط بیضهها را متوقف کند (این داروها در ادامه مورد بحث قرار خواهند گرفت). این داروها عموماً در صورت توقف اثر تاموکسیفن استفاده میشوند. عوارض جانبی اصلی نازک شدن استخوانها و درد در عضلات و مفاصل است.
فولوسترانت (Faslodex یا Fulvestrant)
Fulvestrant نیز دارویی است که روی گیرندههای استروژن اثر میگذارد اما این دارو به جای مسدود کردن گیرندهها، آنها را از بین میبرد. Fulvestrant برای درمان سرطان سینه متاستاتیک، اغلب پس از متوقف شدن عملکرد سایر داروهای هورمونی (مانند تاموکسیفن و اغلب یک مهارکننده آروماتاز) استفاده میشود. این دارو از طریق تزریق به عضلانی هر 2 هفته به مدت یک ماه و سپس به صورت ماهانه تزریق میشود. شایع ترین عوارض جانبی عبارتند از گر گرفتگی، حالت تهوع خفیف، سر درد و درد در محل تزریق.
آنالوگهای هورمون آزاد کننده هورمون لوتئین کننده (LHRH یا Luteinizing hormone-releasing hormone) و آنتی آندروژنها (anti-androgens)
در مردان، آنالوگهای LHRH مانند لوپرولید (Lupron) و goserelin (Zoladex) بر غده هیپوفیز تأثیر میگذارند که تولید تستوسترون را در بیضهها تنظیم میکنند. این داروها باعث میشوند که غده هیپوفیز تولید هورمون مردانه تستوسترون را توسط بیضهها متوقف کند و منجر به کاهش سطح تستوسترون شود. این داروها به صورت واکسن یا هر ماه یا هر چند ماه یکبار تزریق میشوند. این داروها ممکن است به تنهایی یا همراه با مهارکنندههای آروماتاز یا آنتی آندروژنها برای درمان سرطان پستان پیشرفته در مردان استفاده شوند.
آنتی آندروژنها مانند فلوتامید (flutamide) و بیکالوتامید (bicalutamide) با مسدود کردن اثر هورمونهای مردانه بر سلولهای سرطان سینه عمل میکنند. این داروها روزانه به صورت قرص مصرف میشوند.
مگسترول (Megestrol)
Megestrol (Megace) یک داروی پروژسترون مانند است. مشخص نیست که این دارو چگونه از رشد سلولهای سرطانی جلوگیری میکند اما به نظر میرسد برای رسیدن به جایگاههای گیرنده هورمونی در سلولها رقابت میکند. این دارو یک داروی قدیمی است که معمولاً برای مردانی که دیگر به سایر اشکال هورمون درمانی پاسخ نمیدهند، اختصاص داده میشود. مگسترول ممکن است خطر لخته شدن خون را افزایش دهد و اغلب با افزایش اشتها باعث افزایش وزن میشود.
ارکیکتومی (اخته کردن یا Orchiectomy)
برداشتن بیضهها با جراحی (ارکیکتومی) روش دیگری برای تنظیم هورمونهایی است که ممکن است بر رشد سرطان سینه تأثیر بگذارند. برداشتن بیضهها سطح تستوسترون و سایر آندروژنها (هورمونهای مردانه) را تا حد زیادی کاهش میدهد.
اکثر سرطانهای سینه مردانه گیرندههای آندروژنی دارند که ممکن است باعث رشد سلولها شوند. آندروژنها همچنین میتوانند در بدن به استروژن تبدیل شوند. ارکیکتومی اکثر سرطانهای سینه مردانه را کوچک میکند و ممکن است به روند های درمانی دیگر مانند مصرف تاموکسیفن نیز کمک کند. زمانی این روش درمانی رایج برای سرطان سینه در مردان بود اما اکنون به دلیل رویکردهای جدید غیر جراحی برای کاهش سطح آندروژن، مانند آنالوگهای LHRH، کمتر مورد استفاده قرار میگیرد.
عوارض جانبی احتمالی هورمون درمانی
اگرچه برخی از این داروها عوارض جانبی منحصر به فردی دارند (توضیحات بالا را مطلالعه کنید) اما به طور کلی میتوانند باعث کاهش میل جنسی، مشکل در نعوظ، افزایش وزن، گر گرفتگی و تغییرات خلق و خو شوند. حتماً در مورد چنین عوارض جانبی با تیم مراقبت از سرطان خود صحبت کنید زیرا ممکن است راههایی برای درمان این عوارض وجود داشته باشد.
درمان دارویی هدفمند (Targeted Drug Therapy) برای سرطان سینه در مردان
همان طور که محققان در مورد تغییرات سلولهای سرطانی که باعث رشد خارج از کنترل آنها میشود، اطلاعات بیشتری کسب کرده اند، انواع جدیدی از داروها را توسعه داده اند که برخی از این تغییرات سلولی را هدف قرار میدهند. این داروهای هدفمند (Targeted drugs) متفاوت از داروهای شیمی درمانی (chemo) عمل میکنند.
داروهای هدفمند گاهی اوقات حتی زمانی که داروهای شیمی درمانی موثر نیستند، کار میکنند. برخی از داروهای هدفمند میتوانند به عملکرد بهتر انواع دیگر روشهای درمانی کمک کنند. داروهای هدفمند نیز عوارض جانبی متفاوتی نسبت به شیمی درمانی دارند.
چندین داروی هدفمند برای استفاده در درمان سرطان سینه تایید شده اند، اگرچه استفاده از این داروها در مردان اغلب بر اساس میزان عملکرد آنها در زنان است.
درمان هدفمند برای سرطان پستان HER2 مثبت
در برخی از مردان مبتلا به سرطان سینه، سلولهای سرطانی دارای مقدار زیادی پروتئین محرک رشد به نام HER2/neu (یا فقط HER2) روی سطح خود هستند. این سرطانها که به عنوان سرطان سینه HER2 مثبت شناخته میشوند، تمایل به رشد و گسترش بیشتری دارند.
انواع مختلفی از داروها ساخته شده اند که پروتئین HER2 را هدف قرار میدهند.
آنتی بادیهای مونوکلونال (Monoclonal antibodies)
آنتی بادیهای مونوکلونال نسخههای ساخته شده توسط انسان از پروتئینهای سیستم ایمنی (آنتی بادیها) هستند که برای اتصال به یک هدف خاص طراحی شده اند. در این مورد، این آنتی بادیها به پروتئین HER2 روی سلولهای سرطانی متصل میشوند که میتواند به توقف رشد سلولها کمک کند.
تراستوزوماب (Herceptin، دیگر داروها): تراستوزوماب (Trastuzumab) را میتوان برای درمان سرطان پستان در مراحل اولیه و پیشرفته استفاده کرد. این دارو اغلب همراه با شیمی درمانی تجویز میشود اما ممکن است به تنهایی نیز استفاده شود (مخصوصاً اگر شیمی درمانی قبلاً به تنهایی آزمایش شده باشد).
هنگامی که استفاده از این دارو قبل از جراحی (نئوادجوانت) یا بعد از آن (کمکی) برای درمان سرطان پستان اولیه شروع میشود، معمولاً به مدت 6 ماه تا یک سال برای فرد تجویز میگردد. برای سرطان پیشرفته پستان، دوره مصرف اغلب تا زمانی که دارو مفید باشد ادامه مییابد. این دارو در ورید (IV) تجویز میشود.
Herceptin نام تجاری اصلی تراستوزوماب بود اما چندین نسخه مشابه (به نام بیوسیمیلار یا biosimilars) نیز اکنون در دسترس هستند، از جمله Ogivri، Herzuma، Ontruzant، Trazimera و Kanjinti.
نوع دیگری از تراستوزوماب به نام تزریقی تراستوزوماب و هیالورونیداز (Herceptin Hylecta) نیز موجود است. این دارو به صورت تزریق زیر جلدی (زیر پوستی) طی چند دقیقه به فرد داده میشود.
Pertuzumab (Perjeta): این آنتی بادی مونوکلونال را میتوان با تراستوزوماب و شیمی درمانی، قبل یا بعد از جراحی برای درمان سرطان پستان در مراحل اولیه یا برای درمان سرطان پیشرفته پستان تجویز کرد. این دارو در ورید (IV) به فرد داده میشود.
برای افرادی که هر دوی این آنتی بادیهای مونوکلونال را به عنوان بخشی از دوره درمانی خود دریافت میکنند، ترکیبی از تراستوزوماب، پرتوزوماب و هیالورونیداز (Phesgo) نیز بهصورت یک دوره تزریقی در دسترس است. این دارو به صورت تزریق زیر جلدی (زیر پوستی) طی چند دقیقه به فرد داده میشود.
مارگتوکسیماب (Margetuximab یا Margenza): معمولاً پس از آزمایش حداقل 2 داروی دیگر که HER2 را هدف قرار میدهند، این آنتی بادی مونوکلونال را میتوان همراه با شیمی درمانی برای درمان سرطان پستان پیشرفته استفاده کرد. این دارو به صورت تزریق وریدی (IV) تجویز میشود.
ترکیبات آنتی بادی-دارو (Antibody-drug conjugates)
کنژوگه آنتی بادی-دارو (ADC) یک آنتی بادی مونوکلونال است که به یک داروی شیمی درمانی متصل است. در این مورد، آنتی بادی ضد HER2 با اتصال به پروتئین HER2 روی سلولهای سرطانی، مانند یک سیگنال محلی (homing signal) عمل میکند و شیمی درمانی را مستقیماً به آنها میرساند.
Ado-trastuzumab emtansine (Kadcyla یا TDM-1): این ترکیب آنتی بادی-دارو به تنهایی برای درمان سرطان پستان در مراحل اولیه بعد از جراحی (زمانی که شیمی درمانی و تراستوزوماب قبل از جراحی تجویز میشد اما هنوز سرطان در زمان جراحی وجود داشت)، یا برای درمان سرطان پیشرفته پستان در مردانی که قبلاً با تراستوزوماب و شیمی درمانی درمان شده اند، استفاده میشود. این دارو به صورت تزریق وریدی (IV) تجویز میشود.
Fam-trastuzumab deruxtecan (Enhertu): معمولاً پس از حداقل مصرف 2 مورد دارو دیگر، این ترکیب آنتی بادی-دارو میتواند به تنهایی برای درمان سرطان سینه ای که با جراحی قابل برداشتن نیست یا به قسمت دیگری از بدن گسترش یافته (متاستاز) استفاده میشود. داروهای ضد HER2 مورد آزمایش قرار گرفته اند. این دارو در ورید (IV) به فرد داده میشود.
مهارکنندههای کیناز (Kinase inhibitors)
HER2 نوعی پروتئین است که به نام کیناز (kinase) شناخته میشود.
کینازها پروتئینهایی موجود در سلولها هستند که به طور معمول سیگنالهایی را ارسال میکنند (مانند رشد سلولی). داروهایی که کینازها را مسدود میکنند، مهارکنندههای کیناز نامیده میشوند.
لاپاتینیب (Lapatinib یا Tykerb): این دارو قرصی است که روزانه مصرف میشود. لاپاتینیب برای درمان سرطان سینه پیشرفته، معمولاً همراه با داروی شیمی درمانی کپسیتابین یا با داروهای هورمون درمانی خاص استفاده میشود.
Neratinib (Nerlynx): این مهارکننده کیناز قرصی است که روزانه مصرف میشود. Neratinib برای درمان سرطان پستان در مراحل اولیه پس از اتمام یک سال مصرف تراستوزوماب توسط خانم بیمار استفاده شده و معمولاً به مدت یک سال تجویز میشود. همچنین میتوان آن را همراه با داروی شیمی درمانی کپسیتابین برای درمان افراد مبتلا به بیماری متاستاتیک، معمولاً پس از آزمایش حداقل 2 داروی دیگر هدفمند ضد HER2 تجویز کرد.
توکاتینیب (Tucatinib یا Tukysa): این مهارکننده کیناز به صورت قرص معمولاً دو بار در روز مصرف میشود. توکاتینیب برای درمان سرطان پستان پیشرفته، پس از آزمایش حداقل یک داروی دیگر هدفمند ضد HER2 استفاده میشود. این دارو معمولاً همراه با تراستوزوماب و داروی شیمی درمانی کپسیتابین تجویز میشود.
عوارض جانبی داروهای هدفمند HER2
عوارض جانبی داروهای هدفمند HER2 اغلب خفیف است اما برخی از این عوارض میتوانند جدی باشند. آن عوارضی را که ممکن است به آنها دچار شوید، با پزشک خود در میان بگذارید.
آنتی بادیهای مونوکلونال و ترکیبات آنتی بادی-دارو گاهی اوقات میتوانند باعث آسیب قلبی در طول دوره درمان یا بعد از آن شوند. این آسیب وارده میتواند منجر به نارسایی احتقانی قلب شود. برای اکثر (و نه همه) افراد، این اثر مدت کوتاهی باقی میماند و با قطع دارو بهتر میشود. خطر مشکلات قلبی زمانی بیشتر میشود که این داروها با داروهای شیمی درمانی خاصی که همچنین میتوانند باعث بروز آسیب قلبی شوند، مانند دوکسوروبیسین (آدریامایسین) و اپی روبیسین (Ellence) به فرد داده شوند.
از آن جایی که این داروها میتوانند باعث آسیب قلبی شوند، پزشکان اغلب قبل از درمان و به طور منظم در حین مصرف دارو، عملکرد قلب شما را (با اکوکاردیوگرام یا اسکن MUGA) بررسی میکنند. در صورت بروز علائمی مانند تنگی نفس، تورم پا و خستگی شدید این عوارض را به پزشک خود اطلاع دهید.
لاپاتینیب، نراتینیب، توکاتینیب و ترکیب پرتوزوماب با تراستوزوماب میتواند باعث اسهال شدید شود، بنابراین بسیار مهم است که به محض وقوع هر گونه تغییر در وضعیت روده ای خود به تیم مراقبت پزشکی خود اطلاع دهید.
لاپاتینیب و توکاتینیب همچنین میتوانند باعث ایجاد سندرم دست و پا شوند که در آن دستها و پاها زخم و قرمز شده و حتی ممکن است تاول زده و پوسته پوسته نیز شوند.
لاپاتینیب، نراتینیب و توکاتینیب میتوانند باعث مشکلات کبدی شوند. پزشک برای بررسی عملکرد کبد شما در طول روند درمان آزمایش خون انجام میدهد. اگر علائم یا نشانههای احتمالی مشکلات کبدی مانند خارش پوست، زرد شدن پوست یا قسمتهای سفید چشم، ادرار تیره یا درد در ناحیه بالای شکم را دارید، فوراً به تیم مراقبتهای پزشکی خود اطلاع دهید.
Fam-trastuzumab deruxtecan (Enhertu) میتواند باعث بروز بیماری ریوی جدی در برخی افراد شود. در برخی موارد این عارضه ممکن است حتی تهدید کننده زندگی باشد. بسیار مهم است که اگر علائمی مانند سرفه، خس خس سینه، مشکل تنفسی یا تب دارید، فوراً به پزشک یا پرستار خود اطلاع دهید.
درمان هدفمند برای سرطان پستان گیرنده هورمونی مثبت
در حدود ۹ مرد از هر ۱۰ مرد مبتلا به سرطان سینه، سلولهای سرطان سینه دارای پروتئینهایی (گیرنده) در خارج هستند که میتوانند به هورمونهایی مانند استروژن یا پروژسترون متصل شوند تا به رشد آنها کمک کنند. این نوع، سرطانهای پستان گیرنده هورمونی مثبت (HR-مثبت) نامیده میشوند.
گاهی اوقات آنها را سرطان پستان گیرنده مثبت استروژن (ER-مثبت) یا گیرنده پروژسترون مثبت (PR-مثبت) مینامند. این سرطانها معمولا با هورمون درمانی درمان میشوند. برخی از داروهای هدفمند درمانی میتوانند هورمون درمانی را حتی موثرتر کنند، اگرچه این داروهای هدفمند نیز ممکن است به موارد بروز عوارض جانبی اضافه کنند.
مهارکنندههای CDK4/6
این داروها پروتئینهای موجود در سلول به نام کینازهای وابسته به سیکلین (cyclin-dependent kinases یا CDKs)، به ویژه CDK4 و CDK6 را مسدود میکنند. مسدود کردن این پروتئینها در سلولهای سرطان سینه با گیرنده هورمونی مثبت به توقف تقسیم سلولها کمک میکند. این کار میتواند رشد سرطان را کند کند.
Abemaciclib (Verzenio) برای استفاده در مردان مبتلا به سرطان پیشرفته پستان HR مثبت و HER2 منفی که پس از درمان با هورمون درمانی و شیمی درمانی بدتر شده است، تأیید شده است. Abemaciclib به صورت قرص معمولاً دو بار در روز مصرف میشود.
Palbociclib (Ibrance) و Ribociclib (Kisqali) را میتوان همراه با داروهای هورمون درمانی خاص مانند فولوسترانت (fulvestrant) یا مهارکننده آروماتاز ( aromatase inhibitor، مانند لتروزول یا letrozole) در بیمارانی که سرطان پستان HER2 منفی پیشرفته HR مثبت دارند، (اگرچه ریبوسیکلیب به طور خاص برای استفاده در مردان تایید نشده است) استفاده کرد. این داروها به صورت قرص، معمولاً یک بار در روز به مدت 3 هفته در هر نوبت، با یک هفته استراحت قبل از شروع مجدد دوره درمانی مصرف میشوند.
شایع ترین عوارض جانبی این داروها کاهش تعداد سلولهای خونی و خستگی است. تهوع و استفراغ، زخمهای دهانی، ریزش مو، اسهال و سردرد عوارض جانبی کمتر رایج هستند. تعداد بسیار کم گلبولهای سفید میتواند خطر عفونت جدی را افزایش دهد. یک عارضه جانبی نادر که ممکن است تهدید کننده زندگی باشد، التهاب ریهها است که به آن بیماری بینابینی ریه (interstitial lung disease) یا پنومونیت (pneumonitis) نیز میگویند.
مهار کننده PI3K
Alpelisib (Piqray) یک داروی هدفمند است که به عنوان مهار کننده PI3K شناخته میشود. این پروتئین شکلی از پروتئین PI3K را در سلولهای سرطانی مسدود میکند که میتواند به جلوگیری از رشد آنها کمک کند.
این دارو را میتوان همراه با فولوسترانت برای درمان مردان و زنان یائسه مبتلا به سرطان سینه HER2 منفی با گیرندههای هورمونی پیشرفته با جهش ژن PIK3CA که در طول یا بعد از درمان با مهارکننده آروماتاز نیز رشد کرده است، استفاده کرد. حدود 30 تا 40 درصد از سرطانهای سینه دارای ژن PIK3CA جهش یافته هستند. پزشک قبل از شروع روند درمان با این دارو، خون یا تومور شما را برای بررسی وجود این جهش آزمایش میکند.
این دارو یک قرص است که یک بار در روز مصرف میشود.
عوارض جانبی میتواند شامل سطوح بالای قند خون، علائم مشکلات کلیوی، کبدی یا پانکراس، اسهال، زوايد پوستی، شمارش خون پایین، تهوع و استفراغ، خستگی، کاهش اشتها، زخمهای دهانی، کاهش وزن، سطوح پایین کلسیم، مشکلات لخته شدن خون، ریزش مو، واکنشهای پوستی بسیار شدید، مانند زوائد همراه با پوسته و تاول باشند و در صورت بروز باید به پزشک گزارش شوند. بیمارانی که سابقه واکنشهای پوستی شدید دارند باید قبل از مصرف آلپلیزیب به پزشک خود اطلاع دهند.
مهارکننده mTOR (mTOR inhibitor)
Everolimus (Afinitor) یک داروی هدفمند است که به عنوان مهارکننده mTOR شناخته میشود. این دارو mTOR را مسدود میکند، پروتئینی در سلولها که به طور معمول به رشد و تقسیم آنها کمک میکند. Everolimus همچنین ممکن است تومورها را از ایجاد رگهای خونی جدید باز دارد که همین امر میتواند به محدود کردن رشد آنها کمک کند. در دوره درمان سرطان سینه، به نظر میرسد این دارو به داروهای هورمون درمانی کمک میکند تا بهتر عمل کنند.
اورولیموس قرصی است که یک بار در روز مصرف میشود.
این دارو برای درمان سرطان سینه با گیرندههای هورمونی پیشرفته، HER2 منفی در زنانی که یائسه شده اند، تایید شده است. در صورتی که سرطان آنها در حین درمان با لتروزول یا آناستروزول رشد کرده باشد (یا اگر سرطان در مدت کوتاهی پس از توقف درمان با این داروها شروع به رشد کرد) در این زنان باید با اگزمستان (Aromasin یا exemestane) استفاده شود.
Everolimus همچنین برای استفاده در مراحل اولیه سرطان سینه و ترکیب با سایر درمانها مورد مطالعه قرار گرفته است. اگرچه اکثر افراد مبتلا به سرطان سینه در مطالعات اورولیموس زن هستند اما برخی از مطالعات شامل مردان نیز بوده است.
عوارض جانبی رایج این دارو شامل زخمهای دهانی، اسهال، حالت تهوع، خستگی، احساس ضعف یا خستگی، شمارش خون پایین، تنگی نفس و سرفه است. اورولیموس همچنین میتواند میزان لیپیدهای خون (کلسترول و تری گلیسیرید) و قند خون را افزایش دهد، بنابراین پزشک در زمانی که از این دارو استفاده میکنید، عملکرد خون شما را به صورت دوره ای بررسی میکند. این دارو همچنین میتواند خطر ابتلا به عفونتهای جدی را افزایش دهد، بنابراین پزشک در حین روند درمان شما را به شکل دقیقی در رابطه با ابتلا به عفونت زیر نظر خواهد گرفت.
درمان هدفمند برای مردان مبتلا به جهش BRCA
اولاپاریب (Lynparza یا Olaparib) و تالازوپاریب (talazoparib یا Talzenna) داروهایی هستند که به عنوان مهارکنندههای PARP شناخته میشوند. پروتئینهای PARP به طور معمول به ترمیم DNA آسیب دیده در داخل سلولها کمک میکنند.
ژنهای BRCA (BRCA1 و BRCA2) نیز به ترمیم DNA (به روشی کمی متفاوت) کمک میکنند اما جهش در یکی از این ژنها میتواند مانع از وقوع این اتفاق شود. مهارکنندههای PARP با مسدود کردن پروتئینهای PARP کار میکنند. از آن جایی که سلولهای تومور دارای ژن جهش یافته BRCA در حال حاضر در ترمیم DNA آسیب دیده مشکل دارند، مسدود کردن پروتئینهای PARP اغلب منجر به مرگ این سلولها میشود.
اولاپاریب و تالازوپاریب را میتوان برای درمان سرطان سینه متاستاتیک و HER2 منفی در بیماران مبتلا به جهش BRCA که قبلاً شیمی درمانی کرده اند (و هورمون درمانی در صورتی که سرطان گیرنده هورمونی مثبت باشد) استفاده کرد.
تنها بخشی از مردان مبتلا به سرطان سینه دارای ژن جهش یافته BRCA هستند که با آن متولد میشوند و در این ژن در تمام سلولهای بدنشان وجود دارد (بر خلاف تغییر ژنی که فقط در سلولهای سرطانی یافت میشود). اگر مشخص نباشد که جهش BRCA دارید، پزشک قبل از شروع درمان با یکی از این داروها، خون شما را آزمایش میکند تا مطمئن شود که دارای این جهش در ژن خود هستید یا خیر.
این داروها به صورت قرصهایی هستند که یک یا دو بار در روز مصرف میشوند.
عوارض جانبی میتواند شامل تهوع، استفراغ، اسهال، خستگی، از دست دادن اشتها، تغییرات چشایی، تعداد کم گلبولهای قرمز خون (کم خونی)، تعداد کم پلاکتها، کاهش تعداد گلبولهای سفید خون، درد شکم و درد عضلات و مفاصل باشد. به ندرت، برخی از افرادی که تحت درمان با مهارکنندههای PARP قرار میگیرند، به سرطان خون، مانند سندرم میلودیسپلاستیک (myelodysplastic syndrome) یا لوسمی میلوئید حاد (acute myeloid leukemia یا AML) مبتلا شده اند.
درمان هدفمند برای سرطان سینه سه گانه منفی
در سرطان سینه سه گانه منفی (TNBC)، سلولهای سرطانی گیرندههای استروژن یا پروژسترون ندارند و پروتئین HER2 نیز در آنها بیش از حد تولید نمیکنند.
کونژوگه آنتی بادی-دارو
کنژوگه آنتی بادی-دارو (ADC) یک آنتی بادی مونوکلونال است که به یک داروی شیمی درمانی متصل میشود.
Sacituzumab govitecan (Trodelvy): در مورد این ADC، قسمت آنتی بادی مونوکلونال به پروتئین Trop-2 روی سلولهای سرطان سینه میچسبد و دارو را مستقیماً به آنها میآورد. (برخی از سلولهای سرطان سینه مقدار زیادی Trop-2 دارند که به رشد و گسترش سریع آنها کمک میکند.)
این ترکیب آنتی بادی-دارو میتواند به تنهایی برای درمان TNBC پیشرفته، پس از گذراندن حداقل 2 دوره شیمی درمانی دیگر استفاده شود. این دارو به صورت وریدی (IV) به صورت هفتگی و به مدت 2 هفته تجویز میشود و پس از آن یک هفته استراحت به بیمار داده میشود و سپس مجدداً دوره درمانی دوم از سر گرفته میشود.
برخی از عوارض جانبی رایج این دارو عبارتند از: تهوع، استفراغ، اسهال، یبوست، احساس خستگی، زوائد پوستی، کاهش اشتها، ریزش مو، کاهش تعداد گلبولهای قرمز خون و درد شکم. تعداد بسیار کم گلبولهای سفید و اسهال شدید نیز ممکن است رخ دهد و همچنین واکنشهای دیگری نیز در زمانی که دارو تزریق میشود ممکن است ایجاد شوند. داروهایی برای کاهش احتمال واکنش آلرژیک معمولاً قبل از روند درمانی با این دارو تجویز میشود.
ایمونوتراپی (Immunotherapy) برای سرطان سینه در مردان
ایمونوتراپی استفاده از داروها برای تحریک سیستم ایمنی بدن فرد برای شناسایی و تخریب موثرتر سلولهای سرطانی است. ایمونوتراپی میتواند برای درمان برخی از انواع سرطان سینه استفاده شود.
مهارکنندههای ایست بازرسی ایمنی (Immune checkpoint inhibitors)
بخش مهمی از سیستم ایمنی توانایی آن در جلوگیری از حمله به سلولهای طبیعی بدن است. برای انجام این کار، سیستم ایمنی از «نقاط بازرسی یا checkpoints» استفاده میکند که پروتئینهایی روی سلولهای ایمنی هستند که برای شروع پاسخ ایمنی باید روشن (یا خاموش شوند). سلولهای سرطان سینه گاهی اوقات از این نقاط بازرسی برای جلوگیری از حمله سیستم ایمنی استفاده میکنند. داروهایی که این پروتئینهای نقطه بازرسی را هدف قرار میدهند به بازیابی پاسخ ایمنی در برابر سلولهای سرطان سینه کمک میکنند.
مهار کننده PD-1 (PD-1 inhibitor)
پمبرولیزوماب (Keytruda یا Pembrolizumab) برای سرطان سینه
پمبرولیزوماب (Keytruda) دارویی است که PD-1 را هدف قرار میدهد، پروتئینی روی نوعی از سلولهای سیستم ایمنی به نام سلولهای T که به طور معمول به جلوگیری از حمله این سلولها به سایر سلولهای بدن کمک میکند. این داروها با مسدود کردن PD-1، پاسخ ایمنی را در برابر سلولهای سرطان سینه تقویت میکنند. این دارو اغلب میتواند تومورها را کوچک کند.
می توان از آن همراه با شیمی درمانی برای درمان سرطان سینه سه گانه منفی (که پروتئین PD-L1 را میسازد) استفاده کرد که:
- به صورت موضعی بازگشته است (عود کرده است) اما با جراحی قابل برداشتن نیست و این بار با شیمی درمانی درمان نشده است.
- به سایر قسمتهای بدن سرایت کرده است و این بار تحت شیمی درمانی قرار نگرفته است.
این دارو به صورت انفوزیون داخل وریدی (IV) معمولاً هر 3 یا 6 هفته تجویز میشود.
مهار کننده PD-L1
Atezolizumab (Tecentriq) برای سرطان سینه
Atezolizumab (Tecentriq)، PD-L1 را هدف قرار میدهد، پروتئینی که در برخی از سلولهای تومور و سلولهای ایمنی یافت میشود. مسدود کردن این پروتئین میتواند به تقویت پاسخ ایمنی در برابر سلولهای سرطان سینه کمک کند. این دارو میتواند برخی از تومورها را کوچک کرده یا رشد آنها را کند کند.
هنگامی که تومور پروتئین PD-L1 را میسازد، آتزولیزوماب را میتوان با آبراگزان (Abraxane، پاکلیتاکسل متصل به آلبومین یا albumin-bound paclitaxel) برای سرطان سینه سه گانه منفی پیشرفته استفاده کرد. میتوان از این داروها به عنوان بخشی از اولین روند درمانی در برخی افراد استفاده کرد.
آتزولیزوماب به صورت انفوزیون داخل وریدی (IV) هر 2 هفته تجویز میشود.
عوارض جانبی احتمالی مهارکنندههای ایست بازرسی ایمنی
عوارض جانبی این داروها میتواند شامل خستگی، سرفه، حالت تهوع، زوائد پوستی، کم اشتهایی، یبوست و اسهال باشد.
سایر عوارض جانبی جدی تر که کمتر رخ میدهند:
واکنشهای انفوزیون (Infusion reactions): برخی از افراد ممکن است در حین مصرف این داروها واکنش انفوزیون داشته باشند. این پدیده مانند یک واکنش آلرژیک است و میتواند همراه با تب، لرز، برافروختگی صورت، زوائد پوستی، خارش پوست، احساس سرگیجه، خس خس سینه و مشکل در تنفس باشد. مهم است که در صورت داشتن هر یک از این علائم در حین مصرف این داروها، فوراً به پزشک یا پرستار خود اطلاع دهید.
واکنشهای خود ایمنی (Autoimmune reactions Autoimmune reactions): این داروها یکی از محافظهای سیستم ایمنی بدن را حذف میکنند. گاهی اوقات سیستم ایمنی شروع به حمله به سایر قسمتهای بدن میکند که میتواند باعث بروز مشکلات جدی یا حتی تهدید کننده زندگی در ریهها، رودهها، کبد، غدد هورمون ساز، کلیهها یا سایر اندامها شود.
بسیار مهم است که هر گونه عوارض جانبی جدید را به سرعت به تیم مراقبتهای پزشکی خود گزارش دهید. در صورت بروز عوارض جانبی جدی، ممکن است لازم باشد روند درمانی قطع شود و ممکن است حتی دوزهای بالایی از کورتیکواستروئیدها (corticosteroids) را برای سرکوب سیستم ایمنی خود دریافت کنید.
درمان سرطان پستان در مردان به تفکیک مرحله (سطح سرطان)
این اطلاعات بر اساس سیستمهای مرحله بندی AJCC قبل از سال 2018 است که اساساً بر اساس اندازه تومور و وضعیت غدد لنفاوی بوده اند. از آن جایی که سیستم مرحله بندی به روز شده برای سرطان پستان اکنون شامل وضعیت ER، PR و HER2 نیز میشود، ممکن است مراحل گفته شده بالاتر یا پایین تر از مراحل سیستمهای مرحله بندی قبلی باشد. این که آیا استراتژیهای درمانی با این سیستم مرحله بندی جدید تغییر خواهد کرد یا خیر، هنوز مشخص نشده است. شما باید مرحله و گزینههای درمانی خود را با پزشک خود در میان بگذارید.
از آن جایی که کار آزماییهای بالینی کمی در مورد درمان سرطان پستان مردانه انجام شده است، اکثر پزشکان توصیههای درمانی خود را بر اساس تجربیات خود در مورد این بیماری و نتایج مطالعات سرطان سینه در زنان ارائه میدهند. با ایجاد برخی تغییرات جزئی، سرطان سینه در مردان مانند سرطان سینه در زنان درمان میشود.
مرحله (وسعت) سرطان سینه شما عامل مهمی در تصمیم گیری در مورد گزینههای درمانی شما است. به طور کلی، هرچه سرطان سینه بیشتر گسترش یافته باشد، احتمالاً به روند درمان بیشتری و طولانی تری نیاز خواهید داشت. اما عوامل دیگری نیز میتوانند مهم باشند، مانند:
- اگر سلولهای سرطانی حاوی گیرندههای هورمونی باشند (یعنی اگر سرطان ER مثبت یا PR مثبت باشد)
- اگر سلولهای سرطانی دارای مقادیر زیادی پروتئین HER2 باشند (یعنی اگر سرطان HER2 مثبت باشد)
- وضعیت سلامت کلی و ترجیحات شخصی شما
- سرعت رشد سرطان (با تعیین مرحله یا سایر معیارها اندازه گیری میشود)
با پزشک خود در مورد این که چگونه این عوامل میتوانند بر انتخاب گزینههای درمانی شما تأثیر بگذارند، صحبت کنید.
مرحله 0 (کارسینوم مجرای در محل یا ductal carcinoma in situ)
سرطان مرحله 0 به این معنی است که سرطان به داخل مجرای شیری محدود میشود و یک سرطان غیر تهاجمی است. تومورهای پستان مرحله 0 شامل کارسینوم مجرای در محل (DCIS) میباشند.
این نوع با جراحی درمان میشود تا کل تومور از بین برود. اغلب در مردان ماستکتومی (mastectomy) انجام میشود. اگر جراحی حفظ پستان انجام شود، با پرتو درمانی به بافت باقی مانده سینه همراه خواهد بود.
گاهی اوقات DCIS میتواند شامل ناحیه ای از سرطان مهاجم باشد. احتمال اینکه ناحیه ای از DCIS حاوی سرطان مهاجم باشد با میزان اندازه تومور و سرعت رشد سرطان افزایش مییابد. اگر نگرانی از سرطان مهاجم وجود داشته باشد، غدد لنفاوی زیر بازو ممکن است برای گسترش بررسی شوند، اغلب با بیوپسی غدد لنفاوی نگهبان. اگر سلولهای سرطانی در غدد لنفاوی نگهبان یافت شوند، به این معنی است که تومور باید حاوی مقداری سرطان مهاجم باشد و مرد بیمار بر اساس مرحله سرطان مهاجم درمان میشود.
مرحله I
این سرطانها هنوز نسبتاً کوچک هستند و یا به غدد لنفاوی (N0) گسترش نیافته اند یا ناحیه کوچکی از سرطان به غدد لنفاوی نگهبان گسترش یافته است (N1mi).
روند درمانی اصلی سرطان سینه در مرحله اول، برداشتن آن با جراحی است. این کار معمولاً با ماستکتومی انجام میشود اما جراحی حفظ پستان (breast-conserving surgery یا BCS) نیز ممکن است گاهی اوقات یک گزینه باشد. اگر جراحی حفظ پستان انجام شود، معمولا با پرتو درمانی دنبال میشود.
غدد لنفاوی زیر بازو برای گسترش سرطان بررسی میشوند یا با تشریح غدد لنفاوی زیر بغل (axillary lymph node dissection یا ALND) یا بیوپسی گره نگهبان (SLNB یا sentinel node biopsy). اگر غده لنفاوی نگهبان حاوی سرطان باشد، بسته به اندازه سرطان در غدد لنفاوی و همچنین دوره درمانی دیگری که برنامه ریزی شده است، ممکن است به ALND کامل نیاز باشد.
هورمون درمانی، شیمی درمانی (chemo) و یا درمان هدفمند ممکن است به عنوان درمان کمکی (پس از جراحی) بر اساس اندازه تومور و نتایج آزمایشات آزمایشگاهی توصیه شود. هورمون درمانی با تاموکسیفن معمولا برای تومورهای گیرنده هورمونی مثبت توصیه میشود.
شیمی درمانی کمکی معمولاً برای تومورهای بزرگتر از 1 سانتی متر (حدود 1/2 اینچ) و برخی از تومورهای کوچکتر که ممکن است احتمال گسترش بیشتری داشته باشند (بر اساس ویژگیهایی مانند مرحله یا سرعت رشد بالا) استفاده میشود. مردان مبتلا به تومورهای HER2 مثبت نیز ممکن است درمان هدفمند با تراستوزوماب (هرسپتین) را دریافت کنند.
مرحله II
این سرطانها از سرطانهای مرحله I بزرگتر هستند و یا به چند غدد لنفاوی مجاور گسترش یافته اند.
درمان سیستمیک (دارویی) اغلب برای مردان مبتلا به سرطان پستان مرحله دوم توصیه میشود. برخی از درمانهای سیستمیک قبل از جراحی (درمان نئوادجوانت) و برخی دیگر بعد از جراحی (درمان کمکی) انجام میشوند. درمانهای نئوادجوانت ممکن است برای مردانی که تومورهای بزرگی دارند، گزینه مناسبی باشند زیرا میتوانند تومور را قبل از جراحی کوچک کنند.
تومور کوچک شده احتمالاً به اندازهای باشد که جراحی حفظ پستان (BCS) را به یک گزینه برای فرد تبدیل کند. همچنین غدد لنفاوی زیر بازو برای گسترش سرطان – یا با تشریح غدد لنفاوی زیر بغل (ALND) یا بیوپسی غدد لنفاوی نگهبان – بررسی میشوند. اگر غده لنفاوی نگهبان حاوی سرطان باشد، بسته به اندازه سرطان در غدد لنفاوی و همچنین دوره درمانی دیگری که برنامه ریزی شده است، ممکن است به ALND کامل نیاز باشد.
اگر تومور بزرگ باشد یا اگر مشخص شود که به چندین غدد لنفاوی گسترش یافته است، ممکن است پرتو درمانی پس از جراحی انجام شود. پرتو درمانی خطر بازگشت سرطان (عود) را کاهش میدهد.
داروهای مورد استفاده به سن مرد و وضعیت گیرنده هورمونی تومور و وضعیت HER2 بستگی دارد. این داروها میتوانند شامل موارد زیر باشند:
شیمی درمانی: شیمی درمانی را میتوان قبل یا بعد از جراحی انجام داد.
داروهای هدفمند HER2: اگر سرطان HER2 مثبت باشد، داروهای هدفمند HER2 همراه با شیمی درمانی به فرد داده میشوند. هر دو تراستوزوماب (Herceptin) و پرتوزوماب (Perjeta) ممکن است به عنوان بخشی از درمان نئوادجوانت استفاده شوند. سپس مصرف تراستوزوماب پس از جراحی در مجموع یک سال روند درمانی ادامه مییابد.
هورمون درمانی: اگر سرطان گیرنده هورمونی مثبت باشد، هورمون درمانی با تاموکسیفن معمولاً به مدت 5 سال پس از جراحی در نظر گرفته میشود.
مرحله III
این مرحله شامل تومورهای پیشرفته تر (بزرگ یا در حال رشد در پوست یا ماهیچه مجاور) و سرطانهایی است که به بسیاری از غدد لنفاوی مجاور گسترش مییابند.
اغلب، این سرطانها قبل از جراحی با شیمی درمانی (شیمی درمانی نئوادجوانت) تحت روند درمانی قرار میگیرند. برای تومورهای HER2 مثبت، داروی هدفمند تراستوزوماب نیز گاهی همراه با پرتوزوماب تجویز میشود. این کار معمولا با تجویز ماستکتومی دنبال میشود. اکثر مردان مبتلا به این نوع سرطان نیاز به تشریح کامل غدد لنفاوی زیر بغل (ALND) دارند.
اغلب، پرتو درمانی پس از جراحی توصیه میشود. اگر تومور گیرنده هورمونی مثبت باشد، هورمون درمانی کمکی با تاموکسیفن حداقل به مدت 5 سال انجام میشود. مردان مبتلا به سرطان HER2 مثبت نیز احتمالا تراستوزوماب را برای تکمیل روند درمانی یک ساله دریافت خواهند کرد. هورمون درمانی کمکی معمولاً میتواند همزمان با تراستوزوماب مصرف شود.
یکی دیگر از گزینههای درمانی سرطان مرحله سوم این است که ابتدا تحت جراحی قرار گیرد. این کار معمولاً به معنای ماستکتومی با ALND است. جراحی معمولاً با شیمی درمانی کمکی دنبال میشود.
اگر تومور HER2 مثبت باشد، تراستوزوماب همراه با شیمی درمانی به فرد داده میشود و سپس تا یک سال ادامه مییابد. پرتو درمانی پس از جراحی و شیمی درمانی توصیه میگردد. هورمون درمانی کمکی به مردان مبتلا به سرطان سینه با گیرنده هورمونی مثبت حداقل به مدت 5 سال داده میشود.
مرحله IV (متاستاتیک)
سرطان مرحله IV فراتر از سینه و غدد لنفاوی مجاور به سایر قسمتهای بدن نیز گسترش یافته است. سرطان سینه بیشتر به استخوانها، کبد و ریهها سرایت میکند. با پیشرفت سرطان، این بیماری ممکن است به مغز نیز سرایت کند اما میتواند هر اندام و بافتی را تحت تاثیر قرار دهد.
درمان سیستمیک (دارویی) روند درمانی اصلی مرحله چهارم سرطان پستان در مردان است. بسته به عوامل بسیاری، این روند درمانی ممکن است شامل هورمون درمانی، شیمی درمانی، درمان هدفمند، ایمونوتراپی یا ترکیبی از این روشها باشد.
پرتودرمانی و یا جراحی نیز ممکن است در شرایط خاصی استفاده شود، مانند:
- هنگامی که تومور سینه باعث ایجاد زخم باز در سینه (یا قفسه سینه) میشود.
- برای درمان تعداد کمی از متاستازها در یک ناحیه خاص مانند مغز
- برای کمک به جلوگیری از شکستگی استخوان
- زمانی که ناحیه ای از سرطان در حال گسترش بر روی نخاع باشد
- برای درمان انسداد رگ خونی در کبد
- برای تسکین درد یا علائم دیگر
اگر پزشک شما چنین روشهای درمانی محلی (منطقه ای) را توصیه میکند، مهم است که هدف آنها – چه تلاش برای درمان سرطان یا پیشگیری یا درمان علائم – را درک کنید.
در برخی موارد، شیمی درمانی منطقه ای (که در آن داروها مستقیماً به یک منطقه خاص مانند مایع اطراف مغز یا کبد وارد میشوند) نیز ممکن است مفید باشد.
روند درمانی برای تسکین علائم بستگی به محل انتشار سرطان دارد. برای مثال، درد ناشی از متاستازهای استخوانی ممکن است با پرتو درمانی خارجی و یا بیس فسفوناتها (bisphosphonates) یا دنوزوماب (Xgeva) درمان شود.
سرطان سینه سه گانه منفی پیشرفته (TNBC) که پروتئین PD-L1 را میسازد، ممکن است ابتدا با داروی ایمونوتراپی آتزولیزوماب همراه با پاکلیتاکسل متصل به آلبومین (آبراکسان) درمان شود. گزینه دیگر ممکن است درمان با داروی ایمونوتراپی پمبرولیزوماب (Keytruda) همراه با شیمی درمانی باشد. پروتئین PD-L1 در حدود 1 مورد از 5 مورد TNBC یافت میشود.
سرطان پیشرفته ای که در طول دوره درمانی نیز پیشرفت میکند
درمان سرطان پستان پیشرفته اغلب میتواند رشد سرطان را کوچک یا کند کند (گاهی برای سالها) اما پس از مدتی ممکن است کارایی خود را از دست بدهد. دورههای درمانی بیشتر در این مرحله به عوامل متعددی از جمله روشهای درمانی قبلی، محل قرار گیری سرطان و سن، سلامت عمومی و تمایل مرد بیمار برای ادامه دوره درمان بستگی دارد.
پیشرفت در حین هورمون درمانی: برای سرطانهای گیرنده هورمون مثبت که با هورمون درمانی درمان میشدند، تغییر به نوع دیگری از هورمون درمانی گاهی مفید است. گزینه دیگر ممکن است یک داروی هورمونی همراه با یک داروی درمانی هدفمند باشد. اگر این روش مفید نباشد، شیمی درمانی معمولاً روش بعدی است که مد نظر قرار میگیرد.
پیشرفت در حین شیمی درمانی: برای سرطانهایی که دیگر به یک روند خاص از شیمی درمانی پاسخ نمیدهند، روش دیگری ممکن است مفید باشد. بسیاری از داروها و ترکیبات مختلف را میتوان برای درمان سرطان سینه استفاده کرد. با این حال، هر بار که سرطان در طول درمان پیشرفت میکند، احتمال اینکه روند درمانی بعدی تأثیر داشته باشد، کمتر میشود.
برای سرطان پستان سه گانه منفی پیشرفته که در آن حداقل 2 دوره درمانی شیمی درمانی امتحان شده است، ترکیب آنتی بادی-دارو ساسیتوزوماب گوویتان (Trodelvy) ممکن است یک گزینه باشد.
پیشرفت در هنگام دریافت داروهای HER2: سرطانهای HER2 مثبت که دیگر به تراستوزوماب پاسخ نمیدهند ممکن است به داروهای دیگری که پروتئین HER2 را هدف قرار میدهند (گاهی همراه با داروهای شیمی درمانی یا هورمون درمانی)، پاسخ دهند. برخی از گزینهها ممکن است شامل موارد زیر باشد:
- Pertuzumab (Perjeta) با شیمی درمانی و تراستوزوماب
- Ado-trastuzumab emtansine (Kadcyla)
- فام تراستوزوماب دروکستکان (Enhertu)
- مارگتوکسیماب (Margenza) با شیمی درمانی
- لاپاتینیب (Tykerb) و داروی شیمی درمانی کپسیتابین
- لاپاتینیب و یک مهارکننده آروماتاز (برای سرطانهای گیرنده هورمونی مثبت)
- Neratinib (Nerlynx) و داروی شیمی درمانی capecitabine (این ترکیب میتواند برای سرطانهایی که به مغز گسترش یافته اند، مفید باشد)
- توکاتینیب (Tukysa)، تراستوزوماب، و داروی شیمی درمانی کپسیتابین (این ترکیب نیز میتواند برای سرطانهایی که به مغز گسترش یافته اند، مفید باشد)
از آن جایی که روندهای درمانی فعلی برای درمان سرطان پیشرفته سینه بسیار ناکارآمد هستند، اگر از سلامتی خوبی برخوردار هستید، ممکن است بخواهید در مورد شرکت در کار آزمایی بالینی که در آنها درمانهای جدیدتر را آزمایش میکنند، فکر کنید.
سرطان عود کننده
برای برخی از مردان، سرطان سینه ممکن است پس از درمان – گاهی اوقات سالها بعد – عود کند. به این بازگشت مجدد بیماری عود (recurrence) میگویند. عود سرطان میتواند موضعی (در همان سینه یا در محل زخم جراحی)، منطقه ای (در غدد لنفاوی مجاور) یا در یک منطقه دور باشد. اگر سرطان در سینه مقابل یافت شود اما در هیچ جای دیگری از بدن یافت نشود، این سرطان عود کننده نیست. این در واقع سرطان جدیدی است که نیاز به درمان خاص خود را دارد.
درمان سرطان دارای عود موضعی (local recurrence): این حالت شامل بازگشت سرطان در سینه یا دیواره قفسه سینه (نزدیک ماستکتوم) است. اگر بیمار عود موضعی داشته باشد و شواهدی از متاستازهای دور دست در وی دیده نشود، ممکن است همچنان درمان شود.
روند درمان بستگی به دورههای درمانی دیگری دارد که قبلاً انجام شده است. درمان سرطانی که دچار عود موضعی شده است ممکن است شامل جراحی اضافی به دنبال پرتو درمانی باشد. اگر ناحیه قبلاً تحت پرتو درمانی قرار گرفته باشد، ممکن است بدون آسیب رساندن به بافتهای مجاور، تابش بیشتری به آن ناحیه داده شود.
هورمون درمانی، شیمی درمانی، تراستوزوماب یا ترکیبی از آنها ممکن است بعد از جراحی و یا پرتو درمانی استفاده شود.
برای افراد مبتلا به سرطان سینه سه گانه منفی که به صورت موضعی عود کرده است و جراحی قادر به برداشتن کامل تومور نیست و همچنین تومور پروتئین PD-L1 را میسازد، ایمونوتراپی با داروی پمبرولیزوماب همراه با شیمی درمانی ممکن است یک گزینه باشد. اگر حداقل 2 دوره دارویی دیگر قبلاً امتحان شده باشد، ترکیب آنتی بادی-دارو ساسیتوزوماب گوویتکان (Trodelvy) نیز ممکن است یک گزینه باشد.
درمان سرطان دارای عود منطقه ای (regional recurrence): زمانی که سرطان سینه در غدد لنفاوی مجاور (مانند غدد لنفاوی زیر بازو یا اطراف استخوان ترقوه) عود میکند، میتوان با برداشتن آن غدد لنفاوی اقدام به درمان بیماری کرد. این روش ممکن است با پرتو درمانیهایی که به سمت ناحیه مورد نظر متمرکز میشوند، دنبال شود.
درمان سیستمیک (مانند هورمون درمانی، شیمی درمانی، درمان هدفمند یا ترکیبی از اینها) ممکن است پس از جراحی ویا پرتو درمانی استفاده شود.
درمان سرطان دارای عود از راه دور (distant recurrence): مردانی که سرطان آنها در نقاطی مانند استخوانها، ریهها، مغز و غیره عود میکند، اغلب همانند افرادی که در مرحله IV سرطان سینه با گسترش به این اندامها در ابتدا تشخیص داده شدند، درمان میشوند. تنها تفاوت این است که روند درمانی ممکن است تحت تأثیر دورههای درمانی قبلی بیمار قرار گیرد.
عود سرطان سینه گاهی اوقات ممکن است به سختی درمان شود. اگر از نظر سلامتی در وضعیت خوبی هستید، ممکن است بخواهید در مورد شرکت در کار آزمایی بالینی برای آزمایش یک روش درمانی جدیدتر نیز فکر کنید.
مترجم:فاطمه فریادرس
مطالعات بیشتر در بخش راهنمای علمی سایت