فهرست مطالب
نمایش
ساختار سیتومگالوویروس انسانی
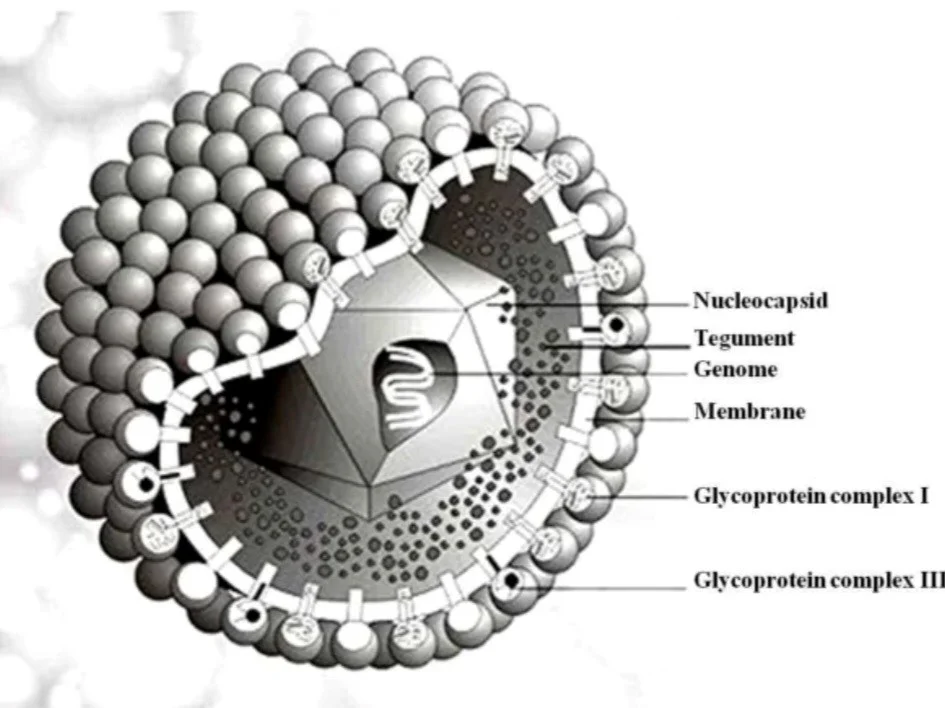
- سیتومگالوویروس یکی از اعضای خانواده ویروس هرپس است که در زیر خانواده هرپس بتا قرار میگیرد.
- CMV به شکل کروی با تقارن بیست وجهی است.
- کپسید پروتئین آن با قطر متوسط 100 نانومتر از 162 کپسومر شش ضلعی و پنج ضلعی توخالی با یک هسته الکترونی متراکم حاوی ژنوم DNA دو رشتهای با نوکلئوتیدهای 230 کیلوباز بر ثانیه تشکیل شده است. اینها با هم نوکلئوکپسید را تشکیل میدهند.
- نوکلئوکپسید توسط پوششی احاطه شده که ماهیت آن لیپوپروتئین است.
- بخش لیپیدی از غشای هستهای سلول میزبان آلوده، مشتق میشود.
- برآمدگیهای روی پوشش، خوشههایی از گلیکوپروتئینهای ویروسی هستند که به گیرنده میزبان خاصی متصل میشوند و به ورود ویروس کمک میکنند.
- gB یکی از گلیکوپروتئینهای سطحی اصلی در CMV است که بر اتصال و ورود ویروس به سلول و انتقال سلول به سلول تأثیر میگذارد.
- gH دومین گلیکوپروتئین نسبتاً فراوانی است که هدفی برای آنتی بادیهای خنثی کننده است.
- در ویروس بالغ، در قسمت بیرونی کپسید یک لایه پروتئینی آمورف، پوسته مانند، که توسط یک پوشش لیپیدی مشتق شده از غشای سلول میزبان، احاطه شده است.
- حداقل 25 پروتئین در لایه تگمنت قرار دارند.
- تگمنت شامل آنزیمهایی مانند VP16 است که مسئول براندازی پروتئینها و آنزیمهای سلولی برای درگیر شدن در تکثیر اسید نوکلئیک ویروسی است. پروتئین VHS (Virion Host Shutoff) سنتز پروتئین سلول میزبان را در سیتوپلاسم متوقف میکند.
ژنوم سیتومگالوویروس انسانی
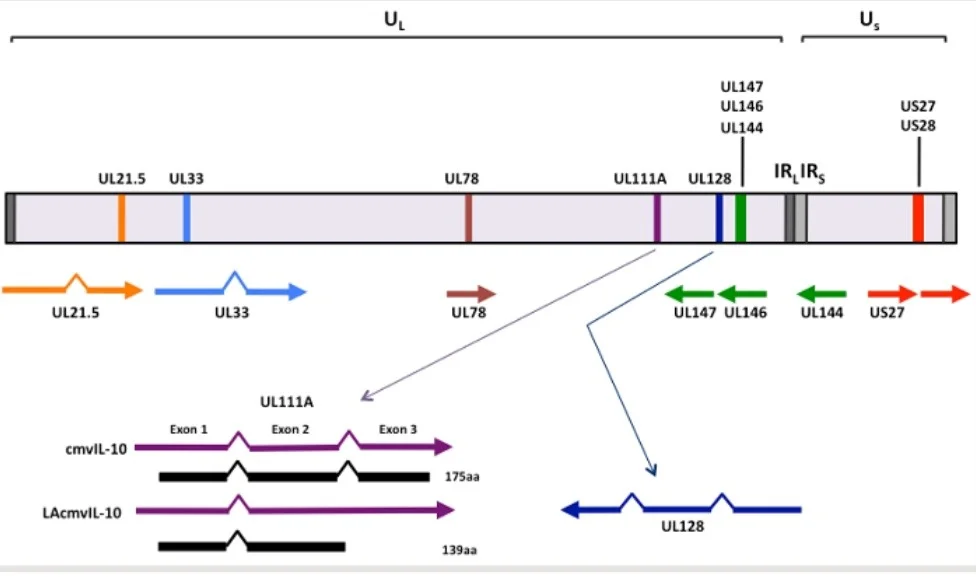
- ژنوم CMV از حدود 230 کیلوباز DNA خطی دو رشتهای تشکیل شده است.
- ژنوم تک بخشی است و شامل توالیهای پایانی و داخلی تکرار شده است.
- ژنوم به یک منطقه طولانی منحصر به فرد (UL) و یک منطقه کوتاه منحصر به فرد (US) تقسیم میشود که هر دو توسط توالیهای معکوس احاطه شدهاند.
- این شامل تقریباً 150 فریم خوانش (ORF) است که پروتئینها را رمزگذاری میکند.
- از این میان، مشخص شده است که 41 مورد ضروری و 117 مورد برای همانندسازی CMV ضروری نیستند.
انتقال و بیماریزایی
- عفونت CMV در سراسر جهان رخ میدهد و شیوع عفونت به طور قابل توجهی متفاوت است.
- CMV از طریق جفت در کانال زایمان و معمولاً در شیر مادر و در کودکان خردسال معمولاً از طریق بزاق منتقل میشود.
- همچنین میتواند از طریق رابطه جنسی منتقل شود. در منی و ترشحات دهانه رحم وجود دارد.
- علاوه بر این، میتواند از طریق انتقال خون و در حین پیوند اعضا نیز منتقل شود.
- عفونت مادرزادی CMV با 1% در ایالات متحده آمریکا و 2-3% در کشورهای در حال توسعه شایعترین عفونت ویروسی در جنین انسان است.
تکثیر سیتومگالوویروس انسانی
- اتصال به سلولهای میزبان با ادغام گلیکوپروتئینهای ویروسی به گیرندههای میزبان انجام میشود. این باعث میانجیگری بیشتر در اندوسیتوز ویروس در سلول میزبان میشود.
- پس از ورود، کپسید به منافذ هسته منتقل میشود و DNA ویروسی در هسته آزاد میشود.
- پروتئینهای Tegument پاسخهای سلول میزبان را تنظیم کرده و آبشار زمانی بیان ژنهای اولیه ویروس I (IE) را آغاز میکنند. به دنبال آن ژنهای زودرس (DE)، که تکثیر ژنوم ویروسی را آغاز میکنند، و ژنهای دیررس (L) با تاخیر.
- بیان دیررس ژن باعث تشکیل کپسید در هسته و به دنبال آن خروج از هسته و رفتن به سیتوزول میشود.
- کپسیدها با پروتئینهای تگمنت در سیتوزول مرتبط میشوند و به مجموعه ویروسی (AC) که حاوی اجزای شبکه آندوپلاسمی (ER)، دستگاه گلژی و اندوزومها است، منتقل میشوند.
- کپسیدها با جوانه زدن به وزیکولهای درون سلولی، پوسته و پوشش ویروسی را ایجاد میکنند.
- جمعآوری ویروس در مراکز هستهای ویروس و جوانه زدن از طریق لایه داخلی غشای هسته با وارد کردن
- تبخال، در گلژی و انتشار نهایی توسط اگزوسیتوز در غشای پلاسمایی صورت میگیرد.
پاتوژنز سیتومگالوویروس انسانی
- HCMV در طیف گستردهای از سلولها، از جمله سلولهای اپیتلیال غده و بافت مخاطی، سلولهای ماهیچه صاف، فیبروبلاستها، ماکروفاژها، سلولهای دندریتیک، سلولهای کبدی و سلولهای اندوتلیال عروقی تکثیر میشود.
- این تروپیسم سلولی وسیع، گسترش سیستمیک در بدن انسان و گسترش بین میزبانها را تسهیل میکند.
- تکثیر اولیه معمولاً با تکثیر در اپیتلیوم مخاطی در نتیجه تماس مستقیم با ترشحات عفونی یک فرد آلوده شروع میشود.
- مرحله سیستمیک عفونت، ویروس را از طریق ویرمی مرتبط با لکوسیت در میزبان منتشر میکند و ممکن است چند ماه طول بکشد.
- علاوه بر این، HCMV در سلولهای میلوئیدی مغز استخوان تحت تأخیر قرار میگیرد که احتمالاً منجر به عفونت مادامالعمر با فعالسازی مجدد پراکنده میشود.
- عفونت HCMV به طور کلی در افراد سالم بدون علامت است. با این حال، در افراد دچار نقص ایمنی، مانند گیرندگان پیوند عضو یا ناقلان ویروس نقص ایمنی انسانی، HCMV یک خطر تهدید کننده زندگی است.
- HCMV همچنین به عنوان عامل عفونی اصلی بیماریهای عصبی مادرزادی از طریق انتقال به وسیله جفت از مادر به کودک شناخته میشود.
- آنتیبادیهای IgM اختصاصی CMV در طول عفونت اولیه تولید میشوند و به مدت 3 یا 4 ماه باقی میمانند. اما در عفونتهای مکرر در افراد دارای ایمنی کافی تولید نمیشوند.
- آنتیبادیهای CMV IgG در زمان عفونت اولیه تولید میشوند و مادام العمر باقی میمانند.
- در عفونتهای داخل رحمی، هر دو IgM و IgG توسط جنین تولید شده، اما پاسخ IgG جنین تنها زمانی قابل تشخیص است که IgG غیرفعال از مادر کاتابولیز میشود.
- از سوی دیگر، تصور میشود که ایمنی سلولی (CMI) نقش کلیدی در سرکوب عفونت CMI ایفا میکند.
تظاهرات بالینی سیتومگالوویروس انسانی
- عفونت حاد CMV ممکن است مونونوکلئوز عفونی ناشی از ویروس اپشتین بار یا عفونت کبد توسط هپاتیت A، B یا C را تقلید کند.
- علائم مشابه ممکن است شامل تب، احساس کسلی، بزرگ شدن غدد لنفاوی، گلودرد، دردهای عضلانی، از دست دادن اشتها، بزرگ شدن کبد یا طحال و احساس خستگی باشد.
- علائم و نشانههای مشابه هپاتیت ممکن است شامل کاهش اشتها، زردی چشم، حالت تهوع و اسهال باشد.
- در افراد مبتلا به سیستم ایمنی سرکوب شده، عفونت CMV میتواند به اندامهای مختلف بدن حمله کند و ممکن است باعث تاری دید و کوری (رتینیت CMV)، عفونت ریه (پنومونی)، بلع دردناک (ازوفاژیت)، اسهال (کولیت)، التهاب کبد (هپاتیت)، یا التهاب مغز (آنسفالیت)، که ممکن است باعث تغییرات رفتاری، تشنج یا کما شود.
- نوزادان مبتلا به عفونت CMV (CMV مادرزادی) هیچ علامتی در بدو تولد ندارند. با این حال، تا 20 درصد از افرادی که در بدو تولد علائمی ندارند دچار ناشنوایی میشوند.
- تنها حدود 10 درصد از نوزادان مبتلا به CMV مادرزادی علائم و نشانههای عفونت را نشان میدهند یا عوارضی را ایجاد میکنند.
- علائم و نشانههای CMV هنگام تولد ممکن است شامل ناشنوایی، زردی پوست و چشم (یرقان)، بثورات پوستی، زایمان زودرس، وزن کم نوزاد هنگام تولد، ذات الریه، بزرگ شدن کبد و طحال، میکروسفالی یا تشنج باشد.
اثرات عفونت مادرزادی CMV عبارتند از:
- ناهنجاریهای CNS – میکروسفالی، عقب ماندگی ذهنی، اسپاستیسیتی، صرع، کلسیفیکاسیون اطراف بطن
- کوروئیدورتینیت و آتروفی بینایی
- ناشنوایی حسی عصبی
- هپاتواسپلنومگالی و زردی که ناشی از هپاتیت است
- پنومونیت
- میوکاردیت
- پورپورای ترومبوسیتوپنیک
- کم خونی همولیتیک
- عواقب دیررس – آسیب به اندام تشکیل دهنده مینای دندان که منجر به تغییر رنگ زرد و شکنندگی دندانها میشود.
تشخیص آزمایشگاهی سیتومگالوویروس انسانی
نمونه: ادرار، محلول نمک، بیوپسی بافت و سایر مایعات بدن
- جداسازی ویروس
- فیبروبلاستهای ریه جنین انسان بیشتر مورد استفاده قرار میگیرند.
- نمونه به سلولهای HEL تلقیح شده و به مدت 28 روز که 14 روز آن در محیط تاریک نگهداری میشود.
- CMV یک اثر سیتوپاتیک معمولی ایجاد میکند.
- میکروسکوپی
- ویریونها در ادرار نوزادان مبتلا به عفونت مادرزادی ممکن است توسط EM مشاهده شوند.
- سیتوپاتولوژی
- اجزای داخل سلولی احاطه شده توسط هالهای شفاف، با لکههای مختلف (گیمسا، رایت، هماتوکسیلین-ائوزین، پاپانیکولائو) نشان داده میشوند.
- اجزای سیتومگالی را میتوان از مواد بیوپسی با “ظاهر چشم جغد” معمولی تشخیص داد.
- ایمونوفلورسانس بافتی
- سلولهای ریه و کبد آلوده ممکن است توسط آنتیبادیهای خاص ضد CMV رنگآمیزی شوند.
- ایمونوهیستوشیمی
- ایمونوهیستوشیمی عمدتاً بر روی نمونههای بافت یا مایع بدن انجام میشود.
- اسلایدها از بخشهای منجمد نمونههای بافت بیوپسی (کبد، ریه) یا با سانتریفیوژ کردن سلولها بر روی یک اسلاید ساخته میشوند.
- سپس آنتیبادیهای مونوکلونال یا پلیکلونال علیه آنتیژنهای اولیه CMV اعمال میشود و توسط آنتیبادیهای نشاندار شده با فلورسنت یا آنتیبادیهای ثانویه نشاندار شده با آنزیم که با تغییر رنگ سوبسترا قابل مشاهده هستند، مشاهده میگردند.
- سپس اسلایدهای رنگآمیزی شده توسط میکروسکوپ فلورسنت یا نوری بررسی میشوند.
- تشخیص آنتیژنی
- آنتیژنمی به عنوان تشخیص آنتیژن CMV pp65 در لکوسیتها تعریف میشود.
- سنجش pp65 برای تشخیص پروتئینهای ماتریکس پیام رسان بر روی ویروس CMV، با روش ایمونوفلورسانس یا تقویت RNA پیام رسان استفاده میشود.
- سرولوژی
- آزمایشات سرولوژیکی برای تعیین اینکه آیا بیمار در گذشته عفونت CMV داشته است یا خیر مفید است که با وجود یا عدم وجود CMV IgG مشخص میشود.
- روشهای مورد استفاده برای تشخیص عبارتند از تثبیت کمپلمان، سنجش ایمونوسوربنت متصل به آنزیم (ELISA)، ایمونوفلورسانس ضد کمپلمان، سنجش رادیو ایمونوآسی و هماگلوتیناسیون غیرمستقیم.
- تشخیص آنتیبادیهای IgM به عنوان شاخص عفونت حاد یا اخیر، مورد استفاده قرار گرفته است.
- سنجشهای جذب IgM به طور گسترده مورد استفاده قرار میگیرند و مبتنی بر اتصال انتخابی آنتیبادی IgM به فاز جامد هستند.
- روشهای مولکولی
- واکنش زنجیرهای پلیمراز (PCR) یک روش سریع و حساس به طور گسترده برای تشخیص CMV بر اساس تقویت اسیدهای نوکلئیک است.
- PCR برای DNA CMV میتواند کیفی یا کمی باشد که در آن مقدار DNA ویروسی در نمونه مربوطه اندازه گیری میشود.
- PCR کمی (Real-Time PCR) به نظارت مستمر افراد دارای نقص ایمنی برای شناسایی بیماران در معرض خطر بیماری CMV برای درمان پیشگیرانه و تعیین پاسخ به درمان استفاده میشود.
- سنجش مبتنی بر توالی اسید نوکلئیک (NASBA) به تکثیر مبتنی بر توالی سنجش نوکلئیک خاص mRNAهای ویروسی ناپیوسته (بیان mRNA pp67 دیرهنگام) در پسزمینه DNA با استفاده از یک تکنیک خاص تکثیر استفاده میشود.
درمان
- مصرف داروهای ganciclovir و foscarnet در عفونت CMV تهدید کننده حیات در بیماران دچار نقص ایمنی مجوز گرفتهاند.
- گانسیکلوویر در بیماری شدید CMV به غیر از رتینیت، درمان اصلی میباشد.
- فوسکارنت و سیدوفوویر به عنوان داروهای خط دوم استفاده میشوند.
- آسیکلوویر و والاسیکلوویر فوایدی در بیماران پیوند مغز استخوان و کلیه نشان دادهاند.
پیشگیری و کنترل
- جدا کردن نوزادان مبتلا به بیماری انکلوژن سیتومگالی ژنرالیزه از سایر نوزادان توصیه میشود.
- غربالگری اهداکنندگان و گیرندگان پیوند از نظر آنتیبادی CMV.
- تجویز IgG انسانی تهیه شده از استخرهای پلاسما نتایج ناهماهنگی را در آزمایشها برای کاهش بروز عفونتهای ویروسی در گیرندگان پیوند نشان داده است.
- هر دو واکسن زنده و نوترکیب در حال توسعه هستند.
همچنین بخوانید:
- ویروس نیپا (NiV):ساختار، انتقال، تکثیر و تظاهرات بالینی
- فلوسایتومتری تصویربرداری برای نظارت بر تعامل ویروس-میزبان
- مروری بر ویروس های انکوژنیک
- روتاویروس چیست؟ ساختار، ژنوم، اپیدمیولوژی و علائم
مترجم: شقایق مرتاضی