اطلاعات عمومی
پروتئین های سطحی دخیل در ایمنی سلولی ساختار شیمیایی و نحوه عملکرد
مقدمهای بر پروتئین های سطحی
پروتئینهای سطحی سلولی پروتئینهایی هستند که درداخل غشای سلولی موجودات یا درسطح آن قرار دارند. این پروتئینها در تعامل سلول با دیگر سلولها بسیار نقش مهمی دارند که در ادامه به توضیح آن خواهیم پرداخت.
همانطور که میدانید پروتئینها از اسیدهای آمینه ساخته شدهاند. این ترکیبات به تبدیل سلولهای کلیدی سیستم ایمنی شما یعنی سلولهای T، سلولهای B و آنتیبادیها، به جنگندههای میکروبی کمک میکنند تا سلولهای مضر وارد شده به بدن شما را قبل از شروع عفونت شناسایی کرده و از بین ببرند.
تعداد زیادی از مولکولهای سیگنالدهنده سطح سلول(CSSM) در سالهای اخیر از نظر مولکولی شناسایی و از نظر عملکردی یا Functional مشخص شدهاند و از طریق این مطالعات، دانش ما در کنترل پاسخ ایمنی به طور تصاعدی افزایش یافته است. اکثر سلولهای ایمنی به یک یا چند مولکول سیگنال دهنده سطح سلول یا CSSM تکیه میکنند تا یک سیگنال محرک اولیه را برای درک محیط خود ارسال کنند که منجر به شروع یک پاسخ ایمنی میشود.
هم CSSM های تحریک کننده که پاسخ را ارتقا می دهند و هم CSSM هایی که پاسخ را مهار می کنند، برای کنترل جهت و بزرگی یک پاسخ ایمنی معین مورد نیاز هستند. با چنین بازخوردهای فشردهای، پاسخ های ایمنی تنظیم شده و به حالت اولیه باز می گردند.
همه ی سلولهای ایمنی، از جمله آنهایی که در پاسخ ایمنی ذاتی و فعال شرکت میکنند، تکامل یافتهاند تا گیرندههای سطح سلولی یا لیگاندهای مجزا را برای حس کردن و پاسخ به نشانههای محیطی بیان کنند. این مولکولهای سیگنالدهنده سطح سلول یا CSSM برای تمایز، تشخیص و عملکرد سلولی حیاتی هستند.
بسیاری از انواع سلول ها به طور مداوم محرک های محیطی پویا را از طریق گیرنده های منحصر به فرد خود برای تشخیص تغییرات خاص نظارت می کنند. به عنوان مثال، یک گیرنده سلول T (TCR) یک ساختار پپتیدی مجتمع سازگاری بافتی اصلی (MHC) را به یک سلول ارائه دهنده آنتی ژن حرفه ای (APC) متصل می کند. این TCR یک سیگنال آنتی ژنی را منتقل می کند و مسیرهای سیگنال دهی یک پاسخ ایمنی را آغاز می کند.
APC ها همچنین به تغییرات در محرکهای محیطی اطراف خود با استفاده از گیرنده های قلاب مانند(Toll-like Receptors) (TLR) برای شناسایی پاتوژن های بالقوه پاسخ می دهند. سلولهای کشنده طبیعی یا سلول های NK از گیرنده های سمیت سلولی طبیعی (NCRs)برای تشخیص تغییرات سلولهای هدف که آلوده به عفونتهای ویروسی هستند، استفاده میکنند. گیرنده های IgE با میل ترکیبی بالا روی مست سلها (Mast cells) با شناسایی کمپلکس های آلرژن-IgE به تشخیص و نظارت ایمنی کمک می کنند.
بنابراین، سلول های ایمنی از این گیرنده ها برای انتقال یک سیگنال اولیه برای روشن کردن پاسخ ایمنی استفاده می کنند.
سالهاست که ایمونولوژیستها به دنبال درک مکانیسم پاسخهای ایمنی اختصاصی و ماهیت گیرندههای آنتیژن بر روی سطح لنفوسیتها بودهاند. برتشر و کوهن در تلاش برای تولید یک مدل سلولی که تئوری تمایز سلول های خودی و غیرخود را در بر می گرفت، اولین کسانی بودند که یک مدل دو سیگنالی را برای توضیح القای تولرانس سلول B ارائه کردند.
مدل دو سیگنالی توضیح میدهد که چرا لنفوسیتها پس از قرار گرفتن در معرض سیگنال1 از گیرنده آنتیژن تنها اندکی فعال میشوند یا حتی برخی مواقع اصلا پاسخ نمیدهند و تنها پس از قرار گرفتن در معرض یک سیگنال دوم تحریک کننده سطح سلولی، فعال شدن کامل لنفوسیت رخ میدهد. آزمایشات بیشتر هویت مولکولی را برای سیگنال ثانویه (که سیگنال 2 نیز نامیده می شود) نشان داد.
در دهه گذشته بیش از 4000 مولکول بهعنوان CSSM بالقوه شناسایی شدهاند که بر اساس شباهتها در ساختار پروتئین گذرندهشان و عملکردهای درون سلولی و خارج سلولی دسته بندی شده اند.
گروهی از این CCSMها دیدگاههای جدیدی در مورد تنظیم پاسخهای ایمنی ارائه میدهند و شیوههای درمانی جدید برای بیماریهای انسانی را ارائه میکنند. درمطالعات اخیر نقش تک تک سلولهای ایمنی و نوع خاص پاسخهای ایمنی آنها مشخص شده است. سیگنال دهندههای حیاتی که در فعالسازی سلولهای ایمنی دخیل اند، از جمله فاکتور نکروز تومور (TNF)، ایمونوگلوبولین (Ig)، گیرنده جفت شده با پروتئین (GPCR) G و خانواده گیرنده لکتین (به عنوان مثال Siglec، Dectin، DNGR-1، DC-SIGN).
هر نوع سلول دارای گیرندههای شناسایی متفاوتی برای سیگنال اولیه است و سیگنالدهی از طریق این گیرندهها بسیار متمایز است. در مورد مولکول های هم سیگنال، بسیاری از آنها در بین چندین نوع سلول مشترک هستند در حالی که برخی به طور منحصر به فرد در انواع سلول های خاص وجود دارند. در تصویر تعدادی از این گیرنده ها برای شما نمایش داده شده است.
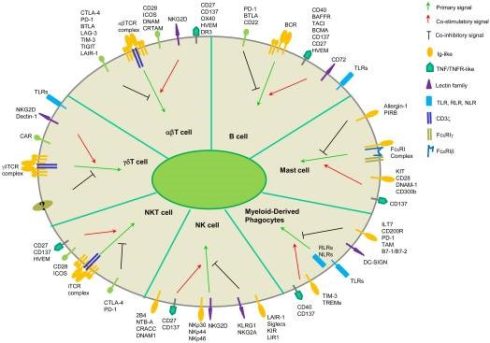
به جهت درک بهتر نقش و مکانیزم عملکرد مولکولهای سطحی، مست سل ها ( Mast cells) یکی از سلولهای ایمنی هستند را برای شما مورد بررسی قرار دادیم
مست سل ها (Mast cells)
مست سل یا Mast cells یک نوع سلول اصلی است که نقش کلیدی در پاسخ های التهابی آلرژیک دارد. مست سل ها به IgE تجمع یافته اطراف آلرژن متصل میشوند و به سرعت واسطههای پیش التهابی متعددی را آزاد میکنند، فرآیندی که به آن دگرانولاسیون گفته می شود. در دهه گذشته مست سل ها به عنوان سلولهای ایمنی شناخته شدهاند که نه تنها به عنوان سلولهای موثر کلیدی در پاسخ های آلرژیک عمل می کنند، بلکه عملکردهای تنظیمی را در پاسخ های ایمنی ذاتی و همچنین سازگاری انجام می دهند.
سیگنال اولیه برای شروع فعال سازی مست سل توسط تجمع گیرندههای با میل ترکیبی بالا برای IgE (FcεRIs) توسط آلرژن ایجاد میشود. گیرنده FcεRI یک کمپلکس تترامری است که شامل یک زنجیره α، که مسئول اتصال IgE است، یک زنجیره β و یک همودایمر زنجیره γ مرتبط با دی سولفید است که مسئول سیگنالدهی هستند.
به دنبال تجمع FcεRI، پروتئین تیروزین کیناز و Syk فعال می شوند که منجر به فسفوریلاسیون تیروزین مولکول آداپتور GAB2 و متعاقبا فعال شدن فسفاتیدیل 3-کیناز(PI3K) و PLCγ میشود. مولکولهای آداپتور غشایی LAT و NTAL برای هماهنگی مسیرهای سیگنالینگ که برای آزادسازی واسطههای مختلف التهابی مورد نیاز هستند، حیاتی هستند.
CD28، CD226 (DNAM-1) و CD137 گیرندههای هستند که به صورت همزمان با سلولهای T تحریک می شوند که برای تنظیم عملکرد ماست سل نیز شناخته شدهاند. SCF-KIT بهترین مسیر تحریکی برای ماست سل ها است. SCF به تنهایی باعث دگرانولاسیون ماست سل نمی شود در حالی که افزودن همزمان SCF و آنتی ژن به طور قابل توجهی باعث افزایش ترشح سیتوکین های متعدد در ماست سل های انسان و موش می شود.
سیگنال دهی SCF منجر به فعال سازی مسیرهای سیگنال دهی متعددی می شود، از جمله فعال سازی PI3K، PLCγ، آزادسازی کلسیم و فعال سازی MAPK-cascade، که با تحریک FcεRI نیز تحریک می شوند. با این حال، تحریک SCF نمی تواند فسفوریلاسیون تیروزین را القاء کند یا PKC را فعال کند، که ممکن است ناتوانی آن را در تحریک دگرانولاسیون ماست سل به خودی خود توضیح دهد.
گیرنده های مهاری مشترک برای ماست سل عبارتند از PIR-B، CD300a، MAFA، gp49B1 و آلرژین-1، که همگی حاوی ITIM در حوزه سیتوپلاسمی خود هستند. در طول شروع فعالسازی ماست سل، فسفوریلاسیون ITIMs تیروزین فسفاتازهای SHP-1 و SHP-2 را به خدمت میگیرد تا سیگنالهای اولیه ناشی از پیوند متقابل FcεRI را مسدود کند. با این حال، لیگاندهای بسیاری از این گیرنده ها هنوز شناسایی نشده اند.




