ابزار و وسایل آزمایشگاهی شامل، محلول ها کیت ها
کلیگلر آیرون آگار (Kligler’s Iron Agar (KIA)) اصول، رویه، نتایج
مقدمهای بر کلیگلر آیرون آگار
کلیگلر آیرون آگار برای تشخیص تخمیر کربوهیدرات استفاده میشود. واکنشهای KIA به شامل بودن یا نبودن یک باکتری خاص در خانواده باکتریهای انتروباکتریاسه (Enterobacteriaceae) کمک میکند. اگر یک ارگانیسم نتواند گلوکز را تخمیر کند، در KIA، واکنش قلیا در سطح – قلیا در عمق (Alkaline slant-Alkaline butt) (بدون تغییر) مشاهده میشود. این واکنش به تنهایی برای حذف یک باکتری از خانواده انتروباکتریاسه کافی است. KIA همچنین برای شناسایی احتمالی سالمونلا شیگلا (Salmonella Shigella) و سایر اعضای خانواده انتروباکتریاسه استفاده میشود.
ترکیب KIA با ترکیب تریپل شوگرآیرون آگار (Triple Sugar Iron Agar (TSI))) یکسان است با این تفاوت که 10 گرم ساکارز به TSI اضافه میشود.
ترکیب کلیگلر آیرون آگار
ترکیبات کلیدی کلیگلر آیرون آگار شامل پپتون (Peptone)، پودر آزمایشگاهی لمکو (Lemco) ، عصاره مخمر، کلرید سدیم، لاکتوز، گلوکز (دکستروز (dextrose))، فریک سیترات (Ferric citrate)، سدیم تیوسولفات (Sodium thiosulphate)، فنل (Phenol) قرمز و آگار است.
| ترکیبات | گرم بر لیتر |
| عصاره گوشت گاو | 3 |
| عصاره مخمر | 3 |
| پپتون | 15 |
| پپتون پروتئوز (Proteose peptone) | 5 |
| لاکتوز | 10 |
| گلوکز | 1 |
| فروس سولفات (Ferrous sulfate) | 0.2 |
| کلرید سدیم | 5 |
| سدیم تیوسولفات | 0.3 |
| آگار | 12 |
| فنل قرمز | 0.024 |
| آب مقطر معادل 1 لیتر | |
| PH نهایی: 7.4 | |
ترکیب چهار مشتق پروتئینی عصاره گوشت گاو، عصاره مخمر، پپتون و پپتون پروتئوز، KIA را از نظر ارزش غذایی بسیار غنی میکند. فقدان بازدارندهها اجازه رشد همه گونههای باکتریایی را به جز گونههای سختپسند (Fastidious) (به استثنای گونههای بیهوازی اجباری (Obligate anaerobe)) را میدهد.
گلوکز و لاکتوز منبع کربوهیدرات هستند و به طور مساوی در هر دو قسمت سطح و عمق لوله، توزیع میشوند. با این حال، لاکتوز در غلظت 10 برابر گلوکز وجود دارد. برخلاف TSI، ساکارز در KIA وجود ندارد. سدیم تیوسولفات منبع گوگرد است و فروس سولفات به عنوان آشکارساز سولفید هیدروژن (Hydrogen sulfide) عمل میکند.
اندیکاتور فنل قرمز در pH کمتر از 6.8، زرد رنگ است. از آنجایی که محیط تلقیح نشده در pH برابر 7.4 بافر میشود، مقادیر نسبتاً کمی از تولید اسید منجر به تغییر رنگ قابل مشاهدهای میشود.
آمادهسازی کلیگلر آیرون آگار (KIA)
کلیگلر آیرون آگار به صورت پودر خشک شده آماده برای استفاده، که توسط تامینکنندگان محیطهای کشت تهیه میشود، در دسترس است. این محیط معمولاً با غلظت 5.5 گرم در هر 100 میلیلیتر آب مقطر استفاده میشود (غلظت ممکن است بسته به سازنده متفاوت باشد).
- محیط کشت را طبق دستور سازنده آماده کنید. هنگامی که تا دمای 50 تا 55 درجه سانتیگراد دمای آن پایین آمد، آن را خوب هم بزنید و به مقدار 6 میلیلیتر در لولههای بزرگ (تقریباً 16 تا 160 میلیمتر) بریزید.
- با اتوکلاو (با درپوش باز) در دمای 121 درجه سانتیگراد به مدت 15 دقیقه آن را استریل کنید.
- اجازه دهید آگار مذاب در سطح محیط جامد شود. این امر منجر به ایجاد دو محفظه واکنش در یک لوله میشود.
- قسمت سطح محیط: در سرتاسر سطح خود در معرض اکسیژن هوا قرار داشته و هوازی است.
- قسمت عمق محیط: از هوا محافظت میشود و نسبتاً بیهوازی است.
- به محیط تاریخ و شماره دسته داده و در جای تاریک خنک یا در دمای 2 تا 8 درجه سانتیگراد نگهداری کنید.
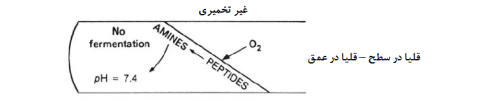
توجه: هنگام تهیه محیط کشت مهم است که عمق محیط بیشتر از طول سطح شیبدار یا حداقل مساوی با آن، هر کدام تقریباً 3 سانتیمتر، باشد تا این اثر دو محفظهای حفظ شود.
ماندگاری: حدود 3 هفته یا بیشتر به شرط اینکه درپوشهای لوله محکم بسته شوند و هیچ تغییری در ظاهر محیط وجود نداشته باشد که نشان دهنده آلودگی، خرابی یا تغییر pH باشد.
PH محیط کشت: این مقدار باید در محدوده 7.2 تا 7.6 در دمای اتاق باشد.
تلقیح KIA
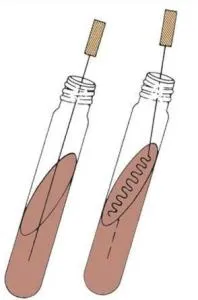
از یک سیم صاف برای تلقیح محیط KIA استفاده کنید، ابتدا به قسمت عمق محیط سیخونک بزنید و سپس سیم را در قسمت سطح به صورت زیگزاگ به کشت خطی دهید. پس از تلقیح، مطمئن شوید که لوله بدون درپوش باقی بماند.
اصول
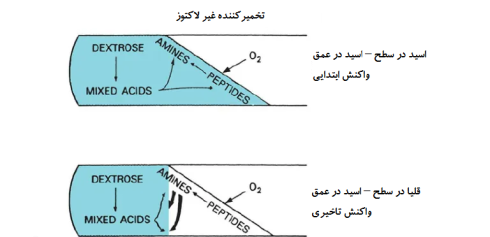
تخمیرکننده غیر لاکتوز
اگر لوله KIA با ارگانیسم تخمیرکننده گلوکز که نمیتواند از لاکتوز استفاده کند، تلقیح شود، فقط مقدار نسبتا کمی اسید از تخمیر با غلظت 0.1 درصد گلوکز در محیط، به دست میآید.
در طی 8 تا 12 ساعت اول انکوباسیون، حتی این مقدار اسید ممکن است برای تبدیل رنگ قسمت عمق و سطح به زرد کافی باشد.
با این حال، ظرف چند ساعت آینده، ذخایر گلوکز به طور کامل تمام میشود و باکتریها شروع به تخریب اکسایشی (Oxidative degradation) اسیدهای آمینه در قسمت سطح لوله که در آن اکسیژن وجود دارد، میکنند. این امر منجر به آزاد شدن آمینهایی میشود که به زودی مقادیر کم اسید موجود در سطح لوله را خنثی میکنند. در 18 تا 24 ساعت، PH کل سطح به pH قلیایی باز میگردد و رنگ به قرمز باز میگردد.
با این حال، در قسمت عمق لوله (بخش بیهوازی)، تخریب اسید آمینه برای خنثیسازی اسید تشکیل شده کافی نیست و محیط زرد باقی میماند.
بنابراین، واکنش قلیا در سطح – اسید در عمق در KIA یک شاخص مهم است که نشان میدهد ارگانیسم مورد آزمایش یک تخمیرکننده غیر لاکتوز است.
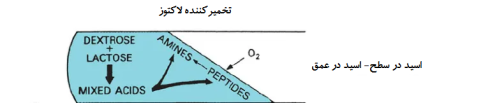
تخمیرکننده لاکتوز
اگر لوله KIA با ارگانیسم تخمیرکننده لاکتوز تلقیح شود، حتی اگر گلوکز بعد از 8 تا 12 ساعت اول به طور کامل مصرف شود، تخمیر ادامه مییابد. زیرا ارگانیسم قادر به استفاده از لاکتوز (که 10 برابر گلوکز غلظت دارد) میباشد.
در نتیجه اگر لوله در پایان 18 تا 24 ساعت بررسی شود، میبینیم که تولید اسید از تخمیر لاکتوز هنوز در حال انجام است، و هر دو قسمت سطح و عمق لوله زرد رنگ به نظر میرسند که منجر به واکنش اسید در سطح – اسید در عمق میشود.
نتایج
باکتریهایی که در KIA رشد میکنند سه نوع واکنش کلی ایجاد میکنند:
بدون تغییر در محیط یعنی قلیا در سطح – قلیا در عمق: بدون تخمیر کربوهیدرات به دلیل وجود باسیلهای گرم منفی غیرتخمیری (جاندارانی که قادر به تولید اسید از تخمیر گلوکز یا لاکتوز نیستند). به عنوان مثال باکتری سودوموناس آئروژینوزا (Pseudomonas aeruginosa).
تخمیرکننده غیرلاکتوز یعنی قلیا در سطح – اسید در عمق: گلوکز تخمیر میشود اما لاکتوز نه. این ویژگی برای باکتریهای غیرتخمیرکننده لاکتوز، مانند گونههای شیگلا است. در ابتدا، تخمیرکننده غیرلاکتوز، هر دو قسمت سطح و عمق محیط را از طریق تخمیر گلوکز، اسیدی میکند، اما PH قسمت سطح به pH قلیایی باز میگردد، زیرا آمینهای قلیایی از دکربوکسیلاسیون اکسایشی (Oxidative decarboxylation) پپتیدهای (Peptide) (مشتقشده از پروتئین موجود در محیط) نزدیک سطح، تشکیل میشوند.
تخمیرکننده لاکتوز یعنی اسید در سطح – اسید در عمق: هر دو قسمت عمق و سطح لوله توسط باکتریهای تخمیرکننده لاکتوز به طور کامل و دائمی اسیدی میشوند. گلوکز و لاکتوز هر دو تخمیر میشوند. این ویژگی باکتریهای کلیفرم (coliform) تخمیرکننده لاکتوز، مانند گونههای باکتریایی اشریشیا کلی (Escherichia coli) و کلبسیلا-انتروباکتر (Klebsiella–Enterobacter)، میباشد.
تولید گاز: وجود فضای خالی در پایین لوله و یا وجود گپ در آگار در وسط لوله، نشان دهنده تولید گاز(CO2) توسط ارگانیسم است.
تولید H2S: وجود رنگ سیاه در عمق لوله نشان دهنده تولید سولفید هیدروژن (H2S) میباشد. گاهی اوقات قسمت عمق لوله کاملا سیاه میشود. در چنین حالتی، فرض میشود که قسمت عمق لوله اسیدی است (رنگ زرد به دلیل تولید H2S پوشانده میشود). باکتریهای غیر تخمیرکننده لاکتوز و مولد سولفید هیدروژن (مانند گونههای سالمونلا (Salmonella)، گونههای سیتروباکتر (Citrobacter) و گونههای پروتئوس (Proteus))، حالت قلیا در سطح – اسید در عمق را تولید میکنند.
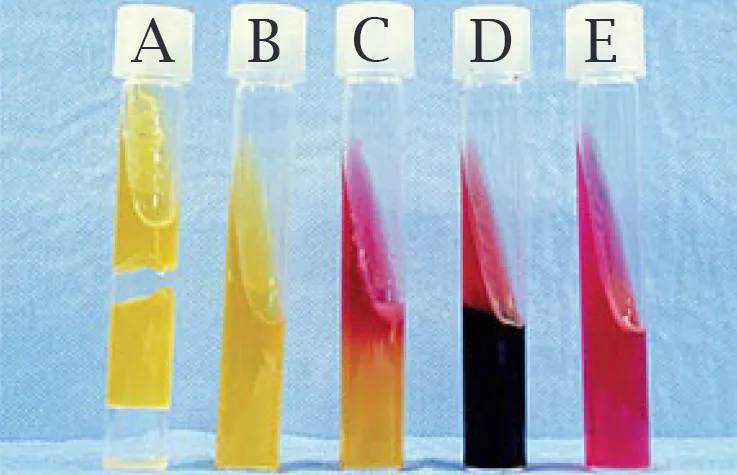
لولههای KIA با چندین الگوی واکنش
A: اسید / اسید، گاز؛ B: اسید/اسید، بدون گاز؛ C: قلیایی/اسیدی؛ D: قلیایی / اسیدی H2S+؛ E: قلیایی / قلیایی
ارگانیسمها و واکنشهایشان در KIA
| H2S | گاز | واکنشها
(قرمز= قلیا، زرد=اسید) |
نام ارگانیسم |
| – | – | قلیا/قلیا | Pseudomonas aeruginosa |
| –
– |
+
+ |
اسید/اسید
قلیا/اسید |
E.coli AD Group |
| – | – | قلیا/اسید | Shigella species (S.dysenteriae, S.flexneri, S.boydii, and S. sonnei) |
| + | – | قلیا/اسید | Salmonella Paratyphi A |
| + | + | قلیا/اسید | Salmonella Paratyphi B |
| + | + | قلیا/اسید | Salmonella Paratyphi C |
| – | + | قلیا/اسید | Salmonella Typhi |
| d | +
(ضعیف) |
قلیا/اسید | Other Salmonella serovars |
| – | ++ | اسید/اسید | Klebsiella pneumonia |
| – | ++ | اسید/اسید | Klebsiella oxytoca |
| – | ++ | اسید/اسید | Klebsiella (formerly Enterobacter) aerogenes |
| – | ++ | اسید/اسید | Enterobacter cloacae |
| + | + | اسید/اسید یا قلیا/اسید | Citrobacter freundii |
| – | + | قلیا/اسید | Serriatia mercescens |
| + | -/+ | قلیا/اسید | Proteus vulgaris |
| + | + | قلیا/اسید | Proteus mirabilis |
| – | + | قلیا/اسید | Morganella morganii |
| – | – | قلیا/اسید | Yersinia enterocolitica |
راهنمای جدول:
+: 90٪ یا بیشتر از سویهها مثبت هستند.
-: 90٪ یا بیشتر از سویهها منفی هستند.
++: واکنش مثبت قوی.
d: سویههای مختلف نتایج متفاوتی میدهند.
از آنجایی که Vibrio cholerae، گلوکز و همچنین ساکارز را تخمیر میکند، حالت قلیا در سطح – اسید در عمق در KIA مشاهده میشود. اما در محیط کشت تریپل شوگرآیرون آگار حالت اسید در سطح – اسید در عمق دیده شده و گاز و H2S تشکیل و تولید نمیشود.
از آنجایی که V. cholerae، گلوکز و همچنین ساکارز را تخمیر میکند، در KIA قلیا در سطح – اسید در عمق مشاهده میشود، اما حالت اسید در سطح – اسید در عمق در محیط کشت تریپل شوگرآیرون آگار دیده میشود.
مطالعات بیشتر:
تست CAMP: اساس، کاربردها، روش و تفسیر نتایج
مترجم: فاطمه فریادرس