دستهبندی نشده
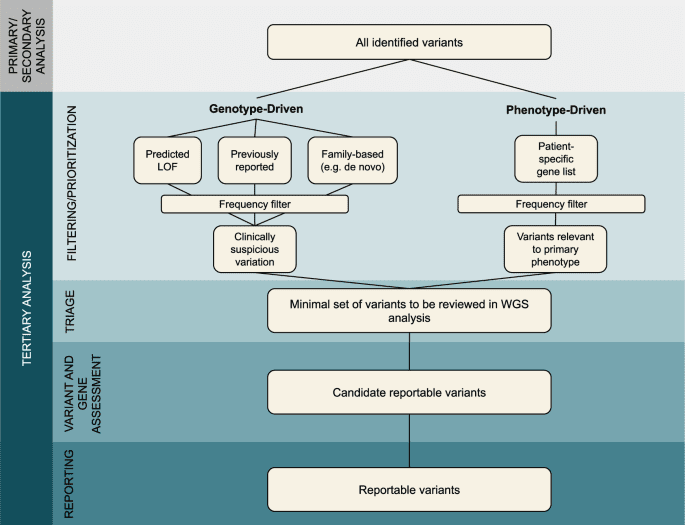
Filtering و Prioritization واریانت ها
توالی یابی کل ژنوم و کل اگزوم اطلاعات زیادی را برای شناسایی بالقوه علت بیماری در یک فرد فراهم می کند. در واقع، یک اگزوم منفرد ده ها هزار واریانت دارد به طور تقریبی 20000 SNV در یک اگزوم انسانی وجود دارد که شامل انواع مترادف و غیر مترادف می شود. روشهای سنتی برای اولویتبندی و فیلتر کردن واریانت ها در این مجموعههای بزرگ اغلب ضعیف عمل کرده و بسیاری از واریانت ها حتی تشخیص داده نمیشوند. الگوریتم های اولویت بندی معمولاً واریانت ها را بر اساس مضر بودن ارزیابی می کنند.
الگوریتمهای سنتی اولویتبندی واریانت ها اغلب فقط به تأثیر اسید آمینه یا حفظ آن در یک موقعیت خاص نگاه میکنند و به فرکانس آلل یا تأثیر کل در سطح ژن نگاه نمیکنند. اولویت بندی واریانت ها یک گام حیاتی در کشف انواع علّی به منظور شناسایی جهش های عامل بیماری است. این به این دلیل است که نتایج فناوریها و کاربردهای NGS، مانند توالییابی کل اگزوم (WES) یا توالییابی کل ژنوم (WGS)، اغلب شامل فهرستی از چندین هزار واریانت با اهمیت ناشناخته است که بسیاری از آنها ثابت شدهاند.
در طی آنالیز داده های NGS تا این مرحله بسته به حجم ناحیه توالی یابی شده تعداد بسیار زیادی از واریانت ها در طی پروسه variant calling به دست می آید که حال می بایست از بین این تعداد عظیم از تغییرات تنها تغییری که با بیماری زایی فرد مذکور ارتباط دارد انتخاب شود زیرا که بسیاری از تغییرات به دست آمده خوش خیم بوده و با فنوتیپ خاصی از یک بیماری ارتباط ندارد (حداقل فعلا با اطلاعات در دسترس ما در دیتابیس ها!!!!) اولویت بندی واریانت ها روشی ساده است که معمولاً در مطالعات بالینی استفاده می شود تا تعداد واریانت های ژنتیکی که نیاز به ارزیابی دستی دارند را کاهش دهد.
Variant filteringیک مرحله تجزیه و تحلیل در NGS است که شامل شناسایی واریانت های بسیار مطمئن و حذف واریانت هایی است که به اشتباه خواند شده اند. فیلترها که اغلب به صورت تدریجی یا به صورت موازی اعمال می شوند، ممکن است زمان گیر و ردیابی آنها دشوار باشد. فیلتر کردن می تواند منجر به حذف زودهنگام یا سهوی برخی از واریانت های کال شده و یا ایجاد واریانت های مثبت کاذب شود. تفسیر نتایج در زمینه انسانی معمولاً توسط افراد واجد شرایط مانند متخصص ژنتیک بالینی و/یا مشاور ژنتیک انجام می شود.
وظیفه آنها شامل جمع آوری تمام اطلاعات موجود از بیمار ، از جمله سابقه خانوادگی بیماری و تطبیق ژنوتیپ بیمار با فنوتیپ بالینی است. بسته به نوع بیماری ، آنها حتی ممکن است مشخصات ژنتیکی والدین را برای درک وراثت آلل های بیماری احتمالی درخواست کنند. اینجاست که اهمیت Annotation و فیلترینگ نمایان می شود که هدف اصلی کاهش بار کاری افرادی است که تفسیر را انجام می دهند. برای استانداردسازی فرایند تفسیر و امکان رویکرد سیستماتیک تر ، ACMG و AMP مجموعه ای از دستورالعمل ها را برای تشخیص بیماری های مندلی تدوین کرده اند.




با سلام و تشکر از مطالب مفیدتان.