اطلاعات عمومی, ویکی ژن
سلول های بنیادی: منابع، انواع و موارد استفاده در تحقیقات
سلول های بنیادی سلول های تمایز نیافته ای هستند که قادر به تجدید خود یا تمایز به سلول ویژه هستند. آنها در مناطقی از بدن وجود دارند که به عنوان تو رفتگی های بیولوژیکی شناخته می شوند و برای رشد در دوران کودکی و هموستاز در تمام بزرگسالی ضروری هستند.
بنابراین ، درک فرآیندهای بیولوژیکی زیربنای این سلول ها می تواند پیامدهای بی نظیری در پزشکی احیا ، درمان بیماری و بهبود آسیب داشته باشد. این مقاله به توصیف هر نوع سلول بنیادی و همچنین برخی از اکتشافات اصلی و مهمترین کاربردهای سلولهای بنیادی در پزشکی و تحقیقات می پردازد.
سلول های بنیادی چیست؟
مشخصه اصلی سلولهای بنیادی این است که آنها می توانند در طی رشد و نمو به چندین نوع سلول مختلف متمایز شوند. این نه تنها در طول زندگی زودهنگام ، بلکه در پی آسیب دیدگی که سلولهای بنیادی با دوباره پر کردن سلولهای آسیب دیده یا مرده به عنوان مکانیسم ترمیم داخلی عمل می کنند ، دارای پیامدهایی است. دو ویژگی اصلی سلول های بنیادی وجود دارد که آن را منحصر به فرد می کند.
طبیعت غیر تخصصی
سلولهای بنیادی برای داشتن ساختارها و عملکردهای خاص تخصصی نیستند. به عنوان مثال ، یک سلول بنیادی غیرتخصصی نمی تواند اکسیژن را مانند گلبول قرمز حمل کند یا خون را مانند سلول قلب پمپاژ کند. با این حال ، با دریافت سیگنال های مناسب ، می تواند به انواع مختلف سلول های تخصصی مانند سلول های عضلانی ، سلول های خونی و غیره تبدیل شود.
پتانسیل تمایز
روند تمایز به سلولهای بنیادی غیرتخصصی اجازه می دهد توابع و خواص خاصی را بدست آورند. سیگنال های نشانه این انتقال می توانند ذاتی (از داخل سلول) یا خارجی (از خارج سلول) باشند. سیگنال های بیرونی که می توانند این انتقال را تحریک کنند ممکن است به صورت نشانه های مکانیکی یا شیمیایی از سلول های همسایه باشد.
پتانسیل تمایز سلول های بنیادی در اندام های مختلف متغیر است. برخی از اندام ها ، از جمله روده و مغز استخوان ، به طور مرتب برای ترمیم و دوباره پر کردن سلول های آسیب دیده تقسیم می شوند. با این حال ، در اندامهایی مانند پانکراس و قلب فراوانی تقسیم و تمایز سلولهای بنیادی بسیار کمتر است.

سلول های بنیادی از کجا آمده اند؟
بند ناف انسان
خون بند ناف را می توان پس از تولد از بند ناف نوزاد جمع کرد و از سلول های بنیادی خونساز و مزانشیمی تشکیل شده است. سلول های بنیادی خونساز می توانند سلول های قرمز خون و سلول های سیستم ایمنی بدن را تشکیل دهند ، در حالی که سلول های بنیادی مزانشیمی می توانند استخوان ، غضروف و سایر انواع بافت ها را تولید کنند. همچنین می توان خون بند ناف را برای استفاده در آینده در بانک های خون بند ناف جمع آوری و ذخیره کرد.
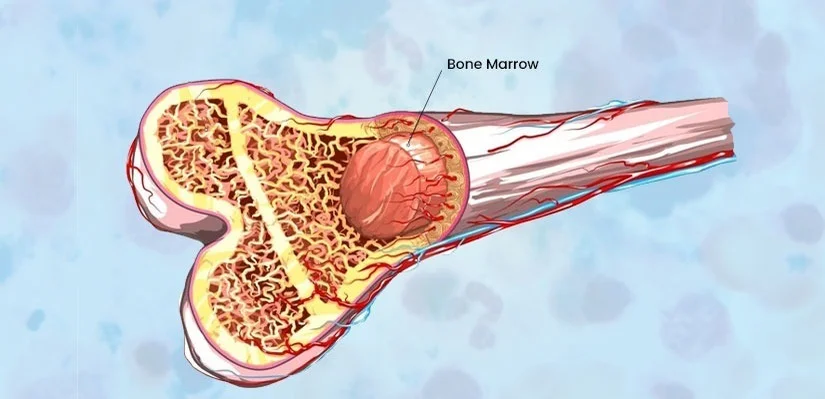
مغز استخوان
مغز استخوان یک بافت ژلاتینی نرم است که در مرکز استخوان ها یافت می شود. سلولهای بنیادی مزانشیمی برای اولین بار در مغز استخوان یافت شد و هنوز هم بیشترین استفاده از سلولهای بنیادی مزانشیمی است. متعاقباً سلولهای بنیادی خونساز یا خونی نیز در مغز پیدا شد ، و آن را به کاندیدایی جذاب برای داروهای احیا و اهداف درمانی تبدیل کرده است.
بافت چربی
سلولهای بنیادی مشتق از بافت چربی سلولهای مزانشیمی هستند که توانایی تجدید خود و قدرت چندانی دارند. آنها می توانند علاوه بر انواع سلولهای دیگر ، به سلولهای چربی ، سلول های غددی ، میوسیت ها ، استئوبلاست ها و سلول های عصبی متمایز شوند. نشان داده شده است که این سلولهای بنیادی نقش مهمی در زمینه های بازسازی و مهندسی بافت برای توسعه درمانهای جدید دارند.
مایع آمنیوتیک
مایع آمنیوتیک مایعی است که اطراف آمنیون یا کیسه ای است که جنین را در بر می گیرد. هم غشای آمنیوتیک و هم مایع آمنیوتیک منابع خوبی از سلولهای بنیادی جنینی هستند که می توانند تکثیر و هر نوع سلول را تشکیل دهند. اگرچه مایع آمنیوتیک و غشا معمولاً پس از تولد دور ریخته می شود ، اما اخیراً برای استفاده درمانی در آینده منجمد می شوند.
انواع سلول های بنیادی
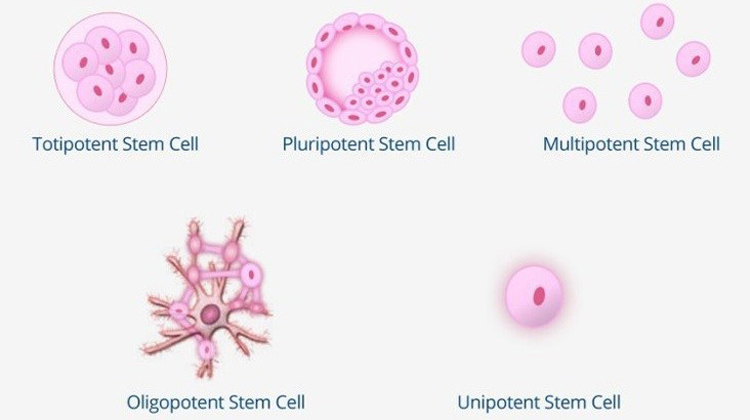
قدرت سلول های بنیادی
بر اساس پتانسیل تمایز آنها ، سلولهای بنیادی را می توان به چهار نوع طبقه بندی کرد:
- توانمند (totipotent)
- پرتوان (pluripotent)
- چند توان (multipotent)
- ناتوان (unipotent)
سلول های توانمند
سلولهای توانا می توانند به انواع سلولها متمایز شوند. به عنوان مثال ، زیگوتی که در هنگام لقاح تخمک و چند سلول اول پس از تقسیم تشکیل شده است ، توانایی بالایی دارد و امکان تبدیل شدن به انواع سلولهای بدن را دارد.
سلول های پرتوان
سلولهای پرتوان تقریباً به انواع سلولها تبدیل می شوند. اینها شامل سلولهای بنیادی جنینی ، سلولهای مشتق شده از لایه های جوانه ای (مزودرم ، اکتودرم ، آندودرم) و سلولهای تشکیل شده در مراحل اولیه تمایز سلولهای بنیادی جنینی است.
سلول های Multipotent ، oligopotent و unipotent
سلولهای Multipotent می توانند به سلولهای نزدیک به هم تقسیم شوند. به عنوان مثال ، سلول های بنیادی خونساز می توانند به سلول های قرمز خون ، گلبول های سفید و پلاکت تبدیل شوند. سلولهای اوليپوپوتنس قادرند به چند نوع سلول تبديل شوند و شامل سلولهای بنيادی لنفوئيدي يا ميلوئيدی باشند ، در حالیکه سلولهای unipotent مانند سلولهای بنیادی عضله فقط به سلولهایی از نوع خود تبديل می شوند.
منابع سلول های بنیادی
سلولهای بنیادی را می توان بر اساس منشا آنها بین اوایل (یا جنینی) و بالغ تقسیم کرد.
سلول های بنیادی جنینی
سلولهای بنیادی جنینی در توده سلولی داخلی بلاستوسیست پس از پنج روز رشد یافت می شوند. این سلول ها به طور بالقوه جاودانه هستند و از جنین ها گرفته می شوند قبل از اینکه خود را در رحم جای دهند. این سلول ها به طور معمول 4-5 روز از عمر آنها گذشته است و بلاستوسیست ها نامیده می شوند – یک گلوله میکروسکوپی توخالی از سلول ها.
سلول های بنیادی بالغ
سلولهای بنیادی بالغ سلولهای تمایز نیافته ای هستند که توانا یا پرتوان هستند. این سلولها در مکانهای مختلف بدن یافت می شوند و به حفظ تعداد سلولهای سالم و دوباره پر کردن سلولهای در حال مرگ یا زخمی کمک می کنند.
سلول های pluripotent القایی
اخیراً ، دسته جدیدی از سلولهای بنیادی ظهور کرده است که از سلولهای سوماتیک سرچشمه می گیرند و می توانند توسط دانشمندان مجدداً برنامه ریزی شوند تا به مرحله pluripotent خود برسند. این کار با دستکاری بیان مجموعه ای از ژن ها انجام شد. از آنجا که سلولهای سوماتیک در این گروه به سلولهای pluripotent تبدیل می شوند ، اصطلاحاً به آنها “سلولهای pluripotent القا شده” گفته می شود.
اصل و نسب سلول های بنیادی چیست؟
سلولهای بنیادی معمولاً دو نوع تقسیم سلولی دارند: متقارن و نامتقارن. در تقسیم متقارن ، دو سلول دختر یکسان با ویژگی های سلول بنیادی پس از تقسیم سلول تولید می شود. در تقسیم نامتقارن ، یک سلول بنیادی و یک سلول پیش ساز تولید می شود.
سلولهای مولد محدودیت بالقوه ای برای تجدید خود دارند و پس از چندین دوره تقسیم ، سلولهای بالغ متمایز ایجاد می کنند. با این حال ، تعیین مکان سلولهای بنیادی اغلب دشوار است زیرا بافتها حاوی تعداد زیادی از چندین نوع سلول هستند.
تجزیه و تحلیل نسب یکی از روش هایی است که برای مقابله با این مشکل استفاده می شود. در این روش ، یک سلول منفرد به گونه ای علامت گذاری شده است که نه تنها سلول هدف بلکه سلول های دختر آن را نیز علامت گذاری می کند. بنابراین ، می توان تعداد ، محل ، حرکت و طول عمر سلول های بنیادی و سلول های دخترش را ردیابی کرد. تجزیه و تحلیل نسب سلول های بنیادی به کشف و شناسایی تو رفتگی سلول های بنیادی که جایگزین سلول ها در طول عمر یک بافت هستند ، کمک می کند.
اکتشافات برجسته در تاریخ تحقیقات سلول های بنیادی
یکی از آزمایشات اولیه در این زمینه توسط سر جان گوردون در دوره دکترای خود انجام شد. در سال 1962. او هسته جنین قورباغه در حال رشد را در مرحله بلاستول برداشته و آن را به سلول تخم مرغی كه هسته از آن خارج شده بود تزریق كرد.
در بیشتر موارد ، تخمک می تواند به صورت قورباغه در آید ، نشان می دهد که هسته های سلول های تمایز یافته هنوز پتانسیل رشد در هر سلول را دارند. این مطالعه اساس شبیه سازی باروری را تشکیل داد که منجر به ایجاد دالی ، گوسفند شبیه سازی شده شد.
کشف مهم دیگر کشت سلولهای بنیادی جنینی از بلاستوسیستهای موش در سال 1981 بود. متعاقباً سلولهای بنیادی جنینی نیز از بلاستوسیستهای انسانی کشت شدند.
هنگامی که شینیا یاماناکا و همکارانش توانستند با معرفی مجموعه ای از 24 فاکتور رونویسی سلولهای سوماتیک را به سلولهای بنیادی پرتوان القا کنند ، یک کشف مهم کشف شد. وی در سال 2012 به همراه سر جان گوردون برای این کشف جایزه نوبل پزشکی دریافت کرد.
مسائل اخلاقی مربوط به سلولهای بنیادی جنینی
اخیراً ، از سلولهای توانمند ناشی از اتولوگ برای درمان انحطاط ماکولا در مطالعات انسانی استفاده شده است. در مطالعه دیگری ، اپیدرم در بیمار مبتلا به اپیدرمولیز بولوزا به طور کامل بازسازی شد. همچنین پیشرفت هایی در ارگانوئیدها ، ساختارهای سه بعدی که سعی در تقلید از ساختار و عملکرد اندام ها دارند ، صورت گرفته است.
این ارگانوئیدها می توانند از سلولهای بنیادی ، سلولهای توانمند القا شده ، نمونه های بیوپسی و غیره تولید شوند و برای پیوند بافت استفاده شوند. ایجاد ارگانوئیدها سوالات اساسی درباره مالکیت ، ذخیره سازی ، اهدا کنندگان و حقوق دستکاری این ساختارها ایجاد کرده است. اگرچه از نظر عملکرد کاملاً بالغ نیستند ، اما تا حدی که می توان به ارگانوئیدها اجازه بلوغ داد ، باید بحث شود.
“قانون 14 روزه” توسط انجمن بین المللی تحقیقات سلولهای بنیادی (ISSCR) وضع شده است که طبق آن تحقیقات سلولهای بنیادی روی جنین ها باید در دو هفته پس از لقاح خاتمه یابد. این زمان با ظهور رگه ابتدایی ، اولین ساختار مغز و نخاع ارتباط دارد.
پیشرفت در ویرایش ژن همچنین درهای مختلفی را برای سالات متقابل اخلاقی باز کرده است ، جایی که ISSCR دستور داده است که تمام مراحل تحقیقات سلول های بنیادی و تحقیقات ویرایش ژن باید شفاف باشد. با این حال ، اخیراً گزارش های خبری منتشر شده است که ادعا می کند اولین نوزادان ویرایش شده با ژن در چین ساخته شده اند ، اما این ادعا هنوز نیاز به اثبات دارد.
مسائل فنی مرتبط با سلول های بنیادی توانمند القاشده
مطالعات نشان می دهد که سلولهای توانمند القاشده تنوع بیشتری نسبت به سلولهای بنیادی جنینی دارند. این تفاوت پیشنهاد شده است که از حافظه اپی ژنتیک ، زمینه ژنتیکی ، برنامه ریزی مجدد و غیره ناشی می شود. دو مطالعه نشان می دهد که سلول های موجود در مرحله انتقالی تفاوت قابل توجهی با سلول های اصلی و کاملاً برنامه ریزی مجدد دارند.
در حالی که بسیاری از سلولهای پرتوان القا شده از نظر مورفولوژی و بیان ژن مشابهی را نشان می دهند ، اما آنها همچنین از کیفیت تمایز ضعیف ، سرعت پایین رشد ، خطاهای در رونویسی ، متیلاسیون DNA و غیره برخوردار هستند. همچنین یکی از عواملی که برای برنامه ریزی مجدد سلولهای سوماتیک استفاده می شود ، KLF4 ، می تواند نوروژنز سلولهای بنیادی توانمند القاشده را مختل کند. بنابراین ، درک بیشتر از برنامه نویسی القایی مورد نیاز است.
کاربردهای اصلی سلول های بنیادی
اهداف درمانی
جدا از پیوند مغز استخوان، روش های درمانی سلول های بنیادی هنوز در مراحل رشد هستند. تلاش برای استفاده از سلولهای بنیادی در معالجه دیابت نوع I، بیماری پارکینسون، بیماری هانتینگتون، سلیاک، نارسایی قلبی و غیره وجود دارد. سلول های بنیادی مغز استخوان می توانند پس از پرتودرمانی در ازدیاد گروه های مختلف خون کمک کنند.
جایگزینی پوست
در حال حاضر از سلولهای بنیادی برای رشد پوست از موهای کنده شده بیمار استفاده می شود. فولیکول های مو حاوی سلول های بنیادی پوست یا کراتینوسیت ها هستند و می توان این سلول ها را جدا و کشت کرد تا یک صفحه اپیتلیال رشد کند. این روش می تواند به کاهش نیاز به استفاده از پیوند پوست از افراد دیگر کمک کند و احتمال رد شدن را کاهش دهد.
پیوند سلول مغز
از سلولهای بنیادی می توان برای تولید دوپامین استفاده کرد – ماده شیمیایی که در بیمارانی که از بیماری پارکینسون رنج می برند ، وجود ندارد. با این حال ، در برخی موارد ، بیماران دچار عوارض جانبی می شوند ، که حاکی از وجود مقادیر بسیار بالای دوپامین یا حساسیت بیش از حد در این روش است.
همچنین بخوانید…
خدمات کشت سلول آزمایشگاه ژنیران





بسیار عالی و کاربری